Incyte和 MorphoSys AG公司近日宣布,欧盟委员会 (EC) 已授予 Minjuvi ®(tafasitamab)与来那度胺(lenalidomide)联合用药,然后是 Minjuvi 单药治疗,用于治疗不适合自体干细胞移植(ASCT)的复发性或难治性弥漫性大 B 细胞淋巴瘤(DLBCL)成人患者的有条件营销授权。EC 的决定是在欧洲药品管理局人用药品委员会 (CHMP) 于 2021 年 6 月收到的积极意见之后做出的,该意见建议对 Minjuvi 进行有条件的营销授权。
Minjuvi ®(tafasitamab-cxix)
有条件批准基于 L-MIND 研究的结果,该研究评估了 Minjuvi 与来那度胺联合用于治疗不符合自体干细胞移植 (ASCT) 的复发性或难治性 DLBCL 患者的安全性和有效性。
结果显示,由独立审查委员会评估的最佳客观缓解率 (ORR) 为 56.8%(主要终点),包括 39.5% 的完全缓解率 (CR) 和 17.3% 的部分缓解率 (PR)。 在最短随访 35 个月(次要终点)后,中位缓解持续时间 (mDOR) 为 43.9 个月。
Minjuvi 与来那度胺一起显示出具有临床意义的反应,并且副作用是可控的。Minjuvi 的警告和注意事项包括输液相关反应、骨髓抑制,包括中性粒细胞减少症和血小板减少症、感染和肿瘤溶解综合征。
关于弥漫性大B细胞淋巴瘤
DLBCL是全球成人最常见的非霍奇金淋巴瘤类型,占所有病例的40%,其特征为淋巴结、脾脏、肝脏、骨髓或其他器官中恶性B细胞团快速生长。这是一种侵袭性疾病,约三分之一的患者对初始治疗无反应,或在治疗后复发。在欧洲,每年约有16000名患者被诊断为复发或难治性DLBCL。
关于L-MIND
L-MIND试验是一项单臂、开放标签的2期研究(NCT02399085),研究了在复发或难治性弥漫性大B细胞淋巴瘤(DLBCL)患者中联合使用tafasitamab和来那度胺的情况,这些患者之前至少接受过一次但不超过三次治疗,包括抗CD20靶向治疗(如rituximab),且不适合接受高剂量化疗(HDC)或自体干细胞移植(ASCT)。该研究的主要终点是总体应答率(ORR)。次要结果指标包括应答持续时间(DoR)、无进展生存期(PFS)和总生存期(OS)。该研究于2019年5月初步完成。
关于 Minjuvi®(tafasitamab)
Tafasitatamab 是一种人源化 Fc 修饰的细胞溶解 CD19 靶向单克隆抗体。 Tafasitatamab 包含一个 XmAb®工程化 Fc(可结晶片段)结构域,它通过细胞凋亡和免疫效应机制介导 B 细胞裂解,包括抗体依赖性细胞介导的细胞毒性 (ADCC) 和抗体依赖性细胞吞噬作用 (ADCP)。
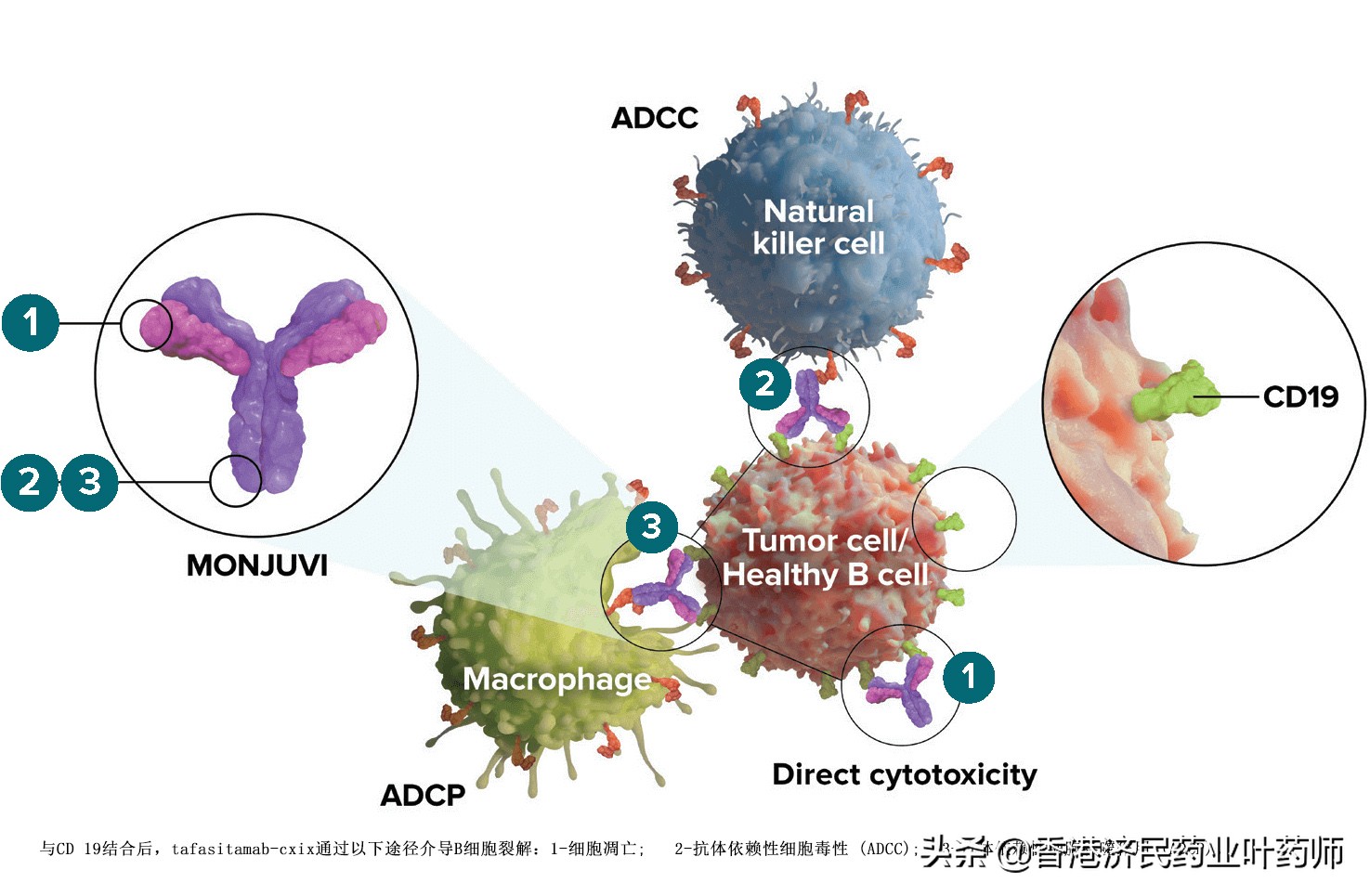
独特的三管齐下的作用机制
在美国,Monjuvi®(tafasitamab-cxix)被美国食品和药物管理局批准与来那度胺联合用于治疗未明确指定的复发性或难治性 DLBCL 成人患者,包括由低级别淋巴瘤引起的 DLBCL,以及 不符合自体干细胞移植 (ASCT) 的条件。 该适应症在基于总体反应率的加速批准下获得批准。 对该适应症的持续批准可能取决于验证性试验中对临床益处的验证和描述。
在欧洲,Minjuvi®(tafasitamab)与来那度胺联合使用,随后是 Minjuvi 单药治疗获得有条件批准,用于治疗不适合自体干细胞移植的复发性或难治性弥漫性大 B 细胞淋巴瘤 (DLBCL) 成人患者 (ASCT)。
在几项正在进行的联合试验中,正在对Tafasitamab作为B细胞恶性肿瘤的一种治疗方案进行临床研究。
在欧洲,每年约有16000名患者被诊断为复发或难治性DLBCL,其治疗方案历来有限,预后也很差。Minjuvi的获批为符合条件的DLBCL患者提供了一个新的、急需的治疗方案。
参考来源:Incyte and MorphoSys Announce the European Commission Approval of Minjuvi® (tafasitamab) in Combination With Lenalidomide for the Treatment of Adults With Relapsed or Refractory Diffuse Large B-Cell Lymphoma
注:本文旨在介绍医药健康研究,不作任何用药依据,具体用药指引,请咨询主治医师。