欢迎关注凯莱英药闻
2022年9月22日,葛兰素史克(“GSK”)和Spero Therapeutics(“Spero”)共同宣布,已就 Spero 正在开发的口服抗感染药物tebipenem HBr,达成独家许可协议;作为首个碳青霉烯类抗生素口服药物,tebipenem HBr可能治疗由某些细菌引起的复杂性尿路感染(cUTI),包括肾盂肾炎。

根据协议条款,GSK将获得独家授权,在除日本和其他亚洲国家以外的地区开发和商业化tebipenem HBr。Spero 将负责 tebipenem HBr 剩余 III 期临床试验的执行和费用;GSK 将负责额外临床开发的执行和费用,包括监管申报和商业化活动。在合作金额上,GSK 将向Spero 支付6600万美元的首付款,其余的潜在付款基于里程碑的完成情况;此外,GSK 将购买 900 万美元的Spero 普通股,不超过GSK 及其附属公司对Spero 19.99%的实益所有权。
关于Tebipenem HBr
Tebipenem HBr是一种 β-内酰胺类碳青霉烯类抗生素,自2009年由 Meiji Seika Pharm 在日本销售注射制剂以来,用于儿科感染且仅限于肺炎、中耳炎和鼻窦炎。碳青霉烯类是抗生素的一个重要子类,研究表明其在治疗耐药革兰氏阴性细菌感染方面是安全有效的。Tebipenem HBr 正在开发用于治疗 cUTI,如果获得批准,将成为第一个在美国获得上市批准的口服碳青霉烯类抗菌药物。目前,该药物已被美国 FDA 授予用于 cUTI 和急性肾盂肾炎治疗的合格传染病产品 (QIDP) 和快速通道指定。

2022年1月, FDA 已受理tebipenem HBr的NDA,治疗成人cUTI,包括致病微生物引起的急性肾盂肾炎。该NDA基于一项关键性全球多中心、随机、安慰剂对照3期临床试验ADAPT-PO,将1372例cUTI(含急性肾盂肾炎)患者,按1:1比例随机分配至每8小时口服一次600mg tebipenem HBr组和每24小时静脉注射1g厄他培南组,持续给药7至10天。结果显示:口服tebipenem HBr组对比静脉注射厄他培南组显示出非劣效性,且耐受性良好,安全性与静脉注射厄他培南组相似。

关于Spero
Spero 成立于2013年,总部位于美国马萨诸塞州剑桥市,是一家临床阶段的生物制药公司,专注于识别、开发和商业化细菌感染的新疗法,包括耐多药细菌感染和罕见疾病。其中,SPR720是一种新型口服治疗候选药物,用于治疗由非结核分枝杆菌感染引起的罕见的孤儿肺部疾病。SPR206是一种静脉给药的多粘菌素候选产品,该产品是从其增效剂平台开发的,用于治疗医院环境中的多重耐药革兰氏阴性菌感染。
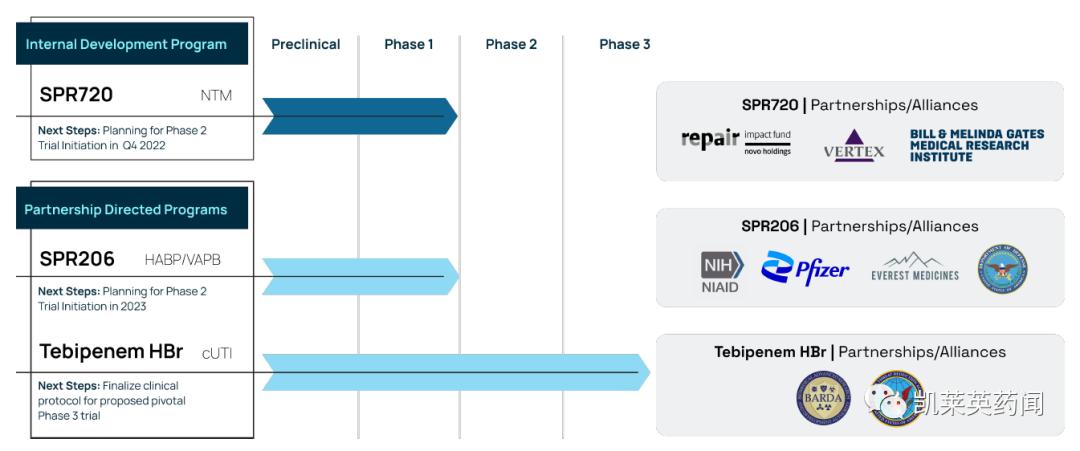
除tebipenem HBr外,该公司的其它在研产品,同样吸引了药企们的注意。2021年7月,辉瑞斥4000万美元投资Spero,并以8000万美元囊获SPR206的开发权益。而此前,国内企业云顶新耀已于2021年1月与Spero达成了一项许可协议的修订;根据该协议的修订内容,云顶新耀获得SPR206在大中华区、韩国和部分东南亚国家(以下简称“区域”)的相关专利权益。2019年1月,云顶新耀和Spero曾宣布一项合作协议,在上述区域对SPR206进行开发、制造和商业化。
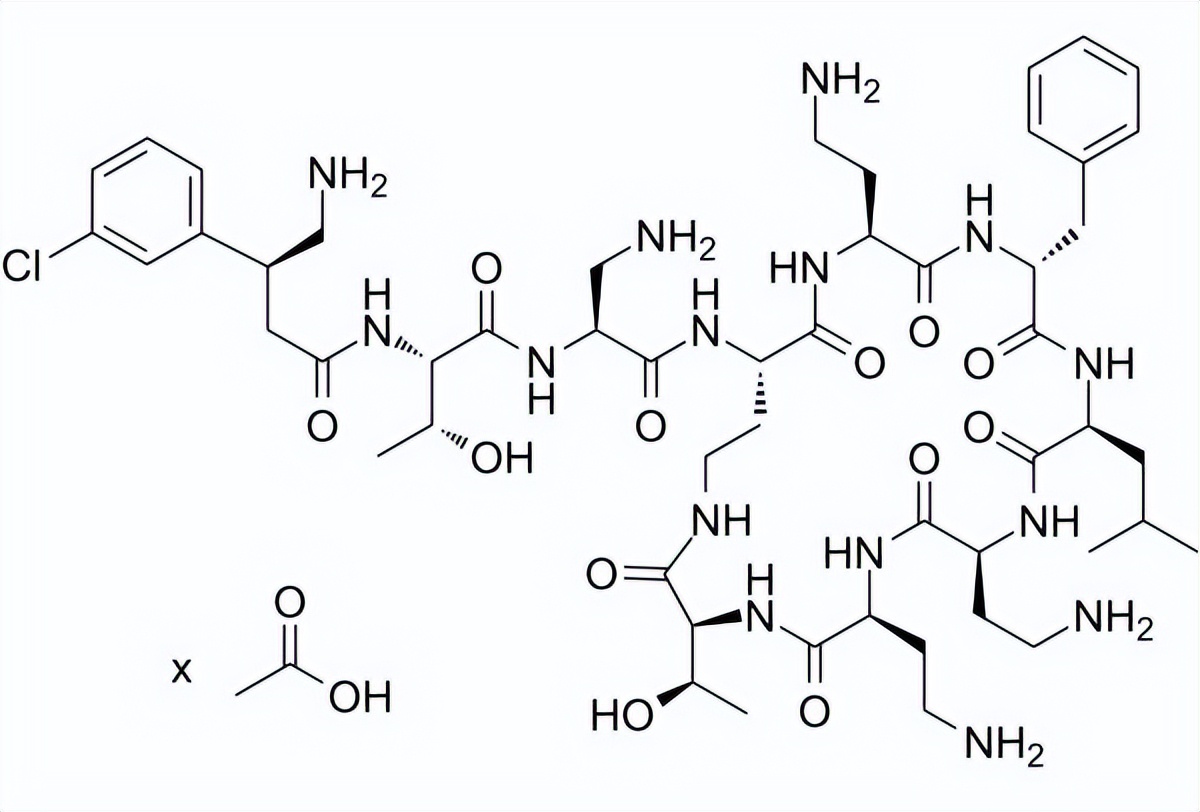
SPR206是一种多粘菌素类静脉给药抗生素,旨在治疗医院环境中的多重耐药革兰氏阴性感染。它通过与革兰氏阴性细菌的外细胞膜脂多醣(LPS)的成分结合,导致外膜完整性丧失和通透性增加。目前,该药物已完成首次人体1期临床试验,数据显示SPR206的耐受性良好,在预期治疗剂量下无肾毒性。

关于碳青霉烯类抗生素
碳青霉烯类抗生素是一类抗菌谱广、抗菌活性强的 β- 内酰胺类抗生素。由于内酰胺酶的稳定性和低毒性,碳青霉烯类抗生素已成为治疗严重细菌感染的最重要的抗菌药物之一。碳青霉烯类抗生素对需氧菌和厌氧菌有很强的抗菌作用,几乎杀死革兰氏阳性菌和革兰氏阴性菌,抗菌谱几乎覆盖临床所有常见的致病菌。然而,随着该类抗生素在临床治疗中的大剂量和不合理应用,碳青霉烯类耐药病原菌已普遍存在,这给临床用药带来很大困扰。
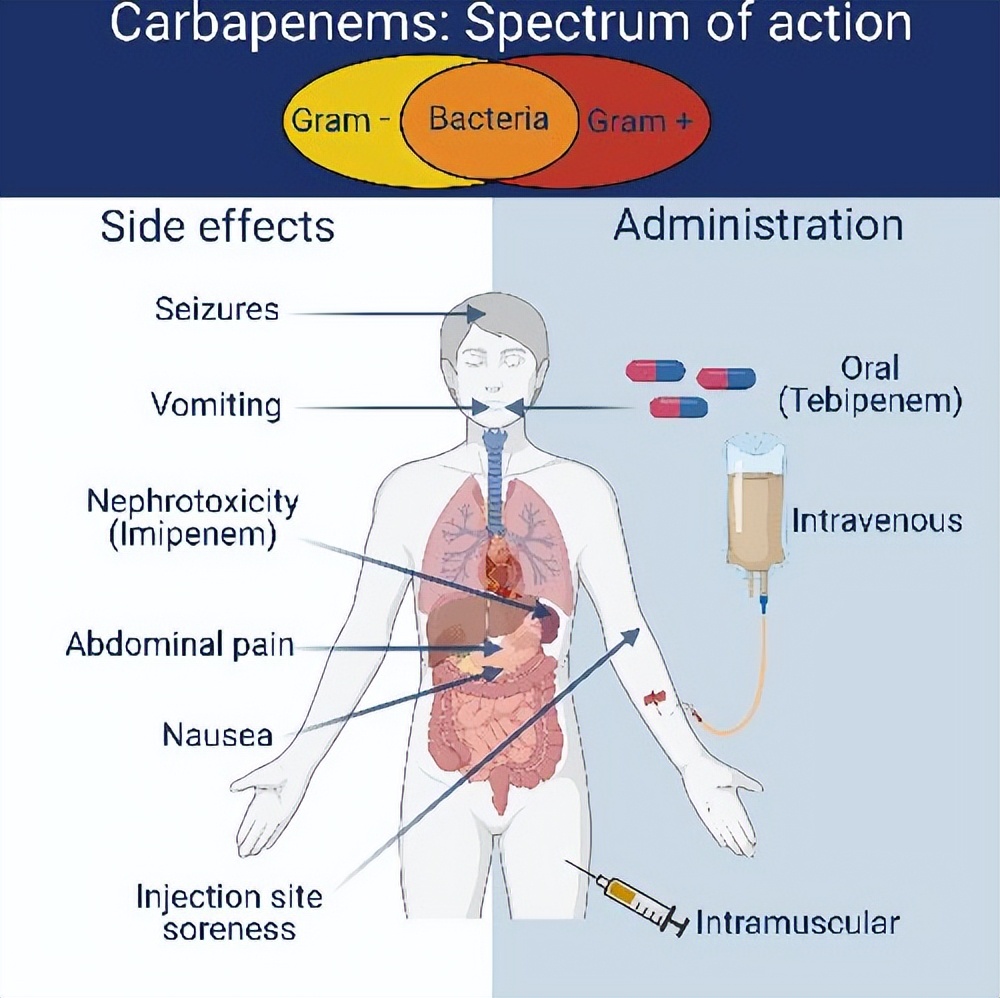
目前,国内外有近十种碳青霉烯类抗生素获批,其中应用最广泛的包括亚胺培南、帕尼培南、美罗培南等,且很多还处于研发阶段。
部分处于临床阶段的碳青霉烯类抗生素