在20世纪90年的外科医生记忆中,肝移植治疗转移性恶性肿瘤的结果十分不理想[1]。术后5年生存率不到两成,手术死亡率则高达30%[1];加上肝源短缺,且治疗费用高昂,很多外科医生放弃了将肝移植作为结直肠癌肝转移(colorectal cancer liver metastasis,CRLM)患者的治疗选项之一。
不久前,医学杂志JAMA Surgery上,来自挪威奥斯陆大学医院(Oslo University Hospital)单中心15年的数据,向外科界提供了关于肝移植治疗CRLM的鼓舞人心的研究结果。
在这一前瞻性的研究中,有50例CRLM患者接受肝移植治疗:
- 低肿瘤负荷(<10个病灶;最大肿瘤<5.5cm;n=21)患者的5年生存率为72.4%;
- 接受肝移植的高肿瘤负荷(>9个肿瘤,最大肿瘤>5.5 cm)患者的5年生存率为33.4%[2]。
这些数据虽然是初步的,但仍有积极意义,将鼓励有条件的地区或中心以临床试验或登记的形式重新评估移植治疗CRLM的效果。
新探索:「转移性大肠癌」哪种治疗方式总生存期更长?
对于高肿瘤负荷CRLM患者,门静脉栓塞术(portal vein embolization,PVE)后肝切除——即两期肝切除术(two-stage hepatectomy,TSH)和肝移植,哪种治疗方式总生存期(overall survival. OS)更长?
研究设计与发现: 搜集了本中心院50例接受肝移植术的CRLM患者数据(2006年11月至2019年8月),将其与同期53例接受PVE或TSH的患者进行比较。
在这项比较有效性研究中,肝移植组和TSH组的所有患者的东方肿瘤协作组(Eastern Cooperative Oncology Group)得分为0到1,年龄小于72岁,并且在肝移植或PVE前切除了原发肿瘤。所有患者均接受标准化化疗。超过50%的肝移植组患者在移植时已接受过二线或后线化疗。
- PVE组患者基线特征:
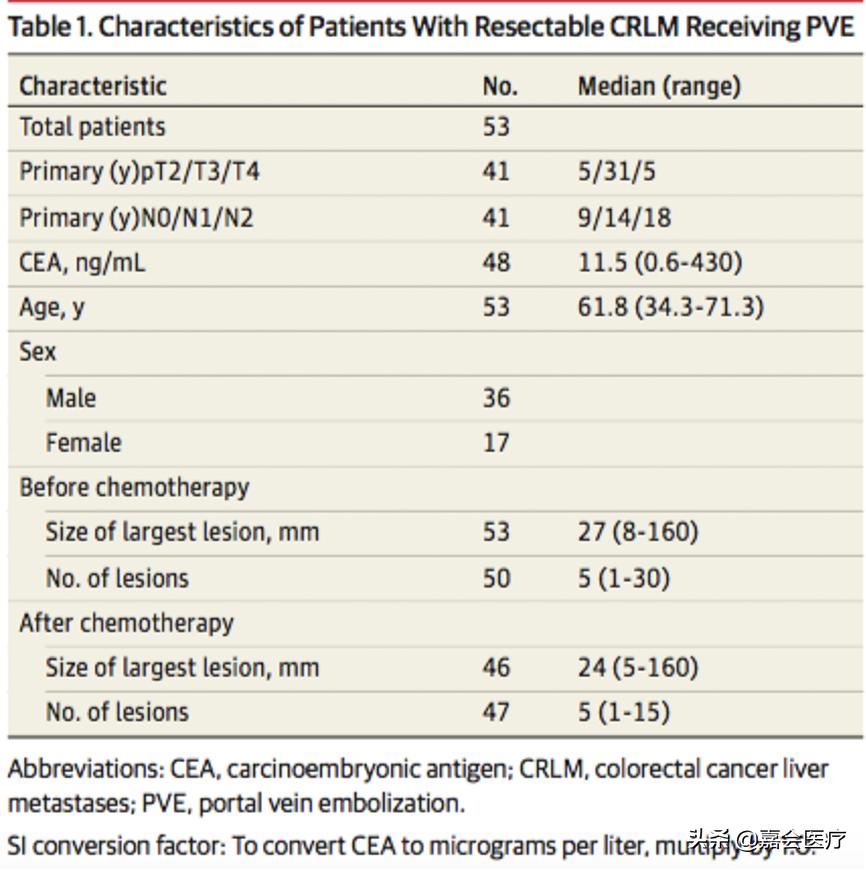
(注:CEA:癌胚抗原;CRLM:结直肠癌肝转移;PVE:门静脉栓塞。SI换算系数:将CEA换算成微克每升,乘以1.0。)
- 肝移植组中高肿瘤负荷患者的基线特征 (又分为升结肠原发肿瘤[n=8]与左侧原发肿瘤[n=21]两组)
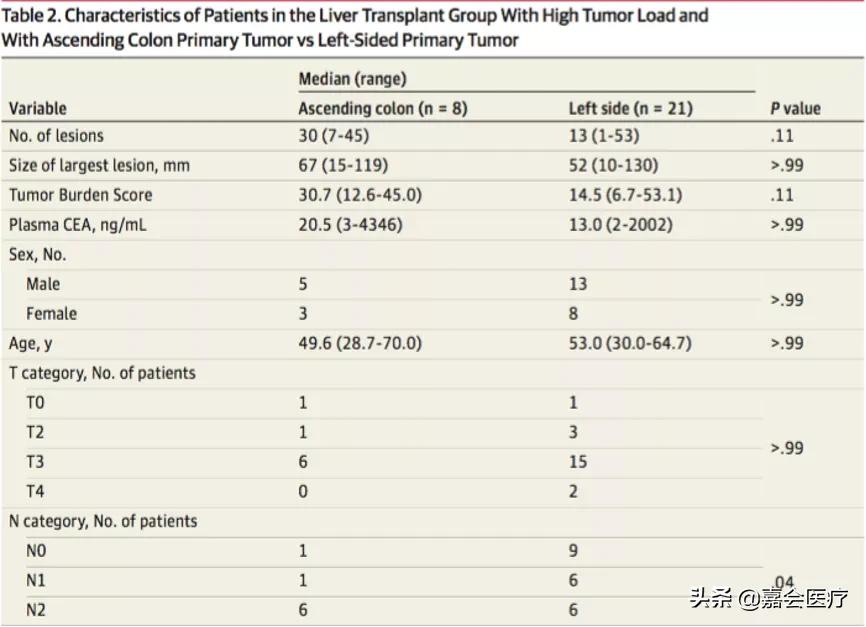
- 对肿瘤负荷的界定标准
肿瘤负荷得分(tumor burden score,TBS)的计算方式在此不赘述(感兴趣的同学请移步到参考文献第11)。先前的研究表明,CRLM病变超过8或10的患者在肝切除后OS降低。此外,最大肿瘤直径超过5 cm与术后生存率降低有关[7],病灶直径5.5 cm或更长的患者在肝移植后OS降低。
高肿瘤负荷在本研究中指的是:转移肿瘤有9个或更多,或最大肿瘤直径等于或大于5.5 cm,而低于这些指标的患者被归类为低肿瘤负荷)。
研究结果:
在高肿瘤负荷的CRLM患者中,左侧原发肿瘤+肝移植患者的OS远超PVE后肝切除治疗(图1):对比可见,2个PVE治疗组(单纯PVE组和PVE后肝切除组)和2个肝移植治疗组(升结肠原发肿瘤肝移植组合左侧原发肿瘤肝移植组)之间的生存率差异有统计学意义(P = .04)。PVE后肝切除组(n = 8)与左侧原发肿瘤+肝移植组(n = 21)也有显著性差异(P = .04)。
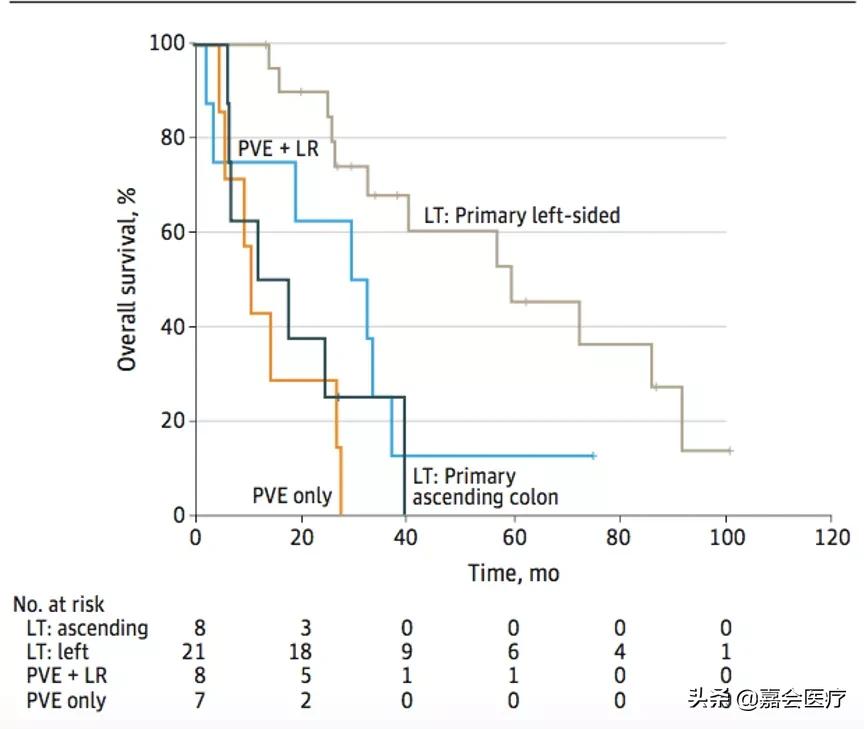
图1:高肿瘤负荷患者总生存率对比:PVE+肝切除(n=8)vs PVE(n=7);左侧原发性肝癌接受肝移植(n=21)vs 升结肠原发肿瘤接受肝移植(n=8)
讨论:研究结果超乎寻常,其中原因是什么?哪些患者可以适用?
这些结果也提醒我们反思一个问题: 移植术还是那个移植术,所以这些年,结直肠癌它都经历了什么?
自20世纪80年代以来,结直肠癌的分期有了很大的改善。氟18-标记的氟脱氧葡萄糖-正电子发射断层显像扫描(FDG-PET-CT)在检测肝外疾病方面具有很高的准确性[3]。在挪威奥斯陆大学医院Dueland等人的研究中,所有患者在移植前均经FDG-PET-CT进行了评估和分期[2]。
化疗在结直肠癌的治疗中也扮演了重要角色。全身化疗可根除肝外微小病变[4]。通过Fong和Stewart等人,我们还了解到, 肝肿瘤负荷既是发生肝外疾病可能性的预测因素[5],也是决定患者寿命长短的最重要因素[6] 。因此,通过精心筛选出肝肿瘤负荷较低的患者,Dueland等人让肝移植治疗CRLM的5年生存率超过了70%。
搞清楚了这项研究结果超乎寻常的主要原因后,一个仍然无解的难题继续摆在我们外科医生面前: 肝移植术的供体始终是一个极其有限的资源 。
每一年,在等待肝移植的名单上,有1000多名没命等到供体的患者[7]。在世界上肝脏供体比较丰富的国家或地区,或者在已有活体供肝移植项目的中心,提倡这样的治疗选择可能更为合理。
此外,我们应该认同,PVE+肝切除和其他围手术期治疗技术,极大地提高了我们安全切除肝脏病灶可能性,在条件允许的情况下,应考虑此法。
关于肝移植术治疗CRLM,还需要更多的临床研究去探索,而在我们的临床实践中,则需要在精心筛选的患者中谨慎实施:
- 对于因自然原因或既往全身和/或局部化疗导致的门静脉高压和肝衰竭的无病患者,可考虑移植 。
- 那些有活动性肝癌、病程长、对化疗反应良好、没有肝外疾病的患者,是开展临床试验或注册登记的理想群体。
参考文献
[1] London NJ, Giles GR. Liver transplantation for malignancy. Br J Cancer. 1991;64(4):621-623.
[2] Dueland S, Yaqub S, Syversveen T, et al. Survival outcomes after portal vein embolization and liver resection compared with liver transplant for patients with extensive colorectal liver cancer metastases. JAMA Surg. Published online March 31, 2021.
[3] Akhurst T, Kates TJ, Mazumdar M, et al. Recent chemotherapy reduces the sensitivity of [18F]fluorodeoxyglucose positron emission tomography in the detection of colorectal metastases. J Clin Oncol. 2005;23(34):8713-8716.
[4] Fakih MG. Metastatic colorectal cancer: current state and future directions. J Clin Oncol. 2015;33 (16):1809-1824.
[5] Fong Y, Fortner J, Sun R L,Brennan M F, Blumgart LH. Clinical score for predicting recurrence after hepatic resection for metastatic colorectal cancer: analysis of 1001 consecutive cases. Ann Surg. 1999; 230(3):309-318.
[6] Stewart C L, Warner S, Ito K, et al. Cytoreduction for colorectal metastases: liver, lung, peritoneum, lymph nodes, bone, brain: when does it palliate, prolong survival, and potentially cure? Curr Probl Surg. 2018;55(9):330-379. doi:10.1067/j.cpsurg.2018.08. 004
[7] UNOS. Making liver distribution more fair and equitable. Accessed February 10, 2021. https://unos.org/policy/liver-distribution/
版权信息
本文由一嘉医课编辑部负责编写或约稿。如需转载,请联系jmre@jmre.org。未经授权使用文章内容及部分内容是侵权行为,版权方保留追究法律责任的权利