
本篇来说说乳腺癌内分泌治疗的专家观点。
记者丨光亚
来源丨医学界肿瘤频道
近年来针对HER2+患者的研究非常丰富,HER2+患者靶向药使用时长、联合应用等的研究一直有更新,这部分患者的无病生存期(DFS)或阶段性DFS已从75%上升到94.1%,数据可观。随着探讨深入,精准治疗开始关注HER2+且HR+的患者,如何用新辅助治疗让这部分患者得到更积极治疗呢?
早前就有研究认为,HER2+、HR+与HER2+、HR-是两组生物学行为不同、对治疗反应不同的人群,两者的治疗策略可能不同。对HER2+、HR+乳腺癌,是否可以选择靶向联合内分泌治疗而不加化疗呢?
HR+/HER2+乳腺癌精准筛选后可避免化疗
8月17日,第三届亚洲乳腺癌会议”暨“第十一届天津国际乳腺癌会议”中,复旦大学肿瘤医院吴炅教授在报告中给出提示。他解读了2018年ASCO年会报告的PerELISA的研究,认为根据HR+、HER2+患者对新辅助内分泌的敏感性以及PAM50等筛选方法,可以一定程度上避免化疗 。一起来看看。
这项研究入组患者特征为绝经后可手术的HER2+、HR+患者,患者先接受2周来曲唑治疗,然后检测Ki67,Ki67变化较治疗前基线降低≥20%界定为内分泌治疗反应型。
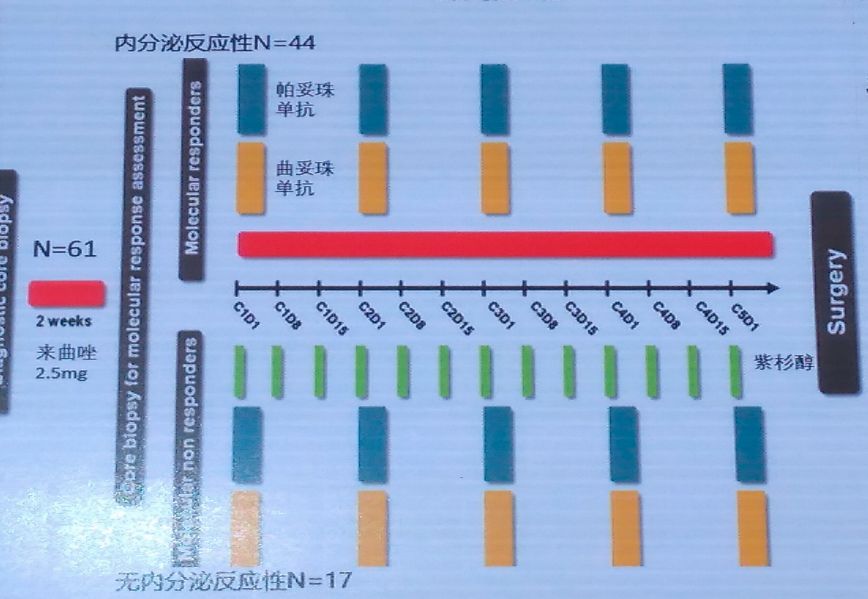
内分泌治疗反应型共纳入44例,给予双靶向治疗(曲妥珠单抗+帕妥珠单抗)+来曲唑新辅助治疗;内分泌治疗无反应型共纳入17例,给予单周紫杉联合双靶向治疗(曲妥珠单抗+帕妥珠单抗)。
结果显示:
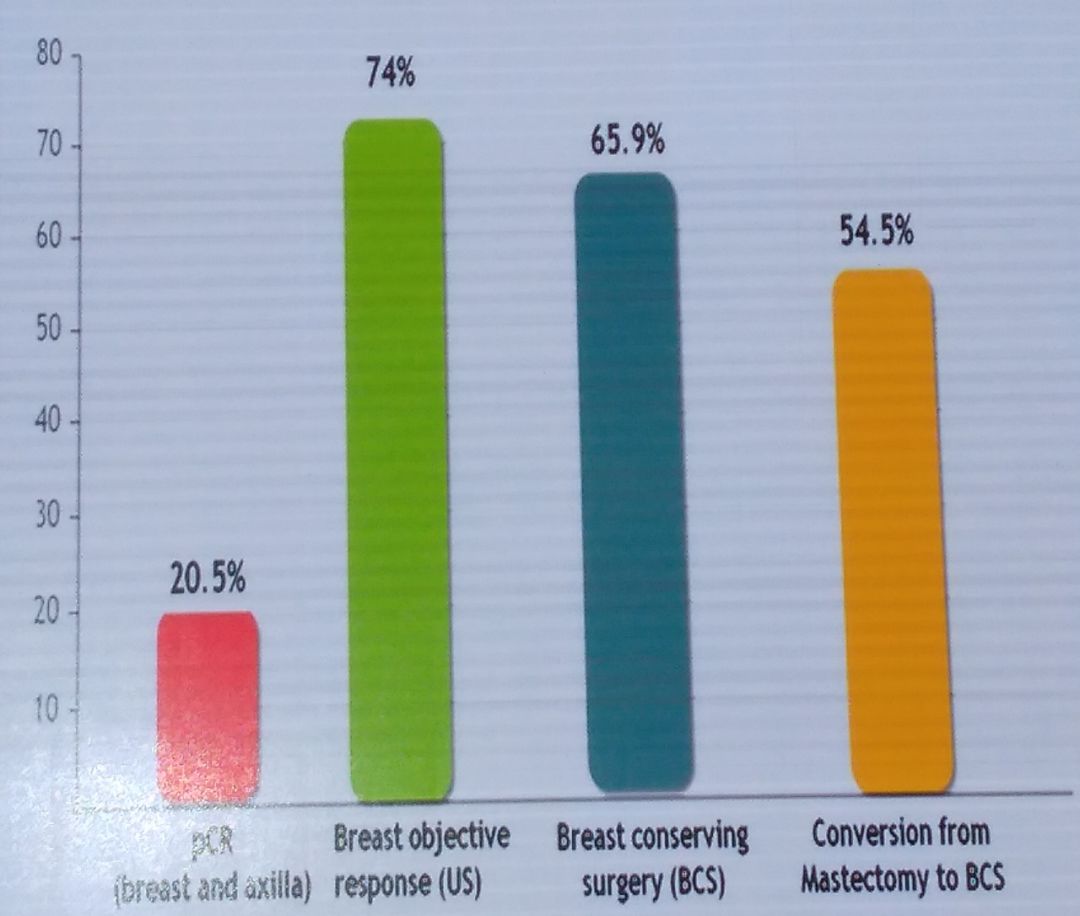
内分泌反应组pCR率为20.5%,乳房客观缓解率达到74%、保乳率为65.9%、乳房切除到保乳增加了54.5%。
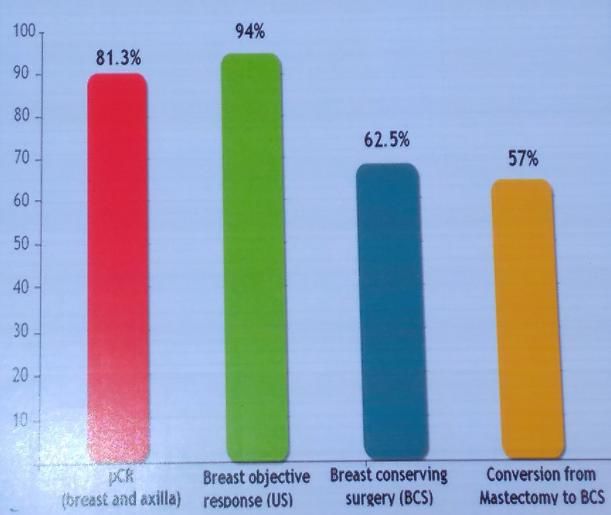
在内分泌无反应组,数据也很可观,pCR率为81.3%,乳房客观缓解率达到94%,保乳率为62.5%、乳房切除到保乳增加了57%。
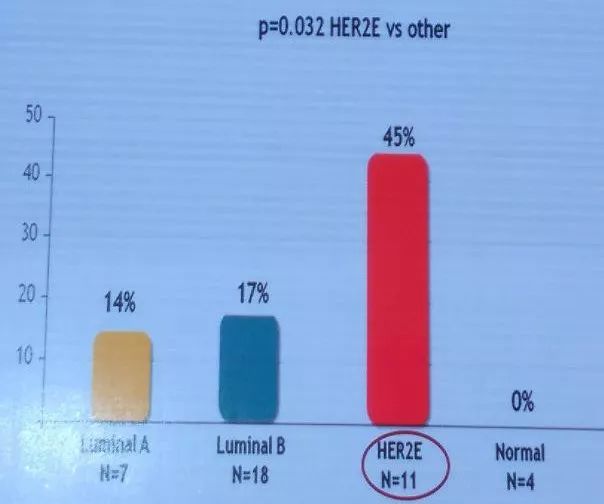
特别的是,研究者对内分泌反应组患者又进行了PAM50基因分型,HER2E亚组患者的pCR率可以达到45%。
“数据非常有启发,说明在HER2+患者中,仍可以找到某些方法,找到可能降低不良事件的治疗策略,让患者获得同样好的疗效。”吴炅教授称。
应对内分泌治疗耐药,需要围追堵截
依照乳腺癌基本分型方法,雌激素(ER)阳性乳腺癌占整个患者群很大一部分,据统计有60%-70%。这类患者整体预后佳,内分泌治疗是有力改善预后的方法。
但不管哪种方法,仍有约30%的腔面型乳腺癌在内分泌治疗后出现复发转移,临床仍有两大困惑,一是患者近期内分泌耐药,二是远期复发转移问题。
现有内分泌治疗手段有以下几种:
(1)选择性雌激素受体调节剂(SERM),包括他莫昔芬、托瑞米芬、雷洛昔芬等;
(2)选择性雌激素受体下调剂(SERD),如氟维司群;
(3)芳香化酶*制剂抑**(AI),如阿那曲唑、来曲唑、依西美坦等;
(4)卵巢功能抑制,包括用促黄体生成素释放激素(LHRH)类似物或卵巢手术/放疗等;
(5)其他。
研究显示,约1/3 ER+患者在他莫昔芬治疗2-5年内出现耐药;ER+患者,约50%复发与66%死亡事件发生在5-15年。因此研究者关注的重点更多在内分泌治疗耐药上,现在的观点认为,要区别对待内分泌治疗耐药和敏感复发两种情况,并根据复发时间决定治疗策略。
仅对耐药就要区分原发耐药和继发性耐药。前者是辅助内分泌治疗2年内复发或一线内分泌治疗6个月内复发转移;后者是辅助内分泌治疗2年后至结束后1年内复发转移或一线内分泌治疗6个月后复发转移。而敏感性复发指辅助内分泌治疗结束后1年以上复发转移。
第三届亚洲乳腺癌会议”暨“第十一届天津国际乳腺癌会议”中,复旦大学肿瘤医院余科达教授这样形容应对内分泌耐药的策略——多层面逆转。
因为细胞内外各通路与ER通路存在交互作用,逆转内分泌耐药要从多层面入手:
-
“针对核心”的ESR1突变;
-
“打击旁路”,即用PI3K/AKT/mTOR通路*制剂抑**;
-
“阻断上游”,使用EGFR/HER2/FGFR等受体*制剂抑**;
-
“抑制下游”,用细胞周期通路及CDK4/6*制剂抑**。
(1)针对核心
有研究显示,某些已被发现的ESR1突变,其编码的ERα可以在没有激素存在的情况下激活,提示对采用直接靶向ER的药物,如高剂量氟维司群是有效的,而对阻断雌激素的AI治疗可能无效。
(2)打击旁路
PI3K/AKT/mTOR通路与ER通路存在相互作用,联合通路*制剂抑**及内分泌药物可产生协同作用,能逆转耐药。
|
靶点 |
*制剂抑**或抗体 |
|
PI3K |
BKM-120 |
|
GDC-0941 |
|
|
GSK2126458 |
|
|
AKT |
MK-2206 |
|
perifosine |
|
|
mTOR |
Everolimus(依维莫司) |
|
Temsirolimus |
2013年BOLERO-2研究和2018年PrE0102研究说明,mTOR*制剂抑**依维莫司联合内分泌药物可使耐药患者获益。
复旦大学肿瘤医院基于149例癌组织测序结果,绘制了中国乳腺癌的PI3K/AKT通路突变谱,结合文库进行“功能性突变筛选”,相应靶向药物正在研发中。
( 3)阻断上游 ,即EGFR/HER2/FGFR信号通路。酪氨酸激酶受体旁通路激活,引起内分泌治疗耐药。
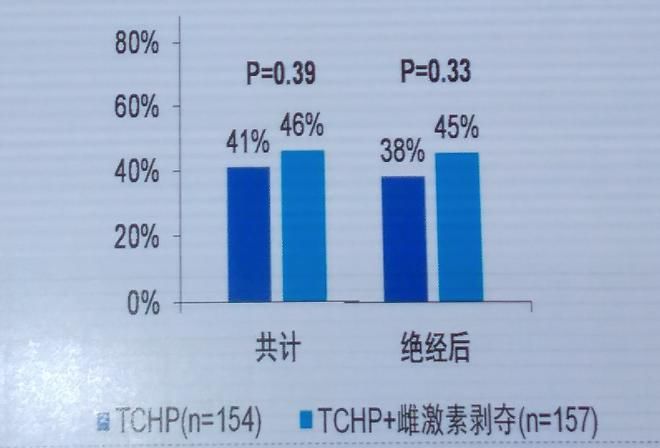
最新NSABP B-52试验是将HER2阳性、ER和/或PgR阳性浸润性乳腺癌通过粗针活检确认,随机分组为TC+曲妥珠单抗+帕妥珠单抗组,以及TC+曲妥珠单抗+帕妥珠单抗+雌激素剥夺组。主要终点为乳腺和淋巴结pCR率。结果提示,虽然两组pCR相差较小,但说明针对某些人群仍有差异。
(4)抑制下游,针对CDK4/6细胞周期通路。
CDK4/6*制剂抑**与内分泌药物产生协同效应,逆转内分泌耐药。PALOMA3研究,一项全球性、随机双盲安慰剂对照临床研究显示,CDK4/6*制剂抑**Palbociclib联合氟维司群显著延长HR+/HER2-内分泌耐药晚期乳腺癌患者的PFS,目前该药已在国内外上市。针对CDK4/6的MONARCH2和MONALEESA3研究也同样提示了CDK4/6对耐药问题的有利作用。
精准医学时代,需根据不同耐药机制选择靶向药物,逆转内分泌耐药,进一步改善患者预后。余教授认为,未来的内分泌治疗,还需要高效挖掘分子靶点,多组学多视角整合多靶点,防治多通路逃逸和交叉耐药。
注:本文部分图片截取自此次大会专家报告。
会议介绍
8月17日,由中国抗癌协会乳腺癌专业委员会主办、天津市肿瘤医院承办的“第三届亚洲乳腺癌会议”暨“第十一届天津国际乳腺癌会议”在津正式召开。
本次会议作为国内首个美国临床肿瘤学会(ASCO)乳腺癌海外会场,由中国抗癌协会乳腺癌专业委员会、美国临床肿瘤学会主办,天津市肿瘤医院承办,邀请美国、英国、日本、韩国、印度等国际知名肿瘤专家,汇聚800余名包括香港、台湾在内的来自全国30余个省、市、自治区的乳腺肿瘤学者,共同梳理乳腺癌诊疗的前沿热点和科研成果,对ASCO大会的核心资讯和焦点问题进行精选汇总和专题解读,并针对乳腺癌精准医学策略、乳腺癌转化医学、乳腺癌影像诊断与外科治疗、靶向治疗、多学科协作及个体化治疗等方面进行学术交流和探讨,旨在传递乳腺癌领域的最新成果和发展动态,进一步推动乳腺癌的整体发展。


(本文为医学界肿瘤频道原创文章,转载需经授权并标明作者和来源。)