·论著·
引用本文:张蒙, 周帆, 刘明东, 等. 经胃联合经皮内镜治疗感染性胰腺坏死的疗效分析[J]. 中华消化内镜杂志, 2022, 39(12): 1009-1013. DOI: 10.3760/cma.j.cn321463-20220125-00503.
经胃联合经皮内镜治疗感染性胰腺坏死的疗效分析
Efficacy of transgastric combined with percutaneous endoscopy for infected pancreatic necrosis
张蒙 周帆 刘明东 邹晓平 韩光曙
*京大南**学医学院附属鼓楼医院消化内科,南京 210008
通信作者:韩光曙,Email: gs_han110@163.com
【摘要】 目的 评价经胃联合经皮内镜治疗感染性胰腺坏死(infected pancreatic necrosis,IPN)的疗效。方法 回顾性分析2015年8月—2020年8月在南京鼓楼医院消化内科重症监护室接受经胃联合经皮内镜治疗的19例IPN患者的临床资料,分析其临床疗效及手术相关并发症的发生情况。结果 每例患者内镜腔内引流术(endoscopic transmural drainage, ETD)治疗(1.1±0.3)次。在ETD术中,9例患者置入双腔固定支架,2例患者置入金属覆膜支架,7例置入双猪尾塑料支架,1例仅置入鼻囊肿引流管。19例患者均在首次经皮穿刺引流术(percutaneous catheter drainage, PCD)中置入12~14 F引流管进行引流,每人置管(1.8±1.2)根,其中3例患者后续更换为双套管持续引流,1例患者后续经皮置入金属覆膜支架进行引流。穿刺引流液培养结果为11例革兰阴性杆菌及革兰阳性球菌,4例革兰阳性球菌,1例革兰阳性杆菌,3例革兰阴性杆菌。19例患者中4例同时合并真菌感染。每例患者清创(3.1±1.8)次,其中2例行经皮内镜坏死组织清除术联合内镜坏死组织清除术治疗。每例患者总操作(6.1±2.4)次。术后出现出血1例(5.3%),经内镜治疗后成功止血,无消化道瘘、穿孔、胰瘘等严重并发症发生。1例死亡,原因为脓毒血症,其余18例经治疗后IPN明显吸收。19例患者均未转为开腹手术。结论 经胃联合经皮内镜治疗IPN安全有效。
【关键词】 胰腺炎,急性坏死性; 内镜腔内引流术; 经皮穿刺引流术; 疗效
在重症急性胰腺炎(severe acute pancreatitis,SAP)的严重并发症病程中,当胰腺和(或)胰周坏死继发感染时,称为感染性胰腺坏死(infected pancreatic necrosis,IPN)[1]。近年来IPN治疗逐渐由各种形式的微创治疗取代传统的开腹手术治疗。这些微创方法包括经皮穿刺引流术(percutaneous catheter drainage, PCD)、内镜腔内引流术(endoscopic transmural drainage, ETD)、经皮内镜坏死组织清除术(percutaneous endoscopic necrosectomy, PEN)、内镜坏死组织清除术(endoscopic transluminal necrosectomy, ETN)等多种方式。有研究指出,采取内镜联合经皮穿刺引流的方式,能够避免慢性胰皮瘘的发生、降低手术相关并发症的发生率并且避免开腹手术[2]。我院自2015年起,对部分IPN患者开展了两种入路联合的升阶梯治疗方式,本文对这些患者的临床资料进行回顾性分析,以评估其疗效,提供IPN干预治疗的新思路。
资料与方法
一、研究对象
纳入2015年8月—2020年8月于我院消化内科重症监护室住院行经胃联合经皮内镜治疗的IPN患者。纳入标准:明确诊断为IPN;IPN位置距离胃壁<1 cm且IPN位置累及结肠旁沟或盆腔,无法经单纯ETD治疗痊愈。排除标准:合并其他严重的基础疾病;合并胰腺癌或胰腺肿瘤性/囊性病变。
二、研究方法
一旦高度怀疑IPN的发生,即经验性静脉应用广谱的碳青霉烯类抗生素抗感染,若患者仍有发热,且血培养或引流液培养提示革兰阳性菌,则加用替考拉宁/利奈唑胺/万古霉素抗感染。干预治疗前均完善全腹部CT平扫+增强以评估IPN的部位、大小及是否具有ETD及PCD治疗的合适路径。依据IPN距离胃壁或十二指肠位置以及患者一般情况,如坏死距体表更近,且患者一般状况无法耐受内镜检查,则先选择PCD,反之则选择ETD。患者术前均签署知情同意书。
ETD治疗:患者取侧卧位,在全身麻醉下,超声内镜经口插入胃腔,在胃内探查IPN的位置、大小、与胃壁间的距离,在多普勒信号指引下,选择适当穿刺点,以19 G穿刺针穿刺至脓腔内,见脓液流出后,循穿刺针置入导丝,循导丝置入扩张球囊或扩张烧灼导管,扩张后经导丝置入双腔固定支架/金属覆膜支架/双猪尾塑料支架,同时放置鼻囊肿管,支架选择依据IPN内坏死物的多少,对坏死物较少的IPN选择塑料支架,而对坏死物较多的则选择金属支架。金属支架中双腔固定支架或金属覆膜支架的选择则依赖于术者的习惯。术后留取标本送检常规、生化、病原学检查。术后用生理盐水经鼻囊肿引流管对囊腔进行冲洗。术后2周复查CT评估疗效,临床症状改善不明显者,或复查CT感染腔最大径缩小<1/2者行ETN。患者取侧卧位,胃镜经口进镜至胃腔,在胃壁内探查到支架所在部位,内镜循开口处进入脓腔,予圈套器清除坏死物质,生理盐水反复冲洗脓腔。可根据病情需要多次行ETN治疗(图1)。
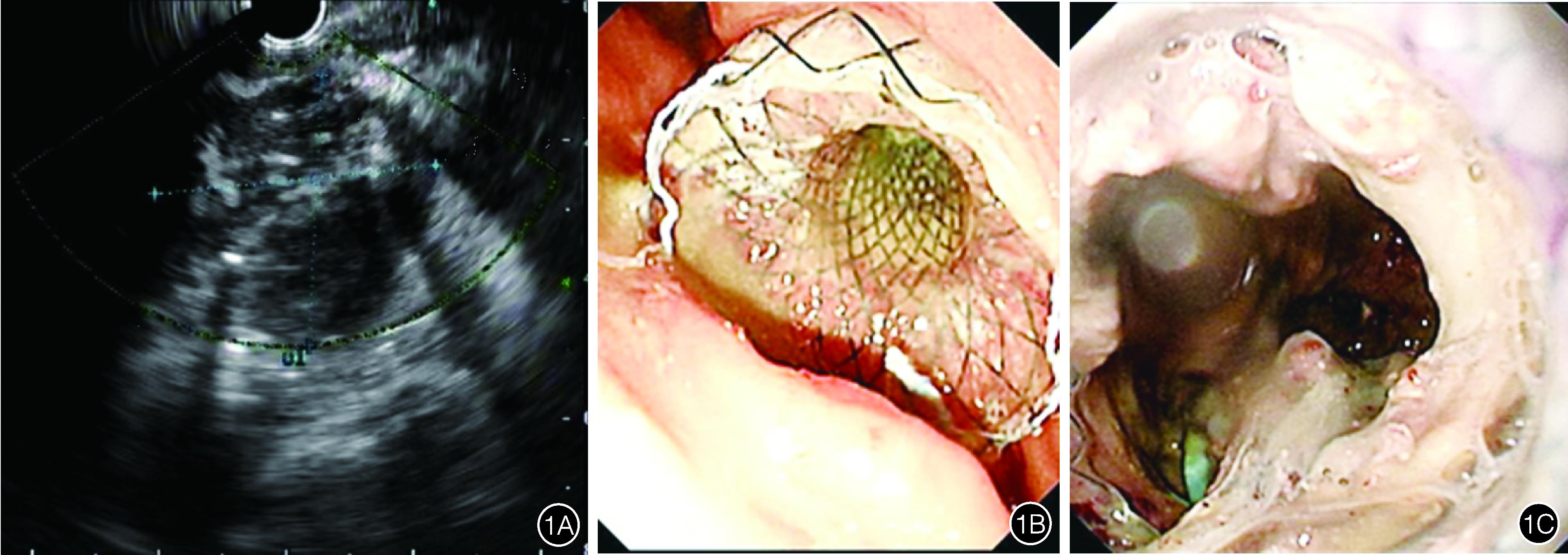
图1 超声内镜下经胃穿刺支架引流及坏死组织清除术 1A:超声内镜下见距离胃壁小于1 cm的感染性胰腺坏死,有明确的炎性壁,内含坏死物质; 1B:内镜下见双腔固定支架置入胃壁; 1C:内镜下见囊腔内大量坏死物质,经金属支架行清创治疗
PCD治疗:患者取平卧位,2%利多卡因局部浸润麻醉,在超声引导下,以穿刺针经皮穿刺至脓腔内,回抽确认穿刺成功后置入导丝,拔除穿刺针,循导丝置入14 F引流管。术后留取标本送检常规、生化、病原学检查。术后用生理盐水经引流管对囊腔进行冲洗。术后2周复查CT,临床症状改善不佳或感染腔最大径缩小<1/2者,可考虑更换为金属全覆膜支架或双套管持续冲洗。若坏死物仍不能充分引流,可进一步行PEN。患者取仰卧位,拔除体表引流管/金属覆膜支架/双套管后,必要时将窦道扩张至1.2~1.5 cm,内镜自腹壁窦道进镜,予圈套器清除坏死物质,生理盐水反复冲洗脓腔,见脓腔壁肉芽组织,循窦道重新置入引流管并固定。可根据病情需要多次行PEN治疗(图2)。
术后密切监测生命体征,动态复查血常规、生化、C反应蛋白及血淀粉酶、引流液淀粉酶以评估病情。根据病情需要择期复查腹部CT评估IPN吸收情况并制定下一步诊疗方案。对于经治疗后生命体征平稳且腹部CT检查见IPN较前明显吸收的患者,可择期安排出院,门诊定期复查(图3)。
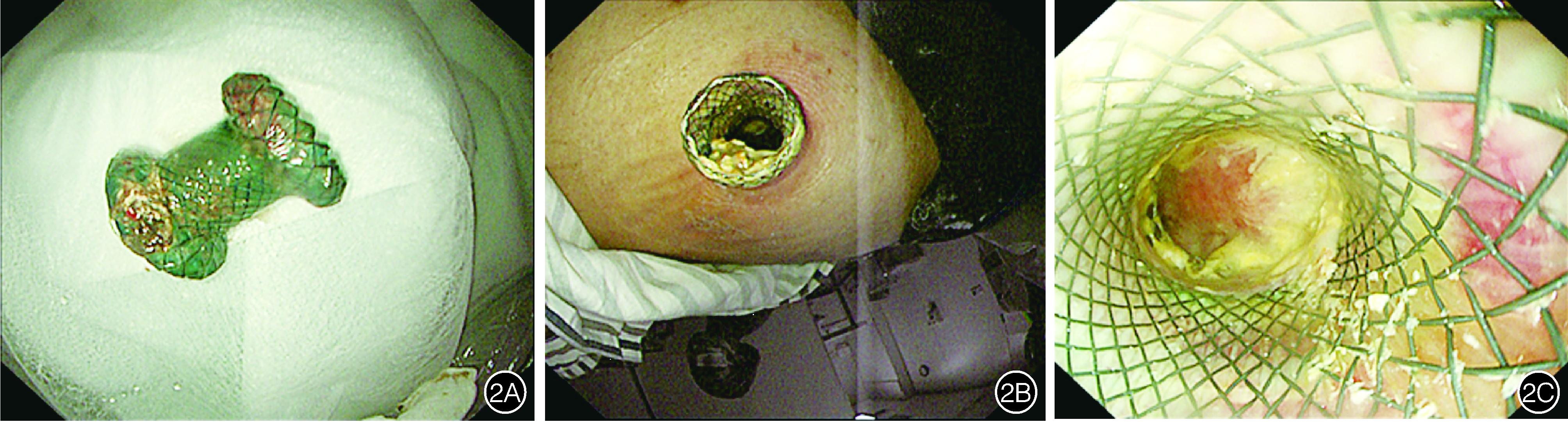
图2 经皮金属支架引流及坏死组织清除术 2A:金属支架的外观; 2B:体外见经皮置入金属支架形成的窦道; 2C:内镜下见囊腔内大量坏死物质,经金属支架行清创治疗
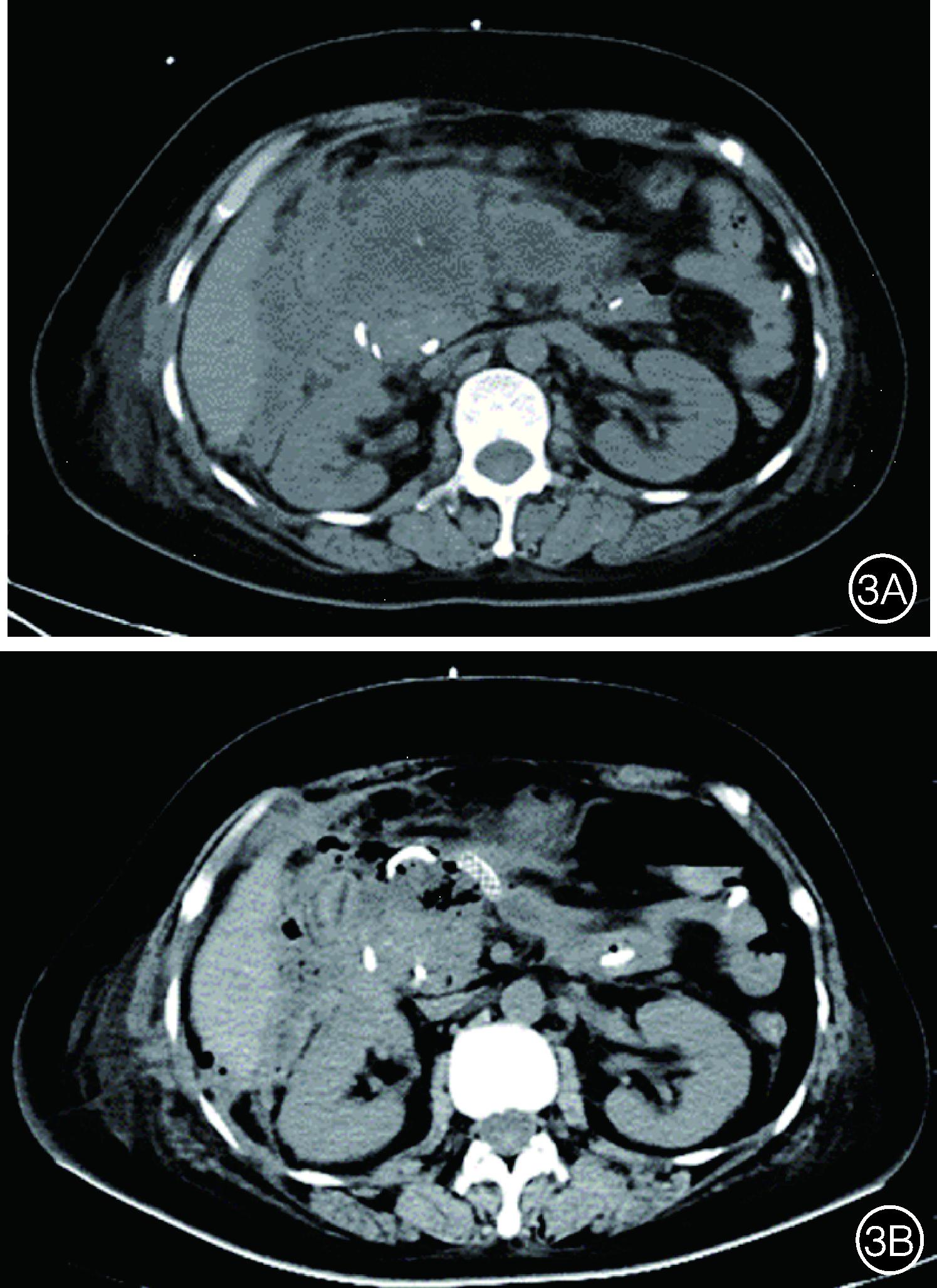
图3 经胃联合经皮内镜治疗前后感染性胰腺坏死的影像学表现 3A:CT见治疗前感染性胰腺坏死面积大,累及胰腺及胰周; 3B:CT见治疗后感染性胰腺坏死基本完全吸收
三、观察指标
观察指标包括4个方面:(1)患者的基本资料:性别、年龄、住院时间、主诉、胰腺炎病因、发病时间、吸烟史、饮酒史及其他基础疾病史;(2)IPN的部位、形成时间、引流液病原学结果;(3)治疗经过:首次干预时间、经胃/经皮穿刺引流次数、经胃置入支架数目、类型及大小、经皮置管数目及直径、是否清创、清创方式及清创次数;(4)手术的疗效及手术相关并发症的发生情况。手术疗效判断标准为经手术治疗后IPN的吸收情况及患者临床症状是否缓解。
四、统计学方法
采用SPSS 26.0统计学软件对数据进行分析,计量资料以或中位数(范围)表示,计数资料以例(%)表示。
结果
一、基本资料
纳入的19例患者中男10例,女9例,年龄(44.6±15.4)岁。以消化道症状,包括腹痛、腹胀、恶心、呕吐等疾病起病的患者18例(94.7%),其中6例同时合并发热,以胆道梗阻症状起病1例(5.3%)。胰腺炎病因包括胆源性6例(31.6%),高脂血症性11例(57.9%),ERCP术后1例(5.3%),特发性1例(5.3%)。既往或现在有吸烟史6例(31.6%),饮酒史2例(10.5%),其中1例同时有吸烟史及饮酒史。
二、IPN的一般情况
IPN位于胰周的患者13例(68.4%),胰头2例(10.5%),胰尾1例(5.3%),同时存在胰腺及胰周3例(15.8%)。IPN确诊距发病中位时间为27 d(12~243 d),IPN确诊距首次手术中位时间为10 d(0~46 d)。穿刺引流液培养结果为11例革兰阴性杆菌及革兰阳性球菌,4例革兰阳性球菌,1例革兰阳性杆菌,3例革兰阴性杆菌,其中4例同时合并真菌感染,最常见的病原体为大肠埃希菌(G-杆菌)、肺炎克雷伯杆菌(G-杆菌)及屎肠球菌(G+球菌)。
三、治疗经过
19例患者均穿刺成功,11例首先行ETD,8例首先行PCD。每例患者ETD治疗(1.1±0.3)次,PCD置管(1.8±1.2)根。两种入路治疗间隔中位时间13 d(2~46 d)。在ETD术中,9例患者置入双腔固定支架,2例患者置入金属覆膜支架,7例置入双猪尾塑料支架,1例仅置入鼻囊肿引流管。19例患者均在首次PCD治疗中置入12~14 F引流管进行引流,其中3例患者后续更换为双套管持续引流,1例患者后续经皮置入金属覆膜支架进行引流。19例患者中2例患者仅通过引流即达到IPN治愈,而另外17例患者(89.5%)引流后需行清创治疗,清创(3.1±1.8)次,其中2例行ETN联合PEN治疗。每例患者总操作次数(6.1±2.4)次。
四、手术疗效及手术相关并发症情况
术后出现手术相关并发症出血1例(5.3%),经内镜治疗后成功止血,术后6个月随访无消化道瘘、穿孔、胰瘘等严重并发症发生。1例因入院时即合并严重的脓毒血症,经积极治疗后仍无明显好转而死亡。19例患者均未转为开腹手术。
讨论
IPN是SAP患者病程后期死亡的主要原因[3],因此IPN的有效治疗是降低SAP死亡率的重要环节。IPN常需采取微创干预治疗,干预的途径可分为经胃和经皮。干预途径的选择主要依据IPN的位置,ETD仅适用于与胃或者十二指肠的距离不超过1 cm的IPN,对于合并结肠旁沟或盆腔的位置较低的IPN通常需要联合经皮途径。
2010年,Ross等[4]在一项小样本回顾性研究中提出,对于适用两种干预方式联合治疗的IPN患者,可在首次PCD治疗结束的同时立即行ETD治疗,以形成胰胃或胰十二指肠内瘘,从而避免胰皮瘘的发生,并将其定义为双模式引流(dual modality drainage,DMD)。这为IPN的干预治疗提供了新的思路,该研究小组后续的一项为期5年的队列研究发现DMD能够完全避免慢性胰皮瘘的发生,并且在手术相关并发症的发生率(6/117,5.13%)和死亡率(4/117,3.4%)方面表现良好,但由于不进行主动清创,在一定程度上延长了经皮引流的时间(中位数63 d)[2]。2016年的一篇报道中提出,对于部分患者,在DMD的基础上早期行经皮窦道视频辅助腹膜后清创(video assisted retroperitoneal debridement,VARD)治疗,有望缩短经皮引流的时间 [5]。2018年,Jagielski 等[6]介绍了一种不同于DMD的治疗方式,以ETD为基础治疗方式,在坏死吸收不理想的情况下进一步行PCD治疗,同时采取主动引流,包括生理盐水通过鼻囊肿管及PCD引流管冲洗,手术相关并发症的发生率(4/20,20%)很低,且随访中无慢性胰瘘的发生。
在以上研究的基础上,我们对经胃联合经皮引流治疗进行了改进。首先,除鼻囊肿管或PCD引流管冲洗,通过内镜观察发现坏死物较多,仅经支架及引流管引流难以使坏死物有效吸收或使临床症状缓解,对于这类患者,我们采取了主动清创治疗。其次,在ETD治疗中,部分坏死较多的患者放置金属支架代替塑料支架,由于其直径大,可避免后续清创治疗中对窦道的扩张,降低手术风险,但缺点是有移位和包埋的风险,因此金属支架放置时间<4周,更换为塑料支架继续进行内引流。再次,PCD置入的引流管直径一般为12~14 F,直径较小,常导致引流不彻底,且在后续PEN治疗前需要行窦道扩张。2011年Jain等[7]首次报道了1例经皮置入自膨式金属支架(self‑expandable metal stent, SEMS)代替引流管治愈的IPN患者,SEMS使得经皮窦道得到充分扩张,为后续清创治疗提供便利。此后2012年童智慧等[8]首次提出可以对IPN的患者经皮置入双套管进行持续负压冲洗,结果显示双套管负压冲洗治疗的IPN患者中转开腹手术的比例(15.8%,3/19)明显低于PCD治疗的患者(48.1%,25/52)。大量文献显示这两种治疗方式效果令人满意且技术逐渐成熟[9‑12]。因此在我们的研究中,对经PCD引流后临床症状改善不佳或IPN最大径缩小<1/2者,首先考虑更换为双套管持续引流(3例)或经皮金属覆膜支架引流(1例),再考虑进一步行PEN治疗。对于部分长径较大的IPN,经内镜治疗后感染仍持续进展或出现严重肠道并发症,如消化道瘘、消化道大出血等的患者,则需进一步行开腹清创手术[13‑14]。本研究中,患者均未转为开腹手术,也未发生慢性胰皮瘘等严重并发症。
Nemoto 等[15]的一项回顾性研究发现,大部分IPN患者经内镜治疗可达到治愈(73/83,88%),其中67%(49/73)仅需ETD治疗,另外33%(24/73)则需联合PCD治疗,平均清创次数3.8次,手术相关并发症的发生率为13%(11/83),包括出血9例,穿孔1例,空气栓塞1例,另有4%(3/83)需要转为开腹手术。另有Meta分析报道,单独PCD治疗能够实现IPN患者55.7%(214/384)的治愈率,有 34.6%(133/384)需要额外手术切除坏死组织,手术相关并发症的发生率为21.2%(75/354),其中大部分为慢性胰皮瘘(53例)[16]。2018年的一项随机对照试验也发现,ETD与PCD在疗效及并发症的发生率方面差异无统计学意义,而ETD的优势在于降低了慢性胰皮瘘的发生率[17]。在我们的研究中,94.7%(18/19)的IPN患者在ETD联合PCD治疗后达到IPN最大径缩小及临床症状缓解的良好效果,清创次数(3.1±1.8)次,手术相关并发症的发生率仅5.3%(1/19),无论是与单纯ETD治疗或单纯PCD治疗相比,还是与既往报道的联合治疗相比,经胃联合经皮引流均在疗效及并发症的发生率方面表现良好。但本研究的样本量偏小,且无合适的对照组进行比较,因此在大样本研究中是否仍然具备优势尚不明确。
总的来说,我们认为,经胃联合经皮内镜治疗IPN安全有效,能够使患者有效避免开腹手术。未来我们的工作重点将放在通过更大样本量的随机对照试验探索经胃联合经皮升阶梯治疗的优化方案,并且进一步明确双套管持续引流或经皮金属覆膜支架引流的指征及优缺点。
利益冲突 所有作者声明不存在利益冲突
作者贡献声明
张蒙、周帆:数据收集与整理、统计学分析,论文撰写;刘明东、邹晓平、韩光曙:研究设计与指导、论文修改
参考文献
[1] Banks PA, Bollen TL, Dervenis C, et al. Classification of acute pancreatitis--2012: revision of the Atlanta classification and definitions by international consensus[J]. Gut, 2013,62(1):102-111. DOI: 10.1136/gutjnl-2012-302779.
[2] Ross AS, Irani S, Gan SI, et al. Dual-modality drainage of infected and symptomatic walled-off pancreatic necrosis: long-term clinical outcomes[J]. Gastrointest Endosc, 2014,79(6):929-935. DOI: 10.1016/j.gie.2013.10.014.
[3] Carnovale A, Rabitti PG, Manes G, et al. Mortality in acute pancreatitis: is it an early or a late event?[J]. JOP, 2005,6(5):438-444.
[4] Ross A, Gluck M, Irani S, et al. Combined endoscopic and percutaneous drainage of organized pancreatic necrosis[J]. Gastrointest Endosc, 2010,71(1):79-84. DOI: 10.1016/j.gie.2009.06.037.
[5] Fagenholz PJ, Thabet A, Mueller PR, et al. Combined endoscopic trangastric drainage and video assisted retroperitoneal pancreatic debridement - the best of both worlds for extensive pancreatic necrosis with enteric fistulae[J]. Pancreatology, 2016,16(5):788-790. DOI: 10.1016/j.pan.2016.06.009.
[6] Jagielski M, Smoczyński M, Studniarek M, et al. Endoscopic drainage combined with percutaneous drainage in treatment of walled-off pancreatic necrosis - a single-center experience[J]. Prz Gastroenterol, 2018,13(2):137-142. DOI: 10.5114/pg.2018.72604.
[7] Jain V, Pauli E, Sharzehi K, et al. Spontaneous gastrosplenic fistula secondary to diffuse large B-cell lymphoma[J]. Gastrointest Endosc, 2011,73(3):608-609. DOI: 10.1016/j.gie.2010.09.015.
[8] 童智慧, 吴丛业, 李维勤, 等. 经皮置管与负压冲洗引流治疗重症急性胰腺炎合并胰腺坏死组织感染[J].中华胰腺病杂志,2012,12(5):302-305. DOI:10.3760/cma.j.issn. 1674-1935.2102.05.004.
[9] Saumoy M, Kumta NA, Tyberg A, et al. Transcutaneous endoscopic necrosectomy for walled-off pancreatic necrosis in the paracolic gutter[J]. J Clin Gastroenterol, 2018,52(5):458-463. DOI: 10.1097/MCG.0000000000000895.
[10] Laopeamthong I, Tonozuka R, Kojima H, et al. Percutaneous endoscopic necrosectomy using a fully covered self-expandable metal stent in severe necrotizing pancreatitis[J]. Endoscopy, 2019,51(2):E22-22E23. DOI: 10.1055/a-0756-8203.
[11] 汪鹏, 李刚, 柯路, 等. 经皮支架辅助内镜下坏死组织清除术治疗胰腺坏死组织感染[J].中华胰腺病杂志,2019,19(6):411-415. DOI: 10.3760/cma.j.issn.1674-1935.2019.06.004.
[12] 张正乐, 荣愈平, 常剑, 等. 经皮支架辅助感染性胰腺坏死清除的疗效分析[J].中华普通外科杂志,2020,35(5):408-409. DOI: 10.3760/cma.j.cn113855-20190724-00419.
[13] 杜越晨, 倪建波. 感染性胰腺坏死的治疗进展[J].同济大学学报(医学版),2020,41(6):796-800. DOI: 10.16118/j.1008-0392.2020.06.019.
[14] Baron TH, DiMaio CJ, Wang AY, et al. American Gastroenterological Association clinical practice update: management of pancreatic necrosis[J]. Gastroenterology, 2020,158(1):67-75. DOI: 10.1053/j.gastro.2019.07.064.
[15] Nemoto Y, Attam R, Arain MA, et al. Interventions for walled off necrosis using an algorithm based endoscopic step-up approach: outcomes in a large cohort of patients[J]. Pancreatology, 2017,17(5):663-668. DOI: 10.1016/j.pan.2017.07.195.
[16] van Baal MC, van Santvoort HC, Bollen TL, et al. Systematic review of percutaneous catheter drainage as primary treatment for necrotizing pancreatitis[J]. Br J Surg, 2011,98(1):18-27. DOI: 10.1002/bjs.7304.
[17] van Brunschot S, van Grinsven J, van Santvoort HC, et al. Endoscopic or surgical step-up approach for infected necrotising pancreatitis: a multicentre randomised trial[J]. Lancet, 2018,391(10115):51-58. DOI: 10.1016/S0140-6736(17)32404-2.
DOI:10.3760/cma.j.cn321463-20220125-00503
收稿日期 2022-01-25 本文编辑 钱程