当前国内不少患者为经济所迫选用未经药监局批准的仿制伊马替尼,十余年来虽未发生严重的毒副作用,但缺乏定期监测是最大的危害。有些患者服药多年从未复查骨髓和分子效应,甚至不定期查血象,直到疾病进展不可挽回。希望专科医生不论采用哪一代TKI均能遵循指南。
01
“神药”格列卫
通用名:甲磺酸伊马替尼片,商品名:格列卫,英文名:imatinib (Gleevec®)
适应证:用于治疗费城染色体阳性的慢性髓性白血病(Ph+CML)的慢性期、加速期或急变期。
02
慢性粒细胞白血病
一种影响血液及骨髓的恶性肿瘤,它的特点是产生大量不成熟的白细胞,这些白细胞在骨髓内聚集,抑制骨髓的正常造血;并且能够通过血液在全身扩散,导致病人出现贫血、容易出血、感染及器官浸润等。
慢性粒细胞白血病(CML )分期:
1. 慢性期外周血或骨髓中原始细胞<10%;未达到诊断加速期或急变期的标准。
2. 加速期符合下列任何一项:外周血或骨髓中原始细胞占10%~19%;外周血嗜碱粒细胞≥20%;与治疗不相关的持续血小板减少(PLT<100×10^9/L)或增高(PLT>1000×10^9/L);治疗过程中出现Ph+细胞基础上的其他克隆性染色体异(CCA/Ph+);进行性脾脏增大或白细胞计数增高。
3. 急变期符合下列任何一项:外周血或骨髓中原始细胞≥20%;骨髓活检原始细胞集聚;髓外原始细胞浸润。
03
诊断标准
国内诊断标准
参照WHO 2008版造血和淋巴组织肿瘤诊断分期标准。
典型的临床表现,合并Ph 染色体和(或)BCR-ABL 融合基因阳性即可确定诊断。
WHO诊断标准
WHO分类2008年第4版CML诊断标准(摘要):慢性粒细胞白血病(CML)属于慢性骨髓增殖性肿瘤(MPN)。源于造血干细胞克隆性异常,具有特异性Ph染色体和(或)BCR-ABL1 融合基因。此病可分为三期:初起为隐匿的慢性期(CP),随后进展为加速期(AP)或急变期(BP)。
04
疗效标准
国内标准基本与国际相同,见下表。
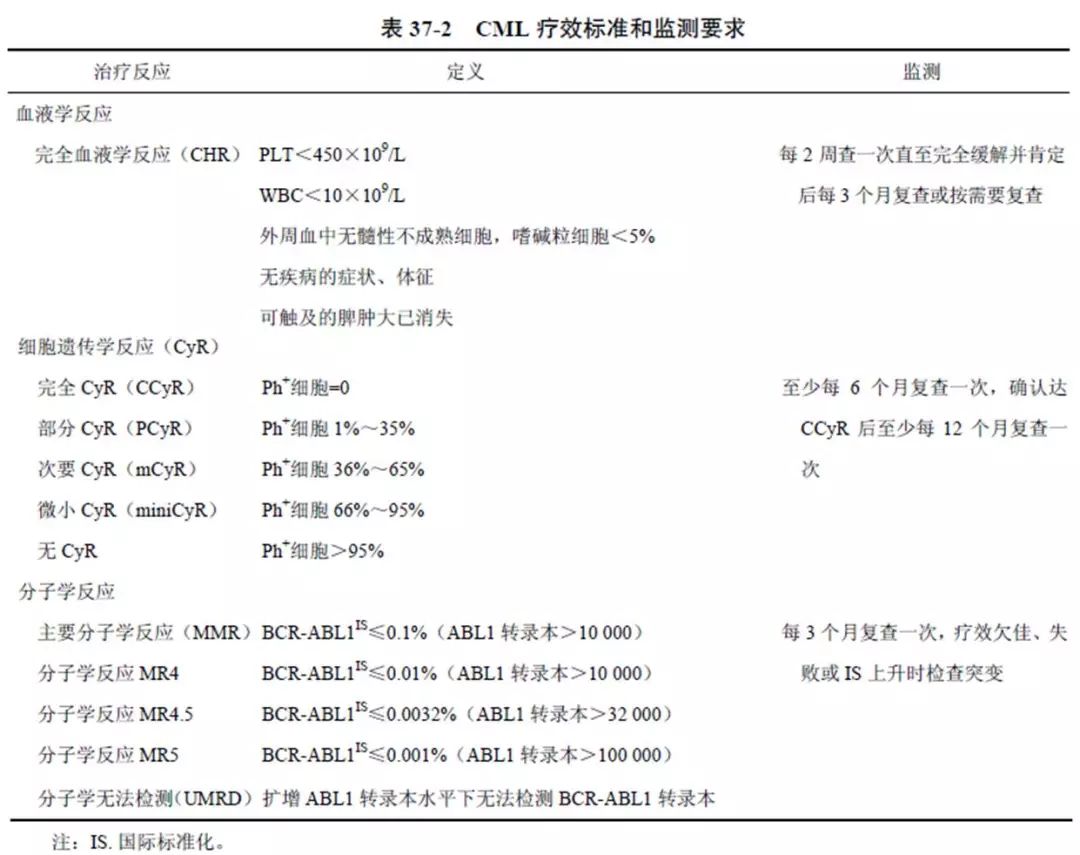
现今国内外不论用哪一代TKI治疗CML判断疗效标准与监测均按表37-2要求。CHR、CCyR及MMR必须再次确定。染色体核型分析必须检测骨髓中20个中期分裂相。当不能获得骨髓时可用FISH术测定BCR/ABL1基因替代。国外多用外周血,实时定量PCR(Q-PCR)术测定分子效应,内参基因ABL1应达10000。各实验室通过国际论证后以国际标准数IS 表示。近年来文献中用MR4.5 替代CMR。
05
“神药”疗效标准
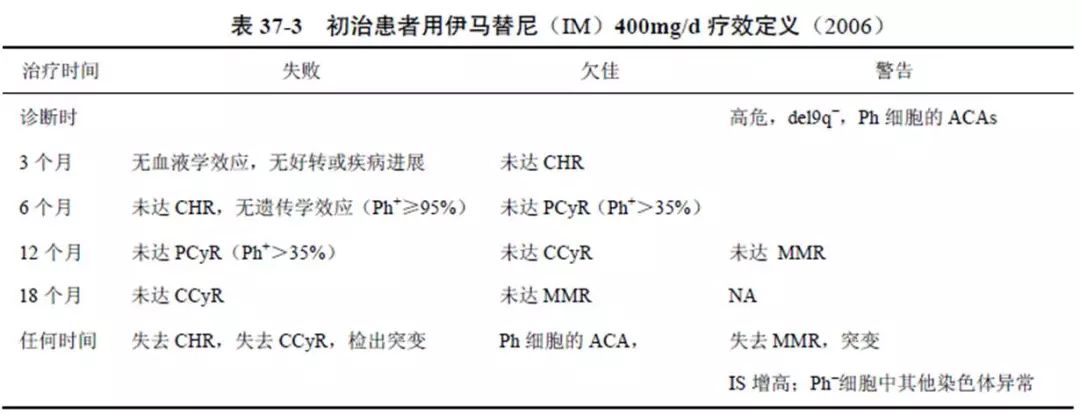
TKI时代确立了严格的定期判断疗效程序以决定后续治疗,防止疾病进展。下表中示2006年欧洲组提出对伊马替尼一线治疗CML-CP患者(400mg/d)疗效不佳标准。治疗失败者必须立即更换治疗,欠佳者可继续观察或有转机,但远期疗效不甚乐观。警告(包括增加伊马替尼剂量后疗效仍未达标者)意味着必须密切观察或更适合于其他治疗。凡获得或失去CHR/CCyR/MMR者,必须复查确定,除非已进展至AP/BC 期。突变指BCR-ABL1激酶区突变,血或骨髓中存在对高浓度伊马替尼(IM)不敏感的突变者属治疗失败。对低浓度IM不敏感突变者属疗效欠佳。2009 年Goldman 又提出治疗3个月达CHR,Ph+<65%,6个月Ph+<35%,12个月获CCyR,18个月MMR 为最佳疗效标准。虽然表37-3 所示疗效定义被多数国家所采用。但欧美之间仍有不同观点。
06
停止治疗的标准
停止酪氨酸激酶*制剂抑**(TKI)治疗的标准:近年来各国纷纷研究停止TKI治疗。2017 年NCCN-CML指南首次提出了标准。指出临床研究虽已证明一些患者停止TKI治疗是有效和安全的。但需要严格的入选标准和更频繁的监测,及时防止疾病复燃。有些患者还可发生停药副作用。临床试验研究组以外的患者必须全部按照下述要求方可考虑停止治疗:年龄≥18 岁、无进展史的CML-CP、用已批准的TKI(伊马替尼、尼洛替尼、达沙替尼、博舒替尼或帕纳替尼)至少3年并无抗药史、稳定的分子学效应≥2年(MR4;IS≤0.01%)、2周内提供一个可靠的Q-PCR 数据(PCR 敏感性≥4~5log;以IS 报告)。停药初6个月每月复查Q-PCR,第7~24个月每2个月复查一次,维持在MMR(IS≤0.1%)者每4个月复查、恢复TKI治疗者最初6个月每月复查Q-PCR,以后每3个月复查一次。停药6个月后未获MMR 者需测定突变并每月复查分子效应连续6个月,如有停药副作用或疾病进展报告NCCN-CML组。