自2018年4月获得批准以来,奥西替尼已被广泛应用于晚期EGFR突变型非小细胞肺癌(NSCLC)患者的一线治疗。了解奥西替尼的耐药机制和当前可用的治疗方案,对于在一线治疗期间病情进展的患者选择最佳二线治疗至关重要。使用从6种奥西替尼耐药系列研究收集的数据,我们在此描述了依赖和非依赖EGFR突变的奥西替尼治疗失败机制的异质性分布。我们发现MET改变(7%-24%),EGFR C797X(0%-29%),SCLC转化(2%-15%)和癌基因融合(1%-10%)是最常见的耐药机制。这篇综述提供了循证方法对奥西替尼治疗进展后的患者进行评估及管理,以及针对该类人群的临床试验纲要。
临床肿瘤学杂志38。©2020美国临床肿瘤学会版权所有
导言
表皮生长因子受体(EGFR)突变是肺癌中最常见的可靶向驱动突变,在各类肺癌中发现率为17%-61%,且在亚洲、女性和从不吸烟的患者中发现率最高。一系列具有里程碑意义的研究确立了第一代(吉非替尼,厄洛替尼)和第二代(阿法替尼)EGFR酪氨酸激酶*制剂抑**(TKIs)作为新诊断的EGFR突变型肺癌治疗的标准。最近,最初开发用于治疗T790M介导的对第一代TKIs耐药的第三代EGFR TKI奥西替尼成为首选的一线选择,这是基于随机III期FLAURA研究的结果,在该研究中,与第一代TKI相比,奥西替尼的无进展生存期(PFS;中位数为18.9 v 10.2个月)和总生存期(OS;中位数为38.6 v 31.8个月)有所改善,并改善了对中枢神经系统转移的控制。由于奥西替尼已成为一线治疗药物,我们现在越来越面临为使用奥西替尼疾病进展的患者选择下一个治疗路线的挑战。在这篇综述中,我们总结了目前对奥西尼耐药机制的理解,并探讨了针对奥西替尼病情进展的患者的实用治疗选择。
对奥西替尼治疗肺癌患者进展的评价
如前所述,肺癌在靶向治疗中获得的耐药性可以表现为多种临床模式,包括缓慢或快速生长,寡进展或广泛的系统性进展。奥西替尼的耐药性在临床上相似;因此,我们建议对临床症状进行全面评估,并对胸部,腹部,骨盆和中枢神经系统进行完整成像,以充分评估奥西替尼进展的程度(图1)。
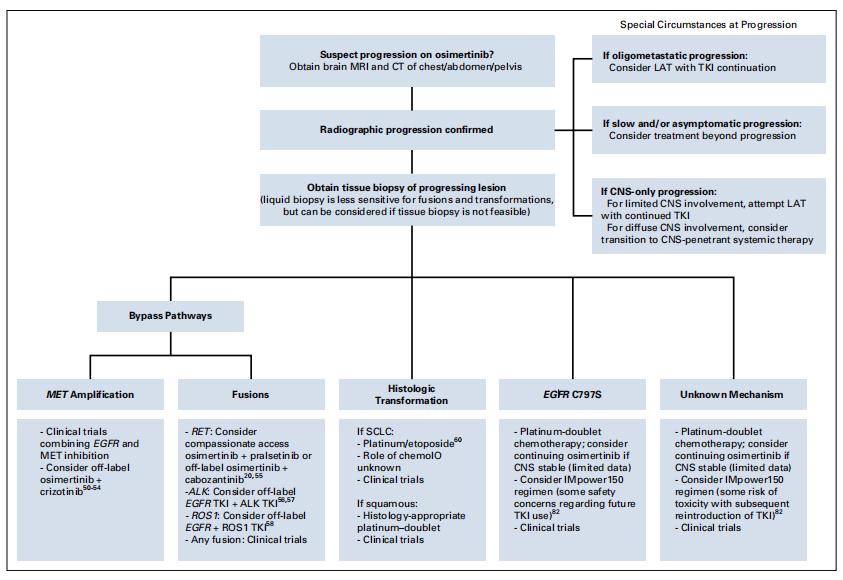
图1。治疗EGFR突变型非小细胞肺癌的方法。建议根据4种最常见的抗药性机制划分。数字参考表明支持每种方法的现有文献。相关临床试验见表2。chemoIO,化疗和PD(L)1*制剂抑**联合治疗;CT,计算机断层扫描;LAT,局部消融治疗;MRI,磁共振成像;SCLC,小细胞肺癌;TKI,酪氨酸激酶*制剂抑**。
缓慢、无症状的进展通常不需要立即进行治疗改变,许多患者可以在最初的影像学进展后安全地继续使用奥西替尼。尽管进展后的奥西替尼的前瞻性数据有限,但我们可以使用进展后的第一代和第二代EGFR TKIs的治疗数据进行推断。对于进展快速的患者,应密切监测新的疾病相关症状或肿瘤生长速度,这将促使治疗方法的改变。
对于进展缓慢的患者,可以考虑在奥西替尼治疗中增加局部消融治疗。回顾其他TKI治疗报告的数据,一项对72例EGFR突变型非小细胞肺癌(NSCLC)患者的研究结果表明,对于后线奥西替尼治疗进展的患者,局部消融治疗可显著改善中位OS(6.1至11.2个月;P 5 .02)。尽管这种做法通常可以很好地耐受并且可以改善治疗效果,但是选择偏倚可能会混淆报告的获益程度,因为病情进展迅速的患者通常会转而接受下一线系统治疗。
奥西替尼的耐药机制评估
当需要改变系统治疗时,治疗选择应尽可能以驱动耐药性的分子机制为指导。重复组织活检仍是评估奥西替尼耐药机制的金标准。为了捕获所有可能靶向的奥西替尼耐药机制(在下一节中详细讨论),我们建议将组织进行组织学评估,DNA下一代测序(NGS)和RNA为基础的融合检测。如果NGS未包括基因拷贝数增加的评估,建议使用MET荧光原位杂交(FISH)。
如果进行性疾病的部位不能安全地进行组织活检,则可以将循环肿瘤DNA(ctDNA)分析(也称为液体活检)视为一种替代方法,请记住这种方法的几个关键限制。首先,必须认识到并非所有的癌症都“脱落”足够的DNA并能通过当前的ctDNA分析方法检测到,有时这种方法的敏感性会受到限制。其次,在液体活检标本中无法检测到组织学改变,包括小细胞或鳞状细胞转化,这些都是奥西替尼的重要耐药机制。最后,必须了解所用ctDNA检测的具体特征。特别是,基因扩增和获得性癌基因融合并不总是可靠地被当前的ctDNA分析所捕获。如果ctDNA无法识别原始的EGFR突变或任何耐药机制,则应重新考虑组织活检。
对奥西替尼耐药机制的报道
自从2013年这些药物首次进入临床以来,奥西替尼和其他第三代EGFR*制剂抑**获得性耐药的机制一直是一个积极的研究领域。由于奥西替尼批准的历史顺序(最初作为T790M状态指导下的二线治疗,2年后,作为一线治疗),迄今为止,大多数对奥西替尼耐药的研究报道主要集中于二线或更晚线治疗的患者。对一线奥西替尼耐药的初步报告目前正在被呈现,而且似乎基本一致,尽管还需要更多时间才能有把握地阐明这一点。虽然已经确定了大量的潜在奥西替尼耐药机制的列表(附录表A1;仅在线提供),但在本综述中,我们将重点讨论最常见和最具临床作用的机制(表1;图2)。
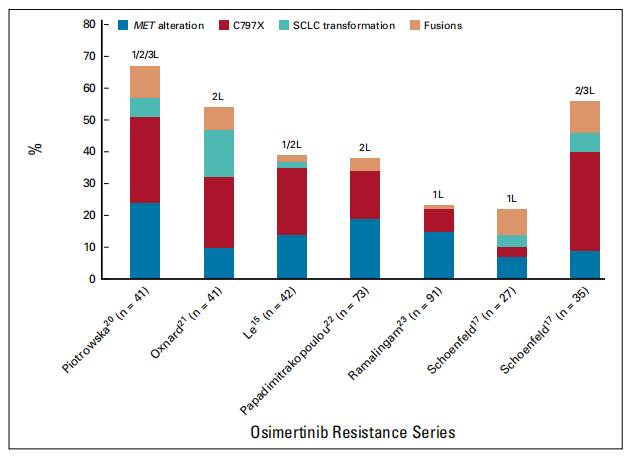
图2.构成每个奥西替尼耐药性系列的作者所组织的四种最常见耐药性机制中的每一种的病例百分比。1L,一线;2L,二线;3L,三线;SCLC,小细胞肺癌。
迄今为止,奥西替尼耐药的6个最大系列研究使用配对组织和/或液体活检标本检查了耐药机制。尽管这些研究是本次讨论的主要重点,但必须认识到几个关键的局限性。这些系列研究的大小是有限的,许多是单一机构的队列研究,此外,特别是那些一线奥西替尼治疗耐药机制的研究,可能更偏向于疾病进展早期的患者。需要更长时间的随访和前瞻性、多机构研究,例如正在进行的ELIOS试验 (ClinicalTrials.gov identifier: NCT03239340),才能更全面地了解奥西替尼的耐药性。
与先前对EGFR TKIs的获得性耐药相似,对奥西替尼的耐药可大致归类为靶向耐药(即EGFR的改变或突变),旁路信号通路的上调和组织学改变。虽然这篇综述仅限于最常见、最具特征和潜在作用的耐药机制,但许多其他假定机制也已被确定。其中包括RAS-MAPK信号通路和细胞周期基因的获得性突变、基因组不稳定性、转录重编程、表观遗传变化和上皮绒毛组织转化等(附录表A1)。这些改变对于理解奥西替尼治疗失败的复杂生物学特征是至关重要的,并且仍然是一个积极研究的领域,虽然它们的对治疗的指导意义还不明确。
我们过去一直认为耐药机制是相互排斥的,但是最近的研究表明耐药肿瘤可以显示出显著的异质性。实际上,组织活检的一个关键局限性是它们仅对单个疾病部位采样,因此可能低估了癌症的异质性。另一方面,液体活检标本可用于检测从多个疾病部位脱落的ctDNA,并有可能从单独但共存的肿瘤亚克隆中鉴定出多种假定的耐药机制。在临床上,这种情况受到了挑战,因为很难确定哪个亚克隆是耐药的主要驱动因素,应该选择其作为治疗靶标。对于具有多种耐药机制的患者,等位基因比例可能提供了对每个亚克隆相对丰度的一些了解,但在许多这样的情况下,化疗等非靶向治疗策略可能是最好的治疗方法。
一些数据表明,进展期活检标本中同时存在推定的耐药机制可能具有负面预后价值,并可能预测对可采取的治疗反应较差。EGFR的797位半胱氨酸残基的获得性耐药性点突变在临床前模型中被预测可导致对奥西替尼和其他第三代EGFR*制剂抑**的耐药,并且是疾病进展患者中最早发现的耐药机制之一。C797是不可逆TKI(如奥西替尼和阿法替尼)的共价结合位点,在此残基获得的突变会干扰药物-蛋白质的结合。某些系列研究表明氟西替尼治疗后,EGFR C797X突变的发生率高达28%,但在一线FLAURA试验的血浆样品中,EGFR C797X突变的发生率明显降低(7%)。同样,Schoenfeld等发现在奥西替尼一线治疗后,在其一系列组织活检标本中也未观察到任何C797X突变,而且靶向耐药很少见。这可能与他们的研究随访时间相对较短(一线奥西替尼治疗的中位时间为13.6个月)有关,导致样本偏向于早期进展者,以至于产生偏倚。在使用第一代EGFR TKIs出现耐药的时间较长的人群中,靶向耐药机制T790M更常见。因此,随着随访时间的延长,包括C797X突变在内的靶点耐药机制的频率可能会增加,尽管用奥西替尼作为初始TKI治疗与作为后线TKI治疗的肿瘤的生物学特征也可能不同。
尽管尚未确定靶向C797S的最佳策略,但已经出现了多种潜在的治疗方法。近期,在各种I期研究中都报告了C797S阳性患者的对治疗的反应,尽管这些结果受到患者数量较少的限制,应谨慎解释。在一项I期研究中,21名EGFR C797S患者中有7名对双特异性EGFR / MET抗体JNJ-61186372(通常缩写为JNJ-372)有反应。在另一项I期临床试验中,4例C797S阳性患者中的2例对奥西替尼和奈替妥单抗(EGFR单克隆抗体)治疗有反应。最后,在早期报告中,针对HER3的新型抗体-药物偶联物U3-1402在3例C797S患者中引起了2例局部应答。目前这3种治疗方法正在被进一步探索,正在进行的临床试验,应考虑C797S阳性的患者(表2)。此外,多臂ORCHARD研究(表2)将研究吉非替尼和奥西替尼联合治疗在一线奥西替尼后出现C797S突变的患者中的疗效。
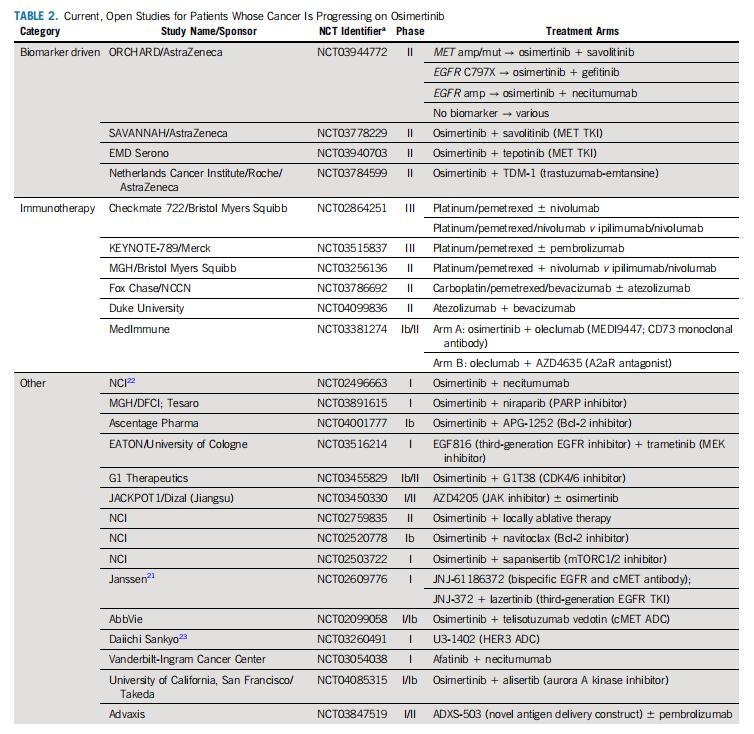
ADC,抗体偶联药物;amp,扩增;DFCI,Dana-Farber癌症研究所;MGH,马萨诸塞州总医院;mut,突变;NCI,国家癌症研究所;NCCN,国家综合癌症网络;TKI,酪氨酸激酶*制剂抑**。A所有的研究都在进行中。
其他几种策略虽然尚未应用于临床,但可能将来会应用于C797S患者的治疗中。临床前研究和病例报告显示,ALK / EGFR TKI布加替尼和抗EGFR抗体(西妥昔单抗或帕尼单抗)联合可同时抑制EGFR突变细胞系表达T790M和C797S。在临床前模型中,变构EGFR*制剂抑**(意味着它们在酪氨酸激酶结构域以外的位点结合EGFR)已显示出对C797S三重突变体的活性,另外的临床前数据表明,这些药物可能与奥西替尼具有协同作用。最近还宣布了第一个*四代第**EGFR*制剂抑**BBT-176的/ II试验。
目前,我们对具有EGFR C797X突变的患者的治疗方法是考虑参加临床试验,例如JNJ-372,奥西替尼 / 耐昔妥珠单抗,U3-1402,ORCHARD等。如果患者不能进入临床试验,我们通常使用标准化学疗法。
与奥西替尼耐药相关的其他较罕见的EGFR点突变包括G724S、 L792H和G769R。据我们所知,目前还没有发表针对这些三级EGFR突变的靶向治疗策略的报告,尽管临床前研究表明阿法替尼可能对G724S突变具有一定的活性。
最后,EGFR扩增也是奥西替尼耐药的常见发现,尽管其临床意义尚不清楚。在ORCHARD临床试验中,获得性EGFR扩增且无其他可作用靶点的患者将被纳入奥西替尼和耐昔妥珠单抗的生物标记物匹配臂中,以评估针对这一发现的作用。对于EGFR扩增患者可考虑的其他治疗策略包括JNJ-372和阿法替尼/西妥昔单抗的临床试验(表2)。
获得性MET扩增
奥西替尼耐药的患者中最常见的旁路途径是cMET扩增。尽管这一发现在第一代或第二代TKI病情进展的患者中很少见(约5%),但在使用奥西替尼治疗的患者中,有10%-24%的患者出现MET拷贝数改变。应使用NGS或FISH对所有活组织检查进行MET扩增的评估,以确定奥西替尼的耐药性,并识别可能受益于MET和EGFR*制剂抑**联合治疗的患者。
TATTON研究了奥西替尼和MET TKI 沃利替尼联合使用对于MET扩增患者的治疗效果,代表了该策略目前最大的数据集。根据MET扩增选择患者,MET扩增定义为MET基因拷贝数≥5或MET:CEP7≥2.2。在第三代TKI治疗下疾病进展且合并MET扩增的48名患者中,奥西替尼/ 沃利替尼治疗的客观缓解率为30%,中位缓解持续时间为7.9个月。在SAVANNAH(表2)和ORCHARD(表2)研究中,这一组合正在进一步研究中。
同样,在奥西替尼治疗后获得性MET扩增或MET外显子14跳跃突变的个体患者中,也报告了对奥西替尼和克唑替尼的反应和耐受性,对于无法进入MET/EGFR-TKI临床试验的患者,可以考虑使用这种组合。最后,在MET扩增患者中也可以看到JNJ-372的反应,这是在上一节中讨论的MET/EGFR双特异性抗体(表2)。重要的是,对于接受MET/EGFR-TKI联合治疗的MET扩增患者,基于抗体的方法在疾病进展后是否有效仍有待观察。
其他旁路:融合
在接受奥西替尼治疗时,随着疾病的进展,有几个团队已经确定了RET,ALK,BRAF,FGFR3和其他癌基因的获得性融合。尽管很少见,但此类融合事件似乎可以激活旁路信号通路并驱动耐药。像MET旁路途径一样,将EGFR*制剂抑**与改变的融合蛋白*制剂抑**结合起来是一种新兴的治疗策略,并且一些病例报告证明了在多种基因融合中的有效性。
我们发现将CCDC6-RET融合基因导入到EGFR突变细胞系中可导致对EGFR TKI单药治疗产生耐药性,但对RET/EGFR*制剂抑**联合治疗敏感。两名患者(1名患者在二线奥西替尼治疗后有获得性CCDC6-RET基因融合,另一名患者在阿法替尼治疗后有获得性NCOA4-RET基因融合)随后接受奥西替尼和普拉斯替尼(BLU-667)治疗,两名患者均证实部分反应。第三名患者在阿法替尼治疗后出现CCDC6-RET基因融合,并证明用奥西替尼和卡波沙丁尼治疗可以控制疾病。同样,Lu等人在57名患者(11%)中发现了获得性RET重排,这些患者的病情在使用奥西替尼治疗时进展。在这一系列研究中,有3名患者接受奥西替尼和卡波沙丁尼治疗,其中一名患者从中获益。
Offin等人报告了2例在奥西替尼治疗后获得性EML4-ALK融合基因(通过ctDNA和基于组织的FISH检测),这两例均从EGFR和ALK-TKIs(阿雷替尼或克唑替尼)的联合治疗中获益。Zhou等人报告了在奥西替尼治疗后NGS检测到的一种获得性STRN-ALK融合基因,它对吉非替尼联合克唑替尼有反应。同样,在一名EGFR外显子19缺失的患者中发现了获得性GOPC-ROS1重排,该患者的病情在奥西替尼治疗中进展,此患者表现出对奥西替尼联合克唑替尼联合治疗有部分反应。最后,我们报道了一例接受奥西替尼治疗后获得性AGK-BRAF融合的患者对奥西替尼和MEK*制剂抑**曲美替尼的反应。在这种情况下,奥西替尼/曲美替尼联合用药具有显著毒性,患者最终因放射检查发现结肠微穿孔而停止治疗,这强调并非所有的TKI组合都是可耐受的,最好在前瞻性临床试验中进行评估。
尽管治疗所有这些旁路通道突变的临床经验仍然充满不确定性,但目前的证据表明获得性基因融合是对奥西替尼耐药的复发和靶向机制,应对进展的病例进行分子水平的分析。值得注意的是,NGS可能并不总是能检测到融合,因此应该进行基于RNA的融合检测。今后,ORCHARD等多臂试验可能会提供机会,前瞻性地验证不同TKI组合治疗这些罕见但复发性融合的安全性和有效性。
组织学转化
据报道,在使用奥西替尼一线治疗的患者中,有高达15%的患者发生了组织学转变,并强调了组织活检在病情进展中的关键作用。小细胞转化已经在EGFR突变型肿瘤中得到了很好的描述,并且在第一代和第二代EGFR-TKIs治疗进展的肿瘤患者中发生率大约为3%-5%。大多数已发表的系列研究表明,在服用奥西替尼的患者中,SCLC转化发生的频率相似。与新生小细胞肺癌相似,EGFR突变型非小细胞肺癌的小细胞肺癌转化与RB1-和TP53介导的肿瘤抑制和EGFR信号丢*密失**切相关。值得注意的是,仅仅在EGFR突变肿瘤中存在RB1和TP53突变并不一定意味着发生了SCLC转化,但明确的是,具有基线TP53和/或RB1突变的EGFR突变型NSCLC在疾病过程中具有更高的SCLC转化风险。由于这一高危人群在SCLC转化之前就往往存在可检测到的TP53和/或RB1突变,血浆ctDNA检测不能用于筛查是否存在组织学转化,必须进行组织活检。在临床实践中,通过ctDNA检测到RB1和TP53突变时应提高对潜在SCLC转化的怀疑,应特别考虑进行组织活检,尤其是对疾病进展迅速的患者。
当发生SCLC转化时,我们建议像新生小细胞肺癌一样,用铂/依托泊苷化疗。在58例具有SCLC转化的EGFR突变型肺癌患者的回顾性研究中,54%的患者对铂/依托泊苷化疗有临床反应。转化后的中位生存期为10.9个月(95%CI,8.0至13.7个月)。值得注意的是,接受免疫疗法(nivolumab单一疗法或联合ipilimumab / nivolumab)治疗的17例患者均无反应,但由于入组患者的时间安排,没有人接受同时接受免疫治疗和化疗(如IMpower13364和CASPIAN65研究)。目前尚不清楚化学免疫疗法在具有SCLC转化的EGFR阳性患者中的作用。
对于具有SCLC转化的EGFR突变型肺癌患者,另一个问题是化疗后是否可以继续使用奥西替尼(或另一种EGFR TKI)进行治疗。尽管转化后的SCLC克隆可能对EGFR*制剂抑**不敏感,但耐药的亚克隆可能是异质的,SCLC转化后腺癌可能重新出现,这为临床考虑使用铂/依托泊苷或在其后继续TKI治疗提供了临床依据。重要的是,当SCLC转化患者的疾病再次进展时,最好(如果可行)重复组织取样以确定哪个克隆在推动疾病进展并指导后续治疗。
在使用奥西替尼和其他EGFR TKIs进展的肿瘤患者中,也有从腺癌到鳞状细胞癌的转变。这一现象及其对后续治疗的影响仍在研究中,但在为这些患者选择化疗时,组织学可能应予以考虑。
进展后化疗的选择
如果可能的话,我们建议考虑在奥西替尼治疗中进展且没有明确靶向耐药机制的患者参加临床试验。例如,ORCHARD试验针对一线奥西替尼进展的患者提供了生物标记物匹配和不匹配的治疗方案,并将提供有关最佳二线治疗策略的重要数据。对于无法参加临床试验的患者,以组织学为参照的铂类化疗仍然是治疗的标准。
关于一线奥西替尼治疗后开始化疗后是否继续使用奥西替尼的数据非常缺乏。IMPRESS III期研究评估了吉非替尼或安慰剂联合二线铂类化疗的益处,但未显示PFS或OS改善。然而,最近3项III期研究的结果表明, 在=一线治疗中化疗与吉非替尼联合使用可能有更显著的获益。我们等待来自随机FLAURA2研究 (ClinicalTrials.gov identifier: NCT04035486)的数据,该研究将一线奥西替尼与奥西替尼联合化疗进行比较,以及一线奥西替尼治疗后继续进行奥西替尼或安慰剂联合化疗的随机COMPEL研究 (ClinicalTrials.gov identifier pending)(具有CNS特异性转归),目前尚不清楚是否应将IMPRESS的结果外推至在一线奥西替尼上进展的疾病患者。与IMPRESS研究中的吉非替尼相反,根据我们的经验,即使面对系统性进展,奥西替尼良好的中枢神经系统渗透性也能持久控制脑转移,因此,尤其是对于奥西替尼能控制的基线脑转移的患者,在全身性疾病进展时,我们考虑在奥西替尼的基础上加用二线铂类化疗。回顾性数据表明,奥西替尼可与卡铂/培美曲塞或其他许多化疗方案联合使用。
免疫疗法
PD(L)1*制剂抑**(IO)单药治疗EGFR突变型NSCLC疗效不明显。尽管我们的经验表明,当IO用于以后的治疗方案时,效果似乎同样差,应答率为仅为10%,无论PD-L1的状态如何,治疗的中位持续时间均为1个月。最新靶向免疫的数据表明,较高的PD-L1可能预示了EGFR突变型NSCLC的IO获益。然而,我们很少对EGFR突变的患者使用IO单药治疗,而是尽可能选择临床试验和/或化疗,尤其是对于PD-L1-低肿瘤患者(大多数)。
对于在奥西替尼治疗中进展并转到二线化疗的EGFR突变型患者,由于其被完全排除在KEYNOTE-189研究之外,并且只有一小部分患者进入IMpower150和IMpower130研究,其化疗联合免疫疗法的作用还不清楚。IMpower150研究表明在卡铂/紫杉醇和贝伐单抗(ABCP)中加入阿特珠单抗时证明了PFS和OS的获益,是迄今为止唯一一个证明EGFR突变型患者受益的化学免疫治疗的临床试验,尽管在这项研究的802名患者中,只有59名已知EGFR致敏突变的患者。此外,仅在IMpower150的四药ABCP组中观察到加入阿特珠单抗对EGFR突变型患者获益,而将卡铂,紫杉醇和阿特珠单抗与单用化疗相比较,并没有看到阳性结果。另外,在IMpower130试验中也并未得到阳性结果,这项试验旨在评估阿特珠单抗联合白蛋白紫杉醇/卡铂对比单纯化疗是否有获益。这些结果增加了PD-L1*制剂抑**和抗血管生成剂可能改善EGFR突变型患者的化疗疗效。更多的研究正在进行中,以确定抗血管生成剂、免疫治疗和化疗在EGFR突变型患者中的作用(表2)。
值得注意的是,新出现的数据表明,当患者在免疫治疗后接受EGFR-TKI治疗时,毒性反应可能出现更频繁。尽管先前的研究表明,同时接受奥西替尼和度伐单抗的患者肺炎的发生率高达38%,但免疫治疗后使用TKI也似乎增加了这种风险。 最近的一项回顾性研究表明,当患者在接受免疫检查点*制剂抑**治疗后3个月内开始使用奥西替尼时,严重的免疫相关不良事件(尤其是肺炎)的发生率高达24%。因此,对于最近接受免疫治疗的患者,应谨慎使用奥西替尼。
脑转移患者
最后一组需要特别考虑的是存在CNS转移的EGFR突变阳性的肺癌患者。中枢神经系统疾病在这一人群中很常见。在FLAURA试验中,大约20%的患者出现CNS转移,而奥西替尼强大的CNS渗透能力。可能是该药物治疗有效的原因。在FLAURA研究表明在脑转移患者中,奥西替尼将PFS延长至15.2个月(95%CI ,12.1至21.4),而第一代TKI则为9.6个月(95%CI,7.0至12.4)。BLOOM试验还显示,奥西替尼在软脑膜病(LMD)患者中是有效的。LMD患者每日服用奥西替尼160mg一次,在12周后的影像学检查中,32例患者中有23例影像学提示疾病稳定或改善,8例患者中的7例在12周后的神经学评估中显示症状改善。在使用奥西替尼治疗中枢神经系统疾病的患者中,全面分期对于确认是否存在并发的系统性疾病进展至关重要。如果确认了颅外进展,则应进行组织和/或液体活检以指导进一步治疗,如本综述前面所述。对于仅具有中枢神经系统进展的患者,液体活检标本通常不易发现,而脑活检可能是高风险的手术。通常仅针对具有与软脑膜受累症状的患者考虑进行腰椎穿刺CSF采样,即使在这些情况下,也很少有关于CSF分子分析准确性的数据。不幸的是,即使检测到可行的突变,活动性中枢神经系统转移的患者通常也不适合进行临床试验,从而有可能限制靶向治疗的机会。
尽管BLOOM试验使用的是每天160 mg的奥西替尼,而不是80mg的标准剂量,但该试验的患者是初次使用奥西替尼,其益处可能与引入奥西替尼而不是更高剂量有关。对于服用80mg奥西替尼的患者,在中枢神经系统进展时剂量增加到160mg是否足以诱导中枢神经系统反应,目前还缺乏相关数据。如果采用剂量递增策略,我们建议仔细监测神经系统症状和进行短间隔影像成像。更常见的是,我们考虑继续使用奥西替尼或进行局部消融治疗(放疗和/或手术)以减慢疾病进展。如果发现多灶或中枢神经系统快速进展,如果可能的话,我们倾向于过渡到已知颅内穿透的替代性全身治疗。在这种情况下,卡铂/培美曲塞,加或不加贝伐单抗,特别有吸引力。对于无症状,多灶性中枢神经系统进展的患者,需要全脑放疗以控制其转移,我们通常将放疗推迟,以免中枢神经系统对全身治疗快速反应时,出现放疗的长期认知毒性。
综上所述,本综述提供了目前关于使用奥西替尼治疗肿瘤进展患者的可用数据,并说明了耐药机制的异质性和临床治疗的指导概念。尽管还需要更多的研究来更清楚地描述每种耐药机制的最佳治疗方法,但目前已经有许多选择,本综述旨在为奥西替尼治疗后的进展提供一个实用指南。
翻译编写:Cathy
审核校对:中山大学肿瘤防治中心 朱娴颖博士 刘俊玲教授
郑重声明:本文分享内容仅供医疗工作者阅读使用,其他平台未经授权不得擅自转载。转载请联系获得授权。