在2021年,妇科恶性肿瘤治疗领域取得哪些新进展?在本文中,复旦大学附属肿瘤医院吴小华教授对宫颈癌、卵巢癌和子宫内膜癌的年度重要研究进行梳理, 与同行一起分享。
宫颈癌年度盘点
局部晚期宫颈癌根治性治疗
OUTBACK研究:放化疗后辅助化疗 vs 单纯放化疗治疗局晚期宫颈癌
OUTBACK研究为大样本III期国际多中心的随机对照研究,纳入926例IB1(淋巴结阳性)、IB2、II、IIIB和IVA患者(FIGO 2008),随机分组接受同期放化疗vs. 同期放化疗联合辅助化疗。2021 ASCO公布的结果显示,局部晚期宫颈癌根治性放化疗后行辅助化疗未改善患者的无进展生存(PFS)和总生存(OS),5年OS率相似(72% vs 71%);5年PFS率也相近(63% vs 61%)。[1]
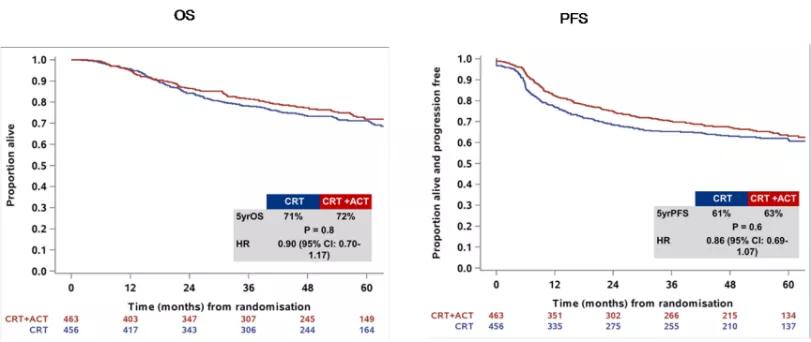
OUTBACK研究结果
OUTBACK研究也存在一些局限性,比如入组辅助化疗组的患者中有接近22%患者未行辅助化疗;该研究参与中心皆为经济条件较高的地区,未入组低收入水平国家人群。未来研究重点应关注IVA期宫颈癌、腹膜后(PA)淋巴结转移的患者,以及其他可耐受的辅助化疗方案。
宫颈癌复发/转移一线治疗
KEYNOTE-826 研究:帕博利珠单抗联合化疗vs安慰剂联合化疗治疗持续性、复发性或转移性宫颈癌
KEYNOTE-826入组了616例既往未接受过系统化疗的持续性、复发性或转移性宫颈癌患者,1∶1随机入组至帕博利珠单抗+化疗±贝伐珠单抗组或安慰剂联合化疗±贝伐珠单抗组。结果显示:①研究组相比对照组显著提高该人群PFS和OS,在所有的主要分析人群(PD-L1 CPS≥1、全人群和CPS ≥10)中均获得显著的临床获益;②所有亚组获益一致,包括使用或不使用贝伐珠单抗的亚组;③PD-L1 CPS≥1、CPS≥10和ITT人群的24个月OS率分别为53.0%、54.4%和50.4%,相较于对照组的OS HR分别为0.64、0.61和0.67;④研究组的客观缓解率(ORR)更高,缓解持续时间(DOR)更长;⑤试验组的AE总体可管理,免疫介导不良反应(AE)发生率高于对照组,试验组的不良反应与PD-1*制剂抑**单药的不良反应一致。
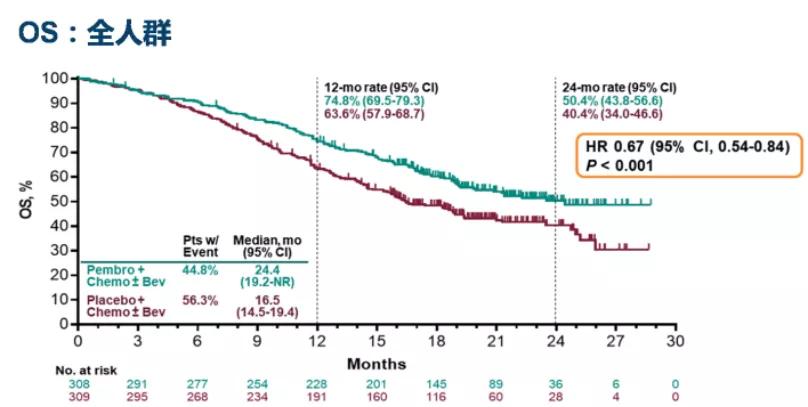
KEYNOTE-826研究ITT人群的OS
KEYNOTE-826使得帕博利珠单抗联合化疗±贝伐珠单抗成为持续性、复发性或转移性宫颈癌新的标准治疗方案。2022年V1版宫颈癌随即更新,将其纳入宫颈癌系统治疗一线推荐。
宫颈癌复发/转移二线及以上治疗
Ⅲ期EMPOWER-Cervical 1/GOG-3016/ENGOT-cx9:在复发性/转移性(R/M)宫颈癌患者中比较cemiplimab与研究者选择(IC)化疗
这项Ⅲ期随机临床研究纳入608例既往接受过含铂一线治疗后进展的R/M宫颈癌患者(477例宫颈鳞癌患者,131例宫颈腺癌患者),随机1∶1分别进入抗PD-1*制剂抑**Cemiplimab组或IC化疗对照组(培美曲塞、长春新碱、拓扑替康、伊立替康或吉西他滨)。对照组没有使用我国常用的紫杉醇等化疗药物。
这是迄今为止在该人群中进行的最大规模的随机研究,结果显示:①在鳞癌患者中,试验组和IC化疗组的中位OS为11.1 vs 8.8个月(HR=0.73);②在总体人群和腺癌人群中观察到OS和ORR双获益;③基于可用的肿瘤样本,在PD-L1<1%人群中观察到Cemiplimab相比IC化疗的OS绝对值获益,但在PD-L1≥1%患者中OS获益更大;④PD-L1≥1%和<1%的患者中使用Cemiplimab均观察到了客观缓解;⑤在总体人群中,GHS/QoL较基线的总体平均变化支持Cemiplimab(单侧标称P值<0.001)的使用,研究未发现新的安全性信号。[3]
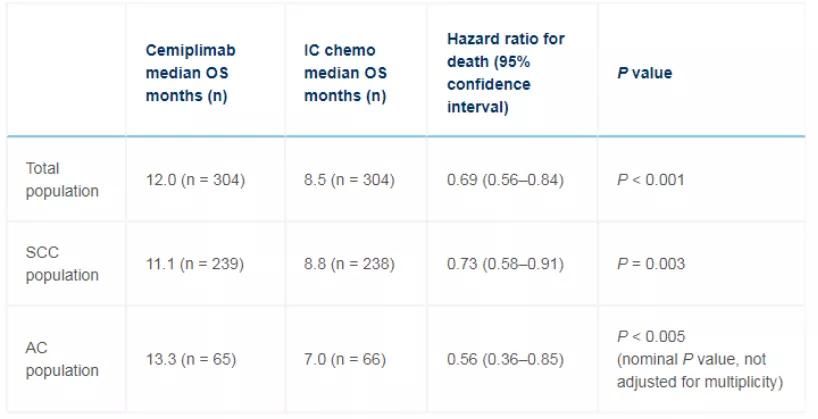
EMPOWER-Cervical 1总体人群的生存分析
ADC药物Tisotumab Vedotin+卡铂用于一线或联合帕博利珠单抗用于复发性/转移性宫颈癌:ENGOT-Cx8/GOG-3024/innova 205研究的中期结果
该研究的剂量扩展阶段包括一线 TV(Tisotumab Vedotin)+卡铂用于既往未接受过系统治疗的复发性/转移性宫颈癌患者队列,以及二/三线TV+帕博利珠单抗用于既往1-2 次系统治疗期间/之后疾病进展的患者队列。根据2021年ESMO年会的报道,两个队列中均显示出令人鼓舞的抗肿瘤活性,经确认的一线 TV+卡铂的ORR为55%(18/33),二/三线TV+帕博利珠单抗的ORR为38%(13/34),安全性可管可控。[4]
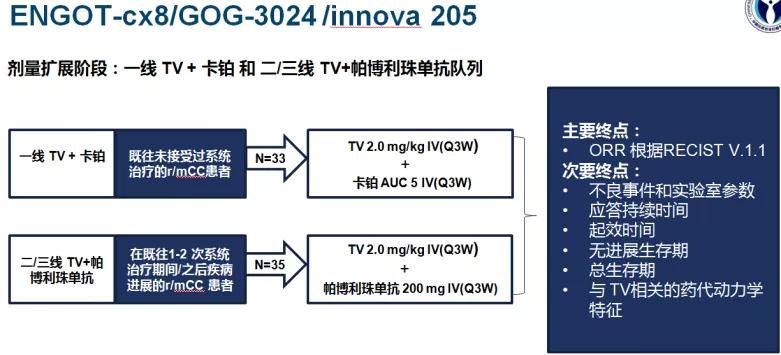
ENGOT-Cx8/GOG-3024/innova 205研究设计
这些数据支持进一步研究以评估加入TV的其他联合方案作为复发性/转移性宫颈癌的治疗选择。TV+帕博利珠单抗一线治疗的剂量扩展队列研究正在进行中,并将在未来的会议上报告。
安罗替尼联合信迪利单抗治疗复发性晚期宫颈癌患者:一项前瞻性、多中心、单臂、Ⅱ期临床研究
研究纳入接受过至少一线含铂化疗的复发性晚期宫颈癌且PD-L1阳性的患者,给予安罗替尼(10 mg qd,d1-14,21天/周期)和信迪利单抗(200 mg q3w)治疗。在疗效评价人群中,ORR为59%,DCR为94.9%,中位PFS为9.40个月。36例(85.8%)患者发生至少1例治疗相关不良事件(TRAE),7例(16.7%)患者发生3级TRAEs。[5]
卵巢癌年度盘点
卵巢癌的初始治疗
- R0仍然是手术追求的目标: 卵巢癌在2021年的研究进展不太多。2021 ESMO展示的一项回顾性研究进一步证明手术切除越干净,患者的OS越好,任何程度的残留均不利于患者的OS。[6]
- 更多的手段运用到IDS: 2021 SGO报道的MIID-SOC试验显示,通过腹腔镜评估对晚期卵巢癌进行微创中间型减瘤术(IDS)有一定预测意义。[7]2021 ASCO的一项报道显示,使用Pafolacianine注射液用于叶酸受体阳性卵巢癌术中成像,有助于识别可能会遗漏的病灶,这可能有助于外科医生实现完全肿瘤细胞减灭。[8]
- 新辅助免疫治疗正在探索,但尚未突破: 2021 SGO报道了德瓦鲁单抗+替西木单抗+新辅助化疗(NACT)治疗晚期上皮性卵巢癌的KGOG 3046/TRU-D研究,初步结果显示该方案具有一些临床疗效和可控的毒性。[9]2021 ASCO报道的一项GINEGO研究显示帕博利珠单抗+NACT治疗高级浆液性卵巢癌(HGSC)患者无PFS获益。[10]
- 一线维持治疗,PARPi以外的选择: 2021 ASCO发布了一项旨在探索贝伐珠单抗(BEV)联合卡铂和紫杉醇用于初治晚期卵巢癌患者最佳疗程的III期随机临床试验,结果证明BEV维持治疗15个月和30个月的PFS和OS无显著差异,BEV一线维持无需延长疗程。[11]复旦大学附属肿瘤医院在2021 SGO展示的一项壁报证明“三步化疗”延长无进展生存,尤其是BRCA野生型和HRP患者。[12]
- 一线免疫治疗无显著进展 :目前还不知道哪些患者可以从一线免疫治疗中获益。JAVELIN Ovarian 100 试验已提前终止,ENGOT-OV42/NSGO-AVATAR 撤回研究。
复发卵巢癌的治疗
- 复发卵巢癌的手术治疗: 2021 ASCO报道的NORA二次减瘤术亚组分析显示,无论是接受二次减瘤术还是非二次减瘤术的患者使用尼拉帕利维持治疗,均能够较安慰剂组延长PFS,并且该获益在二次减瘤术组更多。二次减瘤+PARPi维持治疗是最佳搭档,但手术达到R0很重要。[13] Gynecol Oncol 的一项研究证明了三次减瘤术也有益处。[14]
- 复发卵巢癌的PARPi治疗: L-MOCA结果印证了奥拉帕利对于中国铂敏感复发患者的疗效。[15]2021 ASCO更新的Ⅲ期ARIEL4亚组数据显示,Rucaparib单药对比化疗能提高铂敏感及部分铂敏感患者的ORR,助力“去化疗”策略的探索。[16]
- PARPi以外的尝试 :ADC药物在卵巢癌中的研发如火如荼,2021 ASCO报道的一项研究发现,ADC药物索星-米妥昔单抗(MIRV)联合贝伐珠单抗,铂耐药和铂敏感人群均可获益,肿瘤叶酸受体-α(FRα)高表达者的获益更显著。[17]
- PARPi再维持的获益者有限: OReO/ENGOT Ov-38是第一个提供了铂敏感复发卵巢癌再次使用PARP*制剂抑**研究数据的临床研究,结果显示这种策略似乎可行,但获益幅度有限。[18]真实世界研究也发现,PARPi治疗后使用化疗的ORR也仅有40%。[19]
- 复发卵巢癌的免疫治疗: JAVELIN Ovarian 200试验对比了PLD(脂质体阿霉素)vs PLD+Avelumab治疗铂耐药或铂难治的卵巢癌患者,分别检验了OS和PFS,研究显示联合治疗无明显额外获益。[20]EORTC-1508是首项联合抗PD-L1抗体阿替利珠单抗(ATE)与BEV和不可逆COX1/2*制剂抑**乙酰水杨酸(ASA)的试验。结果显示,与BEV或ATE(+/-ASA)组相比,BEV+ATE联合治疗带来的PFS和TFST(至首次后续治疗的时间)改善差强人意。[21]GINECO BOLD试验中,BEV+奥拉帕利(OLA)+德瓦卢单抗(DURVA)使复发性晚期卵巢癌患者获益,这是一个大胆尝试,但结果并不惊艳。[22]
子宫内膜癌年度盘点
309/KEYNOTE-775研究:仑伐替尼 +帕博利珠单抗治疗铂类经治的晚期子宫内膜癌患者
子宫内膜癌研究在2021年也没有非常重磅的结果。III期309/KEYNOTE-775研究验证了“可乐”组合在既往接受过一线含铂化疗的转移性或复发性子宫内膜癌患者中的疗效。2021 SGO发布的结果显示,在包括组织学类型、MMR状态和既往治疗线数在内的各患者亚组中,均观察到仑伐替尼+帕博利珠单抗相比化疗组的PFS和OS获益。研究组和对照组的≥3级TEAE分别为88.9%和72.7%,导致减量或停药的任何TEAE在研究组显著更高。[23]
KETNOTE-158:帕博利珠单抗治疗高微卫星不稳定性(MSI-H)或错配修复缺陷(dMMR)的经治晚期子宫内膜癌患者
2021 ESMO 发布了对II期KETNOTE-158(NCT02628067)队列D和队列K中MSI-H/dMMR子宫内膜癌患者的42.6个月随访数据,这些患者接受了帕博利珠单抗(200mg IV Q3W)单药治疗,ORR为48%,预计68%的患者DOR≥3年;生存预后令人鼓舞,预计4年生存率达60%;毒副作用可控,且与既往在实体瘤治疗中的结果一致。[24]
小结
- 宫颈癌的治疗始终遵循 个体化标准治疗 ,随着肿瘤精准治疗的不断发展,现有的医疗手段和药物治疗将逐步完善既往治疗模式的局限与不足,靶向治疗和免疫治疗逐步成为宫颈癌治疗的“新*器武**”。
- 卵巢癌靶向治疗不断突破,包括PARPi及抗血管生成药物等在复发治疗及一线维持治疗中均显示了令人鼓舞的生存获益。对 PARPi耐药 后的治疗也在不断探索。
- 分子技术的发展、 新靶点 的探索也为晚期实体瘤带来了新的治疗手段,期待进一步深入此类药物的研究,筛选出可能潜在受益的患者,为肿瘤治疗带来新希望。
参考文献:
1. Linda R, et al. Adjuvant chemotherapy following chemoradiation as primary treatment for locally advanced cervical cancer compared to chemoradiation alone: The randomized phase III OUTBACK Trial (ANZGOG 0902, RTOG 1174, NRG 0274). Journal of Clinical Oncology, 2021 39:18_suppl, LBA3
2. Colombo N, et al. Pembrolizumab plus chemotherapy versus placebo plus chemotherapy for persistent, recurrent, or metastatic cervical cancer: randomized, double-blind, phase 3 KEYNOTE-826 study. ESMO Congress, 2021, Abstract LBA2
3. Tewari KS, et al. EMPOWER-Cervical 1/GOG-3016/ENGOT-cx9: Results of Phase 3 trial of cemiplimab vs investigator’s choice (IC) chemotherapy (chemo) in recurrent/metastatic (R/M) cervical carcinoma. ESMO 2021 Virtual Plenary Debate4
4. I Vergote, et al. Tisotumab Vedotin + Carboplatin in First-Line or+plizumab in Previously Treated Recurrent/Metastatic Cervical Cancer:Interim Resultsof ENGOT-Cx8/GOG-3024/innova TV 205. ESMO 2021 723MO.
5. Qin Xu et al. Anlotinib plus sintilimab in patients with recurrent advanced cervical cancer: A prospective, multicenter, single-arm, phase II clinical trial. ESMO 2021 774P.
6. Impact of Residual Disease on Outcomes in Patients With Ovarian Cancer: A Meta-Analysis. ESMO 2021,761P
7. Anthony Costales, et al. Laparoscopic predictability of minimally invasive interval debulking in advanced ovarian cancer: The MIID-SOC trial. SGO2021,Abs10926.
8. Janos Laszlo Tanyi, et al. Phase 3, randomized, single-dose, open-label study to investigate the safetyand efficacy of pafolacianine sodium injection (OTL38) for intraoperative imaging of folate receptor positive ovarian cancer. 2021 ASCO, abs 5503.
9. a phase II study of durvalumab and tremelimumab with front-line neoadjuvant chemotherapy in patients with advanced-stage epithelial ovarian cancer(KGOG 3046/TRU-D). SGO 2021,Abs65.
10.Isabelle Laure Ray-Coquard,et al. Efficacy and safety results from neopembrov study, a randomized phase II trial of neoadjuvant chemotherapy (CT) with or without pembrolizumab (P) followed by interval debulking surgery and standard systemic therapy ± P for advanced high-grade serous carcinoma (HGSC): A GINECO study. ASCO 2021,Oral5500.
11. Jacobus Pfisterer, et al. Optimal treatment duration of bevacizumab (BEV) combined with carboplatin and paclitaxel in patients (pts) with primary epithelial ovarian (EOC), fallopian tube (FTC) or peritoneal cancer (PPC): A multicenter open-label randomized 2-arm phase 3 ENGOT/GCIG trial of the AGO Study Group, GINECO, and NSGO (AGO-OVAR 17/BOOST, GINECO OV118, ENGOT Ov-15, NCT01462890).2021 ASCO, abs 5501.
12. ZhongZheng, Xiaohua Wu. Maintenance adjuvant chemotherapy of three steps (ACTS) in patients with newly diagnosed advanced ovarian cancer:a randomized open-label ,controlled phase II trial. SGO 2021,poster
13. Lingying Wu,et al. Efficacy of niraparib maintenance therapy in Chinese women with platinumsensitive recurrent ovarian cancer with and without secondary cytoreductive surgery: Results from the NORA trial. 2021 ASCO,abs 5534.
14. Tertiary cytoreduction for recurrent ovarian carcinoma: an updated and expanded analysis. Gynecol Oncol. 2021;162(2):345-352
15. L-MOCA: An open-label study of olaparib maintenance monotherapy in platinum-sensitive relapsed ovarian cancer. ASCO 2021,e17526.
16. Subgroup analysis of rucaparib versus chemotherapy as treatment for BRCA-mutated, advanced, relapsed ovarian carcinoma: Effect of platinum sensitivity in the randomized, phase 3 study ARIEL4.ASCO 2021,5517
17.David M. O’Malley , et al. Mirvetuximab soravtansine, a folate receptor alpha (FRa)-targeting antibodydrug conjugate (ADC), in combination with bevacizumab in patients (pts)with platinum-agnostic ovarian cancer: Final analysis. 2021 ASCO, abs 5504.
18. Eric Pujade-Lauraine, et al. Maintenance olaparib rechallenge in patients (pts) with ovarian carcinoma (OC) previously treated with a PARP inhibitor (PARPi): Phase IIIb OReO/ENGOT Ov-38 trial. 2021 ESMO. Abstract LBA33.
19. Romeo Marin, et al. Real-world-data (RWD) on platinum (Pt)-based chemotherapy (CT) after PARP inhibitors (PARPi) in high-grade serous (or endometrioid) ovarian cancer (HGSEOC). ESMO 2021 748P
20. Eric Pujade-Lauraine, et al. Avelumab alone or in combination with chemotherapy versus chemotherapy alone in platinum-resistant or platinum-refractory ovarian cancer (JAVELIN Ovarian 200): an open-label, three-arm, randomised, phase 3 study.Lancet Oncol. 2021;22(7):1034-1046.
21. BanerjeeS.,et al.Principal results of the EORTC-1508 trial: A phase II randomised, multicentre study of bevacizumab vs atezolizumab and bevacizumab with acetylsalicylic acid or placebo in recurrent platinum-resistant ovarian, fallopian tube or primary peritoneal adenocarcinoma. ESMO 2021,LBA32.
22. G. Freyer A, et al. Bevacizumab (Bev), olaparib (Ola) and durvalumab (Durva) in patients with recurrent advanced ovarian cancer (AOC): The GINECO BOLD study. ESMO 2021,733P
23. Makker, et al. Study 309/KEYNOTE-775: Lenvatinib + Pembrolizumab After Platinum in Advanced Endometrial Cancer. SGO 2021. Abstr 11512.
24.O’Malley DM, Bariani GM, Cassier PA, et al. Pembrolizumab in patients with microsatellite instability–high advanced endometrial cancer: results from the KEYNOTE-158 study. J Clin Oncol. Published online January 6, 2022. doi:10.1200/JCO.21.01874