β-内酰胺类药物(β-lactamsdrug)是指结构中含有β-内酰胺环的一大类抗生素,根据母核结构差异可分为青霉素类、头孢菌素类、碳青霉烯类和单环β-内酰胺类等大类,其中青霉素类药物和头孢菌素类药物在兽医临床应用最为广泛。本部分综述了β-内酰胺类药物的结构与分类、理化性质、药动学研究、毒理学研究、国内外限量要求以及残留检测的样品前处理、仪器测定方法等内容,以期为该类药物的全面了解和残留检测提供参考。
1 结构与分类
1.1 结构
β-内酰胺类药物结构中均含有β-内酰胺母核的四元环结构,这类结构在天然产物中较为罕见,是该类抗生素的代表性特征。其中青霉素类和头孢菌素类应用最为广泛,它们的结构特征见图5-39。

(1)基本结构由母核和侧链两部分组成。母核部分都含有一个四元的β-内酰胺环,内酰胺环通过氮原子及其邻近的3个碳原子与第二个五元环或六元环相稠合。青霉素类的稠合环是氢化噻唑环,母核结构为6-氨基青霉烷酸(6-amino penicillinic acid,6-APA);头孢菌素类的稠合环是氢化噻唑环,母核结构为7-氨基头孢霉烷酸(7-amino cephalosporanic acid,7-ACA)。
(2)C6或C7位含有酰胺基侧链(RCONH—),其常为侧链的连接点。
(3)母核结构中了2个稠合环不共面,青霉素类沿N1~C5轴折叠,头孢菌素类沿N1~C6轴折叠。
(4)青霉素类母核含有3个手性碳原子,8个旋光异构体中仅绝对构型为2S、5R、6R的具有活性,故全合成十分困难;头孢菌素类母核含有2个手性碳原子,有活性的绝对构型为6R、7R,它们的药效还与RCONH—取代基的手性碳原子有关。
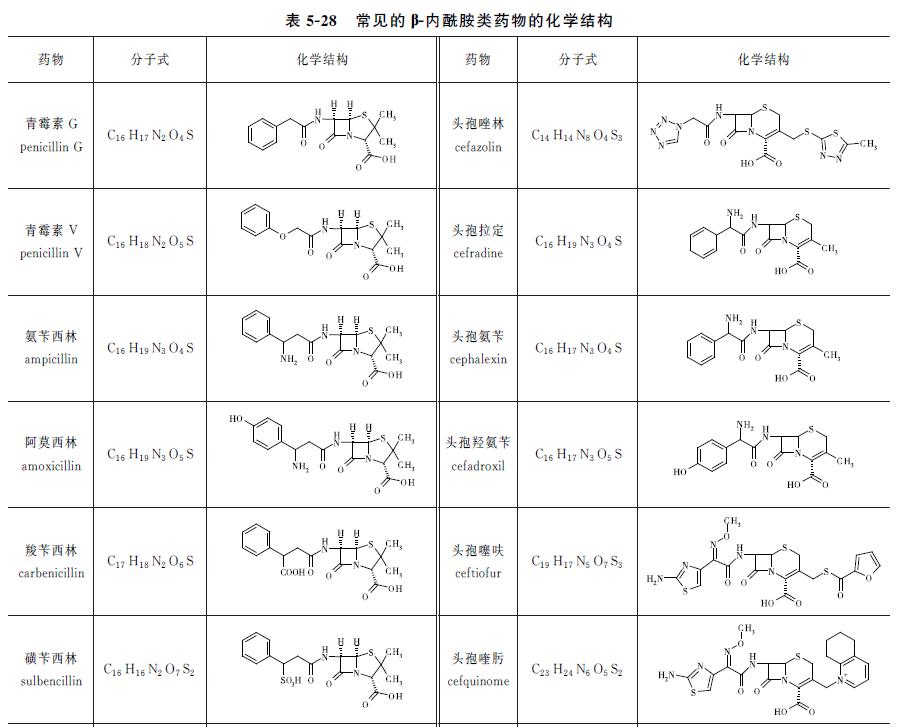
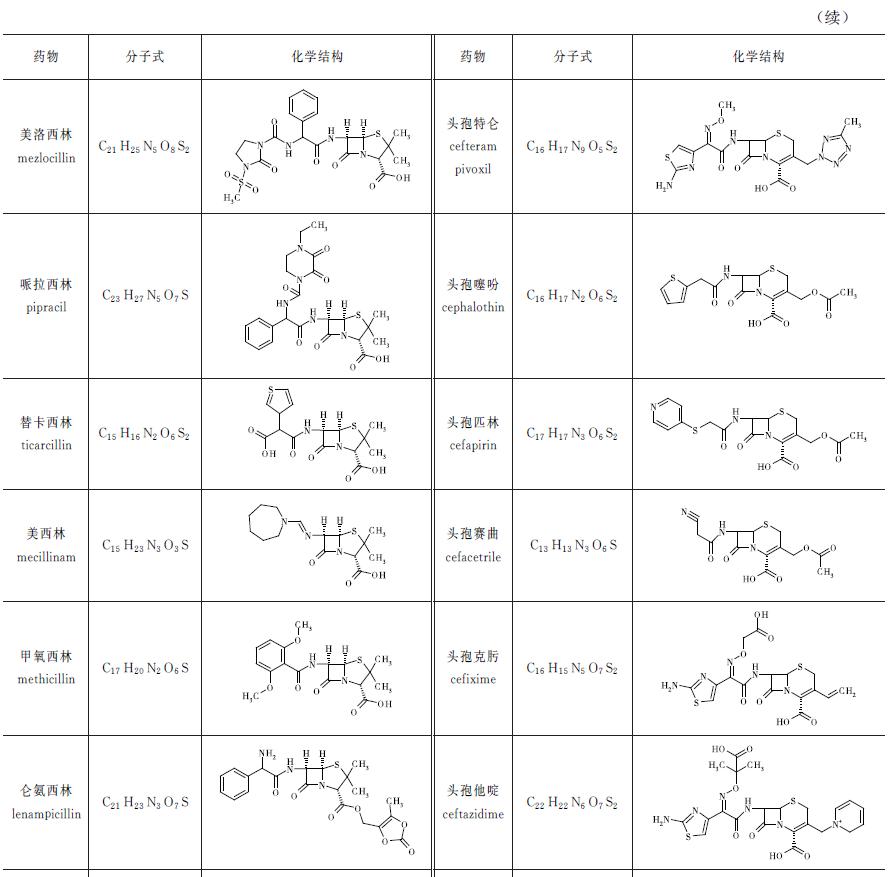
常见的β-内酰胺类药物的化学结构如表5-28所示。


1.2 分类
1.2.1 青霉素类药物的分类
青霉素类药物分为天然青霉素和半合成青霉素,天然青霉素由微生物发酵液提取而来,包括青霉素F、青霉素G、青霉素X、青霉素K和双氢青霉素F5种成分,其中以青霉素G含量最高、疗效最好;半合成青霉素通过改变侧链结构而合成。
根据青霉素类药物的抗菌谱,将其分为五大类,第一类主要用于抗不产β-内酰胺酶的革兰氏阳性菌包括葡萄球菌、链球菌属、芽孢杆菌等所致的感染,属于窄谱青霉素,代表抗生素有青霉素G(注射用)钠盐和钾盐、青霉素V(口服用)、普鲁卡因青霉素、苄星青霉素等;第二类为氨基青霉素,其抗菌谱广,代表抗生素有氨苄西林、阿莫西林等;第三类为耐青霉素酶的青霉素,对青霉素酶稳定,主要用于抗产酶葡萄球菌所致的各种感染,其抗菌谱窄,代表抗生素有氯唑西林、双氯西林、苯唑西林、氟氯西林等;第四类为对绿脓杆菌等假单胞菌有活性的广谱青霉素,代表抗生素有羧苄西林、替卡西林、哌拉西林、阿洛西林、美洛西林等;第五类为主要作用于革兰氏阴性菌的青霉素,仅对肠杆菌科细菌具有良好作用,抗菌谱窄,代表抗生素有美西林、匹美西林、替莫西林等。
1.2.1 头孢菌素类药物的分类
头孢菌素类药物均为半合成药物,主要合成方式是在母核结构的R1、R2位引入不同的侧链基团,根据合成时间的先后可将头孢菌素类药物分为四代。第一代头孢菌素对青霉素酶稳定,但对多数革兰氏阴性菌产生的β-内酰胺酶抵抗力差,包括头孢氨苄、头孢拉定、头孢唑林、头孢羟氨苄等药物。第二代头孢菌素包括头孢呋辛、头孢孟多等,药物产量相对较少,此类药物近年来逐渐在医学临床上被使用,但很少用于动物临床。第三代头孢菌素包含种类较多,临床常用药物有头孢噻肟、头孢哌酮、头孢他啶、头孢曲松等,这些药物对β-内酰胺酶稳定,对厌氧菌及革兰氏阴性菌均有显著作用。*四代第**头孢菌素广谱、高效、对β-内酰胺酶高度稳定,主要用于顽固的感染性疾病的治疗,包括头孢喹诺、头孢匹罗等。其中,第三代的头孢噻呋和*四代第**的头孢喹诺是动物专用药,疗效确实。
2 理化性质
β-内酰胺类药物在水和油性有机溶剂中溶解性差,故临床用药多为其钾盐或钠盐,盐类可溶于水、*腈乙**、甲醇和乙醇等极性溶剂,外观为白色结晶或粉末,无臭或有特异性臭,有不同程度的吸湿性。β-内酰胺类药物多具有旋光性,青霉素类药物母核缺乏紫外吸收性质,其紫外吸收通常来自侧链上的苯环,特征性不强;头孢菌素类药物母核结构中含有“O=C-N-C=C”共轭体系,在260nm附近具有较强的吸收,特征性强。
青霉素类药物和头孢菌素类药物结构中均含有一个羧基,属于有机酸,其pKa一般为25~28,表现出较强的酸性,同时母环上具有一个可质子化的叔胺位点,所以分子总体上表现出一些两性化合物的特征。β-内酰胺环是药物结构中性质最不稳定的部分,与碱、酸、重金属(氧化剂)和酶作用时,易发生水解反应和分子重排,导致药物失效。目前,关于青霉素G降解反应的研究和报道较多,青霉素G在干燥状态下可以保持稳定,在水溶液中则容易代谢,遇酸可生成青霉二酸、青霉烯酸等β-内酰胺类药物残留物质,遇碱、醇或酶可生成青霉噻唑酸和青霉烯酸等物质。其中,青霉噻唑酸可聚合为青霉噻唑酸聚合物,可与多肽或蛋白质结合形成一种速发型致敏原,是青霉素G造成人体过敏反应的主要原因。
3 作用机制
β-内酰胺类药物的作用机制大多相似,通过抑制细胞壁黏肽合成酶的生成,干扰细胞壁肽聚糖的合成,使菌体细胞壁破损、细菌膨胀裂解死亡。β-内酰胺类药物可以通过抑制黏肽转肽酶(peptidoglycantranspeptidase)而抑制细菌细胞壁的合成。黏肽是细菌细胞壁的主要成分,是一些具有网状结构的含糖多肽,是由N-乙酰葡糖胺和N-乙酰壁氨酸交替组成的线状聚糖链短肽,这些高聚物需要在黏肽转肽酶的催化下进行转肽反应,使线状高聚物转化成交联结构,完成细胞壁的合成。β-内酰胺类药物的作用在于抑制黏肽转肽酶的活性。它由于结构与黏肽-D-丙氨酰D-丙氨酸的末端结构类似,构象也相似,使酶识别错误。青霉素竞争性地与酶的活性中心共价结合,构成不可逆的抑制作用。由于缺乏酶的催化,短肽不能转变成链状结构而无法合成细胞壁。无细胞壁,细胞不能定型和承受细胞内的高渗透压,引起溶酶,细菌死亡。这种作用特点有很大的优越性,因为人体细胞没有细胞壁,药物对人体细胞不起作用,具有很大的选择性,因此β-内酰胺类药物是毒性很小的抗生素。
细胞壁黏肽合成酶是一种青霉素结合蛋白(penicillinbindingproteins,PBPs),近年来研究者已证实细菌细胞膜上特殊蛋白PBPs是β-内酰胺类药物的作用靶位,不同细菌细胞膜上的PBPs数目、相对分子质量、对药物的敏感性存在差异,此外,有报道称此类药物还可以通过触发细菌自溶酶的活性而对细菌产生致死效应。
青霉素类和头孢菌素类包含药物种类多,抗菌谱广,在兽医临床上广泛用于由葡萄球菌、链球菌、肺炎球菌、大肠杆菌、沙门氏菌、嗜血杆菌等细菌引起的各类动物感染性疾病。
4 药动学研究
4.1 药物的吸收与分布
β-内酰胺类药物化学性质不稳定,易被胃酸和β-内酰胺酶破坏,除青霉素V、阿莫西林等耐酸性强的小部分药物可口服以外,多数β-内酰胺类药物通过肌内注射、皮下注射或静脉注射等途径给药。通常认为大多数β-内酰胺类药物的吸收位点在肠胃,但不同药物在体内的吸收机制存在明显的差异,Bretschneider等认为吸收机制的差异可能与药物本身的亲脂性和肠道转运蛋白的差异有关,他对23种β-内酰胺类药物在Caco-2细胞单层模型中的跨膜转运过程进行研究,发现寡肽转运蛋白PepT1(peptidetransporter1)能很好地转运头孢羟氨苄、头孢氨苄、头孢拉定、头孢克肟、氨苄西林等药物,对头孢匹林等药物却完全没有亲和作用。另外,肠道的pH差异会对药物的吸收产生影响,通常认为β-内酰胺类药物在哺乳动物肠道内的最佳pH吸收环境是61~68。
β-内酰胺类药物在体内分布广泛,以肝、肾、肺浓度最高,皮脂和肌肉次之,在脑脊液和乳汁中也有一定分布。组织炎症和给药方式的差异可导致体内药物的不正常分布,例如在奶牛乳腺炎的治疗过程中,乳室内乳汁的pH升高,血浆-乳汁屏障受到破坏,β-内酰胺类药物容易发生电离进入乳室,而乳房灌注是将治疗药物直接注入感染区的乳池内,这些特点导致治疗药物被乳腺大量吸收,并随泌乳量的增加而吸收增多,有报道称青霉素G在通过乳房灌注治疗乳腺炎时,在给药24h内乳汁中的药物含量可达注射量的42.6%。
4.2 药物的转化与排泄
β-内酰胺类药物在动物体内的半衰期较短,哺乳动物种属间的差异较小。阿莫西林在奶牛体内的消除半衰期为1.5h,在犬、猫体内为0.75~1.5h;氨苄西林在犬、猫体内的消除半衰期为0.75~1.3h,在猪体内为1.0h;青霉素G肌内注射给药在奶牛、马、犊牛、猪、兔体内的半衰期分别是1.02h、2.6h、1.63h、2.56h及0.52h,静脉注射给药在牛、马、骆驼、猪、羊、犬和火鸡体内的半衰期分别是1.2h、0.9h、0.8h、0.7h、0.7h、0.5h和0.5h。杨大伟等对猪体内头孢喹肟的药动学过程进行研究,肌内注射给药后吸收迅速,0.28~0.52h达到血药浓度最高峰,消除半衰期为1.79~2.77h,将结果与奶牛体内的药动学研究结果进行对比,头孢喹肟注射给药在奶牛体内的消除半衰期为0.3h,两者体内药动学排泄过程差异不明显。
β-内酰胺类药物进入血液循环后在体内不易被破坏,主要以原型从尿中排出,梁蓓蓓等综述了21种常用β-内酰胺类药物的排泄途径,苯唑西林、头孢氨苄等多数药物主要以原型经肾排出,肾功能减退时消除半衰期相应延长,哌拉西林、头孢哌酮等药物除经肾脏排泄外,小部分以原型经肝胆系统排泄,并可经胆汁排入肠道后重新吸收入血,形成肝肠循环。另外,给药方式和给药部位的不同会对药物的排泄途径产生影响,萘夫西林在治疗奶牛乳腺炎时,口服给药主要通过肾脏和胆汁排泄,但乳房灌注给药则大部分药量随乳汁排出。美国FDA的调查表明,不注意安全用药时间是造成牛奶中兽药残留的主要原因,奶中的兽药残留61%是由奶牛泌乳期的药物治疗造成的,31%是来自奶牛干奶期的药物治疗。不同的给药途径可造成牛奶中药物残留时间的不同。青霉素G治疗奶牛的乳腺炎时,在给药剂量和给药时间相同的情况下,肌内注射给药的奶牛在停药120h内的乳汁中可测到青霉素G的残留,而通过乳房灌注给药的奶牛,青霉素G通过泌乳排出的时间为144h。另外,不同的药物在奶牛乳腺组织中的残留时间存在差异。在采用相同方式给药的情况下,头孢氨苄随乳汁排出的时间为52h,头孢喹肟随乳汁排出的时间为84h,邻氯青霉素随乳汁排出的时间为96h。
5 毒理学研究
β-内酰胺类药物本身的毒性一般都很低,但与蛋白质产生复合物可以成为非常强烈的致敏源,从而导致严重的变态反应———过敏反应。
青霉素类药物在体内残留主要不良反应是过敏反应率高,居各类药物之首。据WHO统计,青霉素类药物过敏反应发生率为07%~10%。青霉素过敏反应包括速发型过敏反应和迟发型过敏反应,前者临床表现有过敏性休克、*麻疹荨**、血管神经性水肿等,属Ⅰ型介导的超敏反应;后者临床表现为斑丘疹、接触性皮炎、血清病等,T淋巴细胞可能参与这类反应。其中以过敏性休克最为严重,可在短时间内致死。
Dewndycetal认为,过敏反应的罪魁祸首是在动物体内残留的药物预先形成的致敏原,如青霉素-蛋白质结合物。根据现代免疫学理论,作为过敏原必须有特定抗原决定簇以及多价等必要条件,目前临床上应用的青霉素类药物相对分子质量均小于1000,因此其本身无免疫原性,但通过与蛋白质、多肽、多糖等大分子载体结合形成完全抗原或自身聚合成多价半抗原,成为诱发过敏反应的主要原因之一。此外,Brander研究发现,青霉素可直接与T淋巴细胞表面的组织相容性复合物(MHC)-肽复合物分子结合,刺激T淋巴细胞增殖而诱发进一步的反应,不需要抗原递呈细胞的递呈C。张建民等对8860份有过敏史的住院案例的用药物情况进行调查,结果发现β-内酰胺类药物过敏率所占比例最大,其中青霉素类药物过敏反应率最高,占整体比例的37.8%,头孢菌素类药物的过敏反应发生率为11.3%。就单种药物来说,青霉素G的过敏反应发生率最高,占青霉素类药物过敏率的89.4%。
6 国内外限量要求
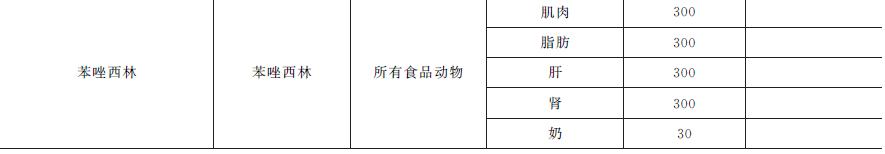
为了保护消费者的健康安全,我国、欧盟、美国等都已制定β-内酰胺类药物在各动物组织中的MRL,表5-29为我国、欧盟规定的动物组织中β-内酰胺类药物的MRL。


7 检测方法
7.1 样品前处理
样品的前处理主要包括提取、净化、浓缩(富集)、衍生化等过程,几乎占用了检测分析全过程近70%的工作量。与其他药物相比,β-内酰胺类药物化学性质不稳定,容易受试剂、温度等前处理因素的影响,且样品中药物残留的浓度较低,所以样品前处理技术对β-内酰胺类药物的分析检测具有重要意义。
7.1.1 样品的提取
7.1.1.1 提取液
提取液的作用是将目标物从样品中提取出来,在保证目标物质提取效率的前提下,需要考虑到基质的干扰。β-内酰胺类药物多以药物原型残留于动物组织中,母体结构中含有羧基和一个可质子化的叔胺位点,显示出两性化合物的一些特征,为中等极性或极性化合物,易溶于极性有机溶剂和酸性或碱性水溶液。故可以根据药物的性质选取合适的提取液,目前常用于β-内酰胺类药物残留分析的提取溶剂有*腈乙**、酸化*腈乙**、酸化甲醇、*腈乙**-二氯甲烷、磷酸盐缓冲液和钨酸钠等。生物样品中β-内酰胺类药物残留常用的提取溶剂可分为无机试剂提取液和有机试剂提取液。
7.1.1.1.1无机试剂提取液
β-内酰胺类药物易溶于酸性或碱性水溶液,在残留分析中选用的无机试剂多为稀酸、缓冲溶液等。刘媛等选用磷酸盐缓冲液提取鸡肉、猪肉、猪皮、猪脂肪等动物组织中的阿莫西林,经HPLC检测,药物的回收率为70.9%~86.8%。Yuko等选用钨酸钠作为萃取溶剂,从牛肾脏和肝脏中提取7种青霉素类药物,提取后用LC-MS/MS检测,药物的回收率均高于66%。黄百芬等用20%的乙酸铅溶液对牛奶中12种青霉素类药物和7种头孢菌素类药物进行提取,样品经蛋白质沉淀后用HLB固相萃取柱净化,用UPLC-MS/MS检测,19种药物的定量限可达0.034μg/L,回收率为73.4%~112.7%。
7.1.1.1.2 有机试剂提取液
β-内酰胺类药物残留分析中广泛采用甲醇、*腈乙**、*酮丙**、二氯甲烷、三氯甲烷等有机溶剂作为提取剂,这些溶剂有良好的溶剂化作用和渗透能力,提取速度快,兼具脱蛋白质和脱脂等优点,是目前选用较多的提取试剂。甲醇容易使β-内酰胺类药物发生醇化,影响药物的回收,且甲醇提取液中的杂质较高,目前使用较少。酸性有机溶液有利于提高一些β-内酰胺类药物的回收率,但由于多数药物的β-内酰胺环不稳定,在酸性溶液中容易发生降解,故酸性有机溶液仅可用于一些稳定*药性**物的提取。为增加提取剂的选择性,必要时可采用混合溶剂提取,如三氯乙酸-甲醇、二氯甲烷-*腈乙**、*腈乙**-水等。沈映冰等采用含25%的高氯酸的*腈乙**溶液作为萃取剂从人血浆中提取头孢吡肟,经HPCE检测,回收率为97.6%~104.5%。DeAlwis等选用甲醇-三氯乙酸对酒糟中青霉素、氨苄西林及其他类型抗生素进行提取,药物回收率为50%~100%。Mieke等以*腈乙**和二氯甲烷为提取剂提取生物组织中氨苄西林、阿莫西林、头孢唑林、哌拉西林、头孢喹肟、美罗培南等β-内酰胺类药物,增加了提取药物的种类,但回收率稍差(59.9%~71.5%)。Cmara对羊奶中的氨苄西林、青霉素G、青霉素V、头孢氨苄、双氯西林、氯唑西林、苯唑西林、头孢唑林、头孢哌酮等9种β-内酰胺类药物用*腈乙**进行提取,5mL羊奶加5mL*腈乙**,节约了提取试剂的用量,但提取剂的沉淀效果不佳,在用SPE柱净化前,需要用0.45μm的滤膜过滤。另外,EDTA、磷酸盐缓冲液等也可用于β-内酰胺类药物的提取,DeAlwis尝试用三氯乙酸-EDTA对青霉素G、氨苄西林2种药物进行提取,药物的回收率为50%~100.0%。Santos等用20%三氯乙酸溶液对牛奶中阿莫西林等6种药物进行了提取,回收率均在72%以上。李牧等以*腈乙**为提取剂从血液和尿液中提取多种头孢菌素类药物残留,经HPLC检测,回收率均高于80%。
为了进一步提高对生物样品中β-内酰胺类药物残留的提取效率,不少科研工作者还对不同的物理或化学提取技术进行了选择,常用的提取技术有匀浆提取、振荡提取、超声波辅助提取等。前两者提取方法为常规技术,而超声辅助提取主要是利用超声波具有的机械效应、空化效应和热效应,通过增大介质分子的运动速度、穿透力以提取生物样品中的待测组分。操作时将适量生物样品和提取溶剂混合,借助超声波水浴作用一定时间,选择合适的超声强度和超声时间达到定量提取的目的,此过程是一个物理过程,在整个提取过程中不发生化学反应,不影响多数药物有效成分的生理活性,操作简单,一次可以同时提取多个样品。张尹等对牛奶中9种β-内酰胺类药物残留进行检测,选用*腈乙**和磷酸盐缓冲溶液为提取液,20kHz超声辅助提取5min,净化后用HPLC进行检测,所有药物的回收率均达到71.0%以上。
7.1.2 样品的净化
由于样品基质性质复杂,提取过程中会有一些与待测组分性质类似的共萃取物一起被提取出来,这些杂质常常干扰光谱检测、增加基线噪声、降低柱效、阻塞色谱管路、污染色谱柱和检测器等,因此在色谱等检测之前进行净化操作是必不可少的。净化处理方法主要包括液-液萃取(LLE)和固相萃取(SPE)两大类。
7.1.2.1 LLE
LLE是一种传统的净化方法,对试验条件要求不高,是净化β-内酰胺类药物残留的基本方法。该方法是利用不同物质在不同溶液中的溶解度不同,使得被分析物由其中一相转移到另一相,从而实现样品的净化。二氯甲烷、三氯甲烷常用作液-液分配的溶剂,有时还可加入氯化钠等以增强溶剂的离子强度,进一步提高β-内酰胺类药物残留在有机相中的转移效率。另外,从样品基质中提取后,通常会用正己烷、*醚乙**等非极性溶剂进行脱脂。Jank等建立了一种基于LLE和LC-MS/MS相结合的快速检测牛奶中β-内酰胺类药物残留的方法,用*腈乙**对牛奶中的药物进行提取,所有药物回收率均在60%以上,检测限符合欧盟规定标准。
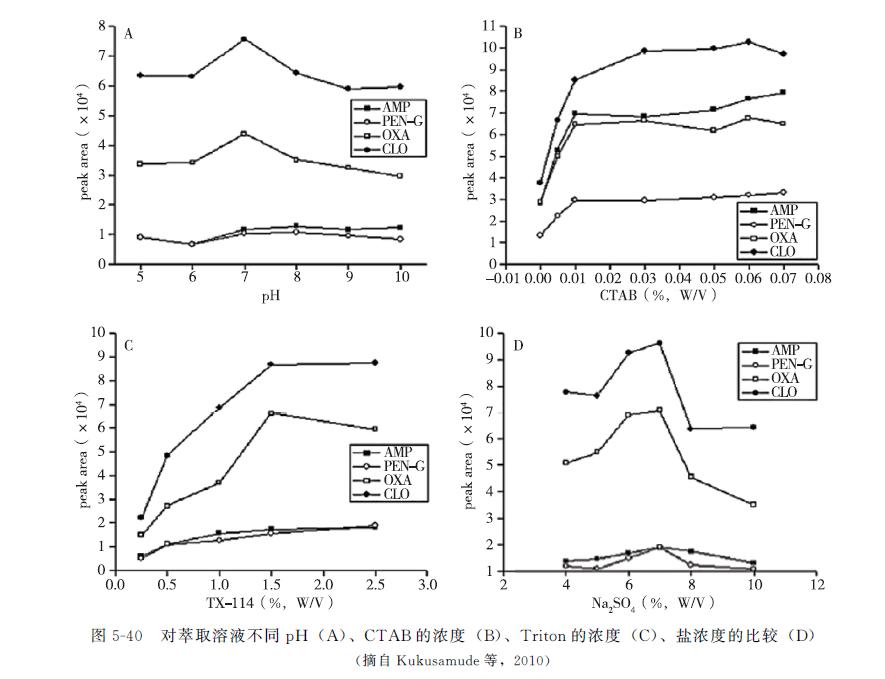
Kukusamude等还利用十六烷基三甲基溴化铵(CTAB)、TritonX-114等建立了混合胶束的浊点萃取法,对萃取溶液不同pH、CTAB的浓度、萃取时间、Triton的浓度、盐浓度等进行了详细考察(图5-40)。
LLE是一种经典的净化方法,对试验条件的要求不高,但需要大量的高纯度溶剂,且萃取时间长,回收率不理想。为了提高提取效率,在使用LLE的同时可使用辅助提取技术如加压液体萃取、超临界流体萃取等。
Kukusamude等利用四丁基溴化铵作为离子对试剂对牛肉和牛奶中青霉素G、氯唑西林、苯唑西林3种药物残留进行了提取,并系统分析了不同pH、不同四丁基溴化铵浓度、不同盐浓度等对离子对试剂提取效果的影响,液-液萃取后的上层溶液直接进行LC-PDA检测,方法的检测限可达1~2ng/mL。Kantiani等用“加压液体萃取(pressurisedliquidextraction,PLE)+固相萃取”的“提取+净化”的方式对动物饲料中6种β-内酰胺类药物残留进行了测定,系统地研究了溶液成分、温度、容器尺寸、萃取循环次数、溶液体积等影响加压溶剂萃取的因素;方法的回收率为71%~115%,RSD小于13%,并利用该方法对14个市场抽取的样品进行了检测。
7.1.2.2 SPE
SPE是在LLE基础上发展起来的新型净化技术,是目前样品前处理的主流净化技术,其原理是利用固体吸附剂将液体样品中的目标化合物吸附,使其与样品基体和干扰物分离,然后再用溶液洗脱或热解吸附,达到分离和富集目标化合物的目的,是目前应用较广的一种样品净化方式。SPE可净化小体积的样品,溶剂用量小、选择性高,根据不同的待测物选用不同的填料,根据保留机理可以分为正向固定相、反向固定相和离子交换固定相等。主要包括C18柱、混合型离子柱(OasisMAX、CleanertPAX)、强阳离子柱(ProElutSAX)、亲水亲酯柱(OasisHLB)等。
β-内酰胺类药物结构中含有羧基、氨基,通常具有极性,故该类药物可选用反相萃取柱,如C18柱和HLB柱等;β-内酰胺类药物属于有机酸,根据目标物质显酸性的化学性质,部分药物可以选用混合型阴离子柱。SPE柱的选择需要根据检测药物的种类和性质进行试验筛选。Macarov等对动物肌肉组织中的8种β-内酰胺类药物残留进行检测,对HLB柱、C18柱、MAX柱、ENV+柱的净化效果进行对比,试验结果显示,ENV+柱的净化效果最好,MAX柱的回收率最低,C18柱对阿莫西林、氨苄西林和青霉素G的保留最高,但邻氯青霉素的回收率明显低于其他萃取柱,HLB柱柱效明显优于MAX柱,但仍低于其他两种萃取柱;另外,该试验研究了pH对4种萃取柱保留能力的影响,发现pH为5~9时,SPE柱对β-内酰胺类药物保留较理想。Fernandez-Torres等比较了C18柱和Plexa固相萃取柱对包括β-内酰胺类药物在内的4类药物的净化效果,该方法详细地比较了不同pH、不同洗涤和洗脱溶液的净化效果,结果表明Plexa固相萃取柱较C18柱好。郭德华等建立了动物源性食品中76种兽药残留的SPE,样品采用*腈乙**和含镁离子的柠檬酸缓冲液进行提取,去除有机相后以缓冲液重溶,聚合物和阳离子交换SPE柱串联净化,用甲醇和甲醇-*水氨**(95∶5)分步洗脱,用LC-MS/MS进行测定,用基质曲线外标法定量,回收率为59.4%~115.3%,RSD为2.6%~27.3%,该方法成功用于对市场中样品的筛选。张琦等用阿莫西林、头孢氨苄、氨苄西林和青霉素V等药物的标准混合液对HLB柱、C18柱、MAX柱的净化效果进行对比,结果表明HLB柱对所测药物的保留能力最好,4种药物的回收率均高于70%。在多残留分析中,药物性质存在差异,除了选择保留机理合适的SPE柱外,为了使SPE柱的保留和净化能力最大化,还需要对SPE柱的净化条件进行试验筛选。
7.1.2.3 基质固相分散(MSPD)
MSPD是类似于SPE的一种净化技术。Barker等在1989年最早提出该技术,使样品与反向键合硅胶结合后均匀、研磨、装柱,再选用合适的淋洗液洗柱,将目标化合物洗脱下来。该方法净化效率高、耗时少、节约溶剂,但不易实现自动化。王炼等人建立了畜禽肉和牛奶中20种兽药残留的MSPD净化方法,将生物样品与C18填料混合均匀,填入SPE空管压实,置于SPE装置上,用甲醇减压洗脱,洗脱液用40℃氮气吹干,经*腈乙**-乙酸铵(2∶8,V/V)溶解,过滤膜进样,药物的检测限为0.05~3.05g/kg,回收率均达70%以上。
7.1.2.4 QuEChERS方法
QuEChERS方法是近年来国际上新发展起来的一种用于农产品快速检测的样品前处理技术。该方法具有回收率高、结果准确、样品处理量大等优点,从而减少了试剂的消耗和对试验人员与有毒溶剂的接触,可有效地将提取、分配、净化有机结合,进一步减少提取步骤,提高提取效率。QuEChERS方法通常主要以分散固相萃取体现,Pérez-Burgos等建立了检测牛肉中7种头孢类药物残留的QuEChERS方法,牛肉样品经15mL甲醇水溶液(8∶2,V/V)振荡提取、离心后,将10mL上清液加入150mgC18和900mg无水硫酸镁,振荡5min,离心取5mL上清液,用氮气吹干、复溶后进行LC-MS/MS检测;方法的定量限为4~50μg/kg,RSD小于15%。Karageorgou等利用超声辅助-MSPD的方法建立了检测牛奶中12种-内酰胺类药物残留的QuEChERS方法。
7.1.2.5 分子印迹技术
分子印迹技术使用分子印迹聚合物(MIP)作为固定相,对目标分子具有特定识别能力。王慧等对应用分子印迹技术合成了对青霉素有特异性吸附能力的印迹聚合物PenG-MIP,将MIP用于检测牛奶中的青霉素,实现分子印迹技术用于乳中青霉素残留的快速定量检测,检测限为5μg/L,结果准确度高,操作简便,且PenG-MIP颗粒可以反复使用,极大地降低了检测成本。
7.1.2.6 免疫亲和色谱(IAC)
IAC是以抗原抗体的特异性、可逆性免疫结合反应为原理的色谱技术。净化过程中使用连有抗体的惰性基质固定相,特异性好,选择性高,是生物样品有效的净化方式之一。Zhi等建立了自动流动电流免疫分析系统,定量测定了牛奶中头孢氨苄残留,检出限为1μg/L,定量限为3μg/L,均低于欧盟标准规定的牛奶中头孢氨苄的MRL。该方法对头孢氨苄具有很强的选择性,其他头孢菌素类和青霉素类药物对其检测干扰很小,适用于牛奶中头孢氨苄残留的定性和定量分析。IAC特异性好、选择性高,在药物分析中有广阔前景,但由于免疫方法自身的局限性,目前应用还不广泛。
7.2 检测方法
国内外对β-内酰胺类药物残留检测技术的文献报道很多。目前,用于β-内酰胺类药物残留检测的方法主要有高效液相色谱法(HPLC)、毛细管电泳(CE)、液相色谱-质谱联用(LC-MS)、气相色谱(GC)、免疫分析法、微生物法等。
7.2.1 GC
GC是以气体作为流动相的色谱过程,适用于气体、沸点低、易汽化的物质,而β-内酰胺类药物本身不易汽化,在前处理过程中需要进行衍生化操作。Meetschen等用GC测定了动物组织中7种β-内酰胺类药物残留,用重氮甲烷进行衍生化,形成易挥发的青霉素甲基酯类化合物,回收率为46.0%~73.0%。GC要求样品能够汽化,受到样品挥发性的约束,多数β-内酰胺类药物挥发性差且热不稳定,虽然可以采用一些预处理办法,但增加了操作上的难度,过程复杂,且改变了样品原来的形态,不易复原,因此在-内酰胺类药物残留分析方面,GC已基本上被LC所取代。
7.2.2 HPLC
HPLC是β-内酰胺类药物残留分析中应用最多的一种技术,常用的检测器包括紫外检测器(UVD)、荧光检测器(FLD)和二极管阵列检测器(DAD)等。
由于多数青霉素类药物没有专一的紫外发射基团,其吸收波长一般为200~235nm,而在这段波长范围内的选择性较差。由于生物样品中青霉素类药物的残留量较低,其背景干扰往往较严重,因此一般都是使用柱前或柱后衍生化技术,衍生化反应可以有效提高UVD的灵敏度。如使用咪唑或1,2,3-*唑三**催化作用下使青霉素形成青霉烷酸硫醇汞衍生物,其最大波长为325nm,在该检测波长下很少有共生组分干扰测定,而且该方法对β-内酰胺环的化合物有专一性,利用此原理,Bioson、Verdon等分别建立了检测青霉素类药物残留的检测方法。蔡玉娥等使用HPLC-UVD法检测生物样品中头孢羟氨苄、头孢克洛、头孢氨苄、头孢拉定、头孢噻吩5种头孢菌素类药物残留,以磷酸缓冲液-*腈乙**为流动相,在270nm处检测,检出限均低于9.7μg/kg,回收率为96.5%~105.0%。DAD属于UVD的一种,原理同UV,能进行全波长的扫描,可用于混合物中不同波长的物质的检测。Cmara等使用DAD建立了检测羊奶中阿莫西林、青霉素G、青霉素V、阿莫西林、双氯西林、氯唑西林、苯唑西林、头孢唑林、头孢哌酮9种β-内酰胺类药物残留的HPLC,检出限为3.4~8.6μg/kg,回收率为79.0%~96.0%。在药物多残留分析中,为了达到理想的检测效果,HPLC可以串联不同的检测器,Benito-Pena等建立了青霉素G、青霉素V、萘夫西林、苯唑西林、氯唑西林、双氯西林、阿莫西林、氨苄西林8种β-内酰胺类药物残留的HPLC-UVD/DAD检测法,选择220nm为检测波长,检出限为8.0~24.0μg/kg,平均回收率为82.0%~97.0%。
FLD与UVD相比具有更强的灵敏度和特异性,但要求药物具有荧光特质,对单种或少数药物的准确检测较UVD有一定优势。由于β-内酰胺类药物没有荧光发射基团,因此必须采用衍生化使它产生荧光发色基团。罗道栩等建立了牛奶中氨苄西林残留的HPLC-FLD检测法,用甲醛法对药物进行衍生化,激发波长和发射波长分别为346nm和420nm,检测限为1.0μg/kg,回收率为70.0%~110.0%。Terada等利用氨苄西林在甲醛和三氯乙酸溶液中能产生荧光衍生物的原理,用FLD测定了牛奶中氨苄西林的残留量。
7.2.3 LC-MS
LC-MS是一种以LC为分离手段、MS为检测器的现代分析技术。LC-MS实现了LC和MS优势的结合,将LC对复杂样品的高分离能力与MS高选择性、高灵敏度的优点结合起来,尤其是串联质谱(MS/MS)能够提供更详细的相对分子质量与结构信息,使得这项联用技术在药物分析、食品分析和环境分析等多个领域中得以广泛应用。
由于MS/MS的研究和发展,LC-MS/MS在β-内酰胺类药物多残留检测领域中获得较大发展。Ohmori等选用LC-MS/MS检测了血浆中8种β-内酰胺类药物残留,其检测限为0.01~0.5μg/mL,除多里培南、美罗培南的回收率为49.1%、62.3%外,其他药物的回收率均超过80.2%。Macarov等建立了牛、猪、鸡肉组织中阿莫西林、氨苄西林、双氯西林、青霉素G、青霉素V、苯唑西林、氯唑西林、萘夫西林8种青霉素类药物的LC-MS/MS检测法,用内标法定量,除阿莫西林回收率只有50.0%外,其他药物的回收率均超过70.0%,所有药物检测限均低于或等于欧盟规定的MRL。Becker等采用LC-MS/MS法测定了牛奶等组织中15种β-内酰胺类药物残留,阿莫西林、氨苄西林、头孢氨苄、头孢匹林、头孢唑啉等使用ESI+检测,头孢哌酮、青霉素G、青霉素V、苯唑西林、邻氯西林、双氯西林和萘夫西林使用ESI-检测,使用基质添加法校正基质效应,除阿莫西林的回收率只有57.0%外,其他目标分析物的回收率都大于81.0%,所有药物检测限均符合欧盟规定标准。Lina等建立了饲料中11种β-内酰胺类药物残留的LC-MS/MS法,以0.1%甲酸水溶液-0.1%甲酸甲醇作为流动相,在30min内将18种药物分离,平均回收率均为71.0%~115.0%,检测限为0.12~3.94μg/kg。
Carlier等用超高效液相色谱(UPLC)代替HPLC建立了血浆中7种β-内酰胺类药物残留的检测方法,方法选用BEHC18(1.7μm,100mm×2.1mm)色谱柱对检测物进行分离,含0.1%甲酸水和*腈乙**作为流动相,所有药物在5.5min内检测完毕,大大缩短了检测时间,所有药物的回收率均为86.8%~101.5%。Liu等建立了用UPLC-MS/MS检测牛奶中青霉素G、阿莫西林及多种代谢产物(苄青霉噻唑酸、苄青霉脱羧噻唑酸、苄青霉二酸、阿莫西林噻唑酸、阿莫西林二酮哌嗪)的方法,所有药物选用ESI+进行检测,8min内8种化合物成功得到分离,药物的定量限为2.5~5.0μg/kg,回收率为85.0%~108.0%,RSD均小于13%。Tang等应用UPLC-MS/MS同时测定牛奶中23种兽药残留,包括7种β-内酰胺类药物、12种大环内酯类药物和4种其他兽药,所有药物的检出限均小于5μg/mL,加标回收率分别为51.5%~100.6%、51.8%~139.0%和82.4%~102.5%,RSD小于15.0%。UPLC的使用极大地提高了色谱的分离能力,加快了药物的分析速度,结合MS/MS检测器能够提供检测物详细的分子质量与结构信息,使得UPLC-MS/MS在化学品的定性和定量检测中具有独特的优势,近年来在药物分析、食品检测领域的应用中发展迅速。
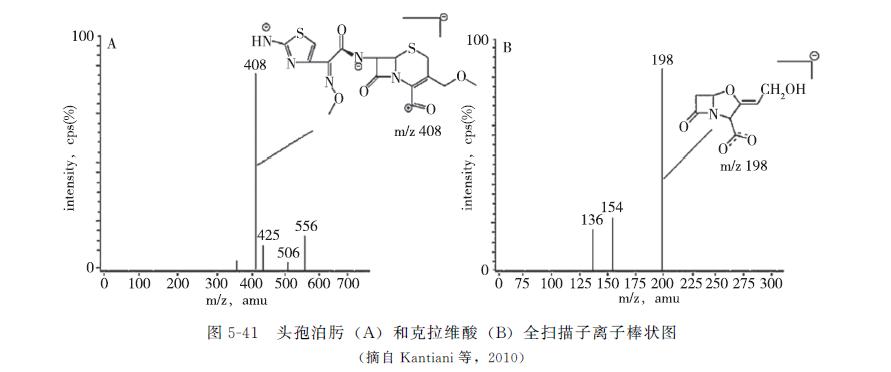
Kantiani等用液相色谱-线性离子肼-串联质谱法测定了动物饲料中头孢唑林、头孢哌酮、氯唑西林、双氯西林、青霉素G、青霉素V等药物残留。Dubala等建立了同时检测人血浆中头孢泊肟和克拉维酸残留的LC-MS/MS方法,以甲醇-*腈乙**-2mmol/L乙酸铵溶液(25∶25∶50,V/V,pH3.5)为流动相,用负离子检测,分别选取m/z408[M-(CH3)--2H)]-和m/z198[M-H]-为母离子,进行SIM检测,2种药物的化学结构及全扫描图见图5-41,Kantiani等还对方法的线性、精密度、准确度、离子抑制、基质效应、灵敏度及稳定性等进行了考察。
7.2.4 微生物法
微生物法又称为微生物抑制试验,是基于药物对微生物生理机能和代谢的抑制作用,定性或定量地测定样品中药物残留量的检测方法。常用的微生物法有纸片法(paperdiskmethod,PD)、氯化三苯基四氮唑(TTC)法、杯碟法(cylinderplatemethod,CP)、浑浊度法、戴尔沃检测法(Delvotest-SP)、微生物受阻法等。
PD将阳性对照纸片和吸满受检乳样的纸片放入接种菌株的琼脂平皿上,在适宜条件下进行培养,观察抑菌圈从而判断结果。TTC法为定性检测牛奶药物残留的方法,最早由Neel和Calbert等在1955年提出,乳中加入嗜热链球菌作为菌种进行培养,根据TTC指示剂的颜色变化判断结果。王大菊等用藤黄八叠球菌为指示剂,用CP检测猪、鸡组织中氨苄西林残留,其最低检测限可达0.00025μg/mL,低于Vilim用嗜热脂肪芽孢杆菌测定的0.0009μg/mL,标准曲线的工作范围为0.00125~0.02μg/mL,变异系数为(2.91±0.2)%,不同浓度氨苄西林的回收率为83%~107%。李延华等用国标TTC法和AOAC纸片法对乳中β-内酰胺类药物残留的检测结果进行对比研究,AOAC纸片法可以成功检测出青霉素G、氨苄西林、羟氨苄西林、苯唑西林、头孢氨苄、头孢吡啉6种β-内酰胺类药物残留的MRL浓度,而TTC法不能成功地对MRL浓度的上述药物进行检测,仅能用于定性检测。微生物法由于易受组织中其他抗生素的影响,特异性低,灵敏度不高,但操作简便、样品用量少、预处理简单,适合于大量样品的筛选,目前常被牧场、乳品企业等用于对大批量奶样中抗生素进行筛选检测。
7.2.5 CE
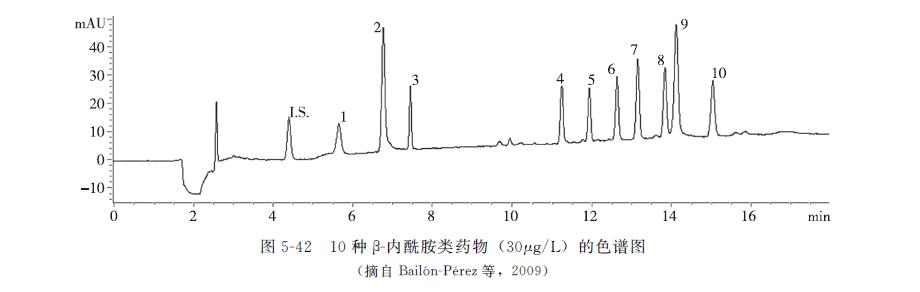
CE或称为高效毛细管电泳(HPCE),是一类以高压电场为驱动力、毛细管为分离通道,根据样品组分之间电泳强度和分配行为的差异而实现分离的一种液相分离技术。与HPLC相比,HPCE有柱效高、选择性好、进样体积小、样品分析范围宽的特点,是近年来分析化学中较活跃的技术之一。由于β-内酰胺类药物具有有机酸碱基团,毛细管区带电泳的方法使用也较为普遍。Bailón-Pérez等用HPCE-UV/DAD法检测环境污水及饲料中克拉维酸、阿莫西林、氨苄西林、青霉素G、青霉素V、萘夫西林、苯唑西林、氯唑西林、双氯西林、哌拉西林10种β-内酰胺类药物残留,水样和饲料中的检测限分别是0.04~0.06μg/L和0.80~1.4μg/L,回收率均为82.9%~98.2%,RSD小于9.0%,10种药物的色谱图如图5-42所示。Sérgio等建立了同时检测牛奶中氨苄西林、阿莫西林、青霉素、氯唑西林、四环素、氯霉素6种药物残留的CE,以pH8.0的KH2PO4、Na2B4O7溶液为流动相,在18kV的电压条件下,在210nm处用UVD检测;以2.5μg/mL2个和5.0μg/mL添加浓度进行添加回收试验,方法的回收率在72%以上,RSD小于5%。电渗流不稳定,导致HPCE的结果重现性较差,且HPCE的载样量少,灵敏度不及HPLC,在残留分析的应用中受到限制。Bailon等用HPCE-UV/DAD法检测水中7种β-内酰胺类药物残留,选用离线SPE法净化和浓缩样品,检测限为0.08~0.8μg/L,回收率为94%~99%,RSD小于10%。
7.2.6 免疫分析法
该法的优点是操作简单、检测快速,一些生物样品如尿液等可以直接测定,在β-内酰胺类药物残留的检测中主要用于筛选分析。免疫分析法主要包括ELISA、放射免疫法(RIA)等。ELISA是当前应用最广的免疫分析法,并已有多种已商品化的ELISA酶标试剂盒,可用于多种兽药残留的检测,如美国柏尔(Bioo)公司生产的总抗生素(牛奶)试剂盒可用于检测牛奶中青霉素G、氨苄西林、阿莫西林、苯唑西林等β-内酰胺类药物残留,检测限为4.0μg/kg;北京望尔生物技术有限公司生产的青霉素检测试剂盒可用于检测牛奶、蜂蜜、组织中的青霉素G,检测限为0.2μg/kg。Lamar等利用重组蛋白制备的青霉素结合蛋白(PBP)建立了检测牛奶、牛肉、猪肉、蜂蜜、鸡蛋中β-内酰胺类药物残留的ELISA。
青霉素类药物分子中由于具有多个抗原决定簇,可在动物体内免疫产生多种类型抗体,因而可以根据待测物结构和分析目的来指导人工抗原的合成。为了获得主要识别某种青霉素药物的抗体,抗原决定簇需以侧链抗原决定簇为主,因而在抗原合成时要突出侧链结构,Edwards等成功将蛋白载体交联于青霉素分子噻唑环的羧基部位上,获得了特异性抗体。同样为了获得母核特异性抗体,能识别整个青霉素类药物,抗原合成时则要突出母核结构(6-APA)。Shirazid等采用戊二醛法、青霉素化反应等不同的免疫抗原合成法,用小鼠进行免疫反应,获得了对多种青霉素有交叉反应的单克隆抗体,采用间接竞争ELISA可同时对牛奶和畜产品中氨苄西林、青霉素G、羟氨青霉素、苯唑西林、双氯青霉素等β-内酰胺类药物残留进行检测,检测限度为2.5~5ng/mL,检测灵敏度都在欧盟MRL内。DeLewu等直接利用6-APA制备抗青霉素卵黄抗体;Diertihc等用戊二醛法将氨苄青霉素侧链氨基与蛋白质连接制备核特异性抗体;Cliuqet等利用青霉素生理学反应合成青霉噻唑蛋白,制备获得核特异性抗体。这些获得的母核特异性抗体与整个青霉素类药物有很大的交叉反应性,可以用来做青霉素类药物残留分析检测。
张佳等建立了动物组织中β-内酰胺类药物残留的放射性受体快速筛选分析法,成功地用于检测猪肉、牛肉、鸡肉、鱼肉、虾肉中的青霉素G、阿莫西林、氨苄西林、双氯西林、氯唑西林、头孢噻呋等药物残留的筛选,在90min内即可完成一批样品的测定,大大加快了测定速度,并节约了测定成本。魏东等采用间接竞争ELISA对牛奶中阿莫西林残留进行检测,以人工合成的AMX-OVA为检测抗原、AMX标准品为竞争半抗原,该方法的最低检测限为3.926ng/mL,在0.5~2000ng/mL范围内样品添加平均回收率为91.45%。