人教化学2019高考一轮基础练习2
一、选择题
1、化学与生活、生产、环境密切相关,下列有关说法不正确的是( B )
A.为了防止肿痛,用小苏打溶液清洗蚂蚁叮咬处
B.二氧化硫有毒,严禁在任何食品和饮料中添加
C.我国最早使用的青铜器主要成分是铜、锡等金属
D.加油站墙壁上粘贴的危险化学品标志是

解析 为了防止某些食品氧化,常添加SO2抗氧化和防腐,但需严格遵照国家限量标准,B项错误。
2、
2.下列叙述正确的是( D )
A.氢氧化钠的摩尔质量是40 g
B.1 mol NaOH的质量是40 g/mol
C.1 g H2和1 g N2所含分子数相等
D.阿伏加德罗常数个钠原子的质量是23 g
3、利用焰色反应,人们在烟花中有意识地加入特定金属元素,使焰火更加绚丽多彩。下列说法中正确的是( B )
A.非金属单质燃烧时火焰均为无色
B.NaCl与Na2CO3灼烧时火焰颜色相同
C.焰色反应均应透过蓝色钴玻璃观察
D.只有金属单质灼烧时火焰才有颜色
解析 某些非金属单质燃烧时火焰有颜色,A、D项错误;焰色反应为金属元素的性质,与元素的存在形式(化合态或游离态)无关,同种金属元素的焰色反应相同,B项正确;观察钾元素的焰色反应时应透过蓝色钴玻璃,C项错误。
4、二氧化硅(SiO2)又称硅石,是制备硅及其化合物的重要原料(见下图)。下列说法正确的是( C )
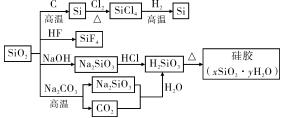
A.SiO2既能与HF反应,又能与NaOH反应,属于两性氧化物
B.SiO2和Si都是光导纤维材料
C.在硅胶中加入CoCl2可显示硅胶吸水是否失效
D.图中所示转化反应都是非氧化还原反应
解析 两性氧化物的定义为与酸和碱反应均生成盐和水的氧化物,SiO2与HF反应得到的SiF4不属于盐类,A项错误;SiO2是光导纤维材料,Si为半导体材料,B项错误;CoCl2在吸水和失水状态下显示不同的颜色,C项正确;制取Si的过程中涉及了氧化还原反应,D项错误。
5、下列关于指定粒子构成的几种描述不正确的是 ( C )
A.37Cl与39K具有相同的中子数
B.第114号元素的一种核素 eq \o\al(298,114)X与 82Pb具有相同的最外层电子数
C.H3O+与OH-具有相同的质子数和电子数
D.Oeq \o\al(2-,2)和S2-具有相同的质子数和电子数
6、下列关于热化学反应的描述正确的是( D )
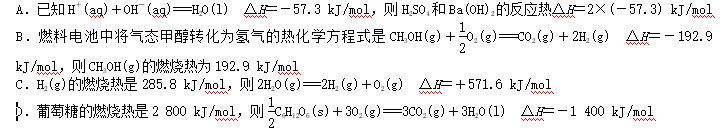
解析 A项,H2SO4和Ba(OH)2反应除了生成水还生成BaSO4沉淀,所以该反应的热效应不是中和热,错误;B项,该反应生成的氢气不是稳定产物,所以该热效应不是燃烧热,错误;C项,表示H2(g)的燃烧热时生成的是液态水,错误;D项,1 mol葡萄糖燃烧放热2 800 kJ,所以当热化学方程式的化学计量数变为原来的1/2时,热效应减半,正确。
7、对A(g)+3B(g)===2C(g)+2D(g)来说,下列四种不同情况下的反应速率最快的是( A )
A.v(A)=0.005 mol/(L·s)B.v(B)=0.6 mol/(L·min)
C.v(C)=0.5 mol/(L·min)D.v(D)=0.45 mol/(L·min)
解析 A项中v(A)=0.005 mol/(L·s)的单位转化为mol/(L·min),得到v(A)=0.3 mol/(L·min),再将其他选项中用各物质表示的反应速率全部转化为用A表示,B项转化为v(A)=0.2 mol/(L·min),C项转化为v(A)=0.25 mol/(L·min),D项转化为v(A)=0.225 mol/(L·min),故A项表示的反应速率最快,正确。
下表中物质的分类组合完全正确的是( A )
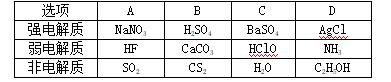
解析 CaCO3虽难溶,但溶于水的部分完全电离,是强电解质;H2O是弱电解质;NH3是非电解质。
9、下列关于化石燃料的说法正确的是( C )
A.石油裂化主要得到乙烯
B.石油分馏是化学变化,可得到汽油、煤油
C.煤干馏主要得到焦炭、煤焦油、粗*水氨**和焦炉气
D.煤制煤气是物理变化,是高效、清洁地利用煤的重要途径
10、在进行化学实验时必须注意安全,下列说法不正确的是( D )
A.如果苯酚浓溶液沾在皮肤上应立即用酒精清洗
B.不慎将酸液溅到眼中,应立即用水冲洗,边洗边眨眼睛
C.不慎将浓碱液沾到皮肤上,应立即用抹布拭去,再用大量水冲洗,然后涂上稀硼酸溶液
D.如果酸流到实验台上,立即用适量的氢氧化钠溶液中和,然后用水冲洗,再用抹布擦干
11、下列物质的分类中,所属关系不符合"X包含Y、Y包含Z"的有 ( D )
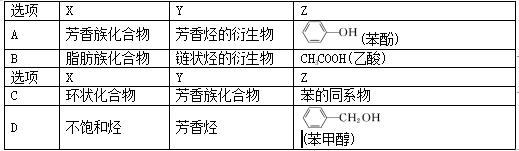
二、非选择题
(2018·甘肃兰州联考)煤的气化和液化是现代能源工业中重点考虑的能源综合利用方案。最常见的气化方法为用煤生产水煤气,而当前比较流行的液化方法为用煤生产CH3OH。
(1)如图甲是反应CO(g)+2H2(g)CH3OH(g)在不同温度下CO的转化率随时间变化的曲线。
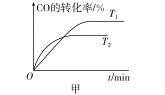
①T1和T2温度下的平衡常数大小关系是K1__>__K2(填">""<"或"=")。
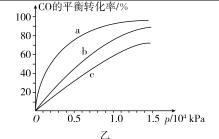
②由CO合成甲醇时,CO在250 ℃、300 ℃、350 ℃下达到平衡时转化率与压强的关系曲线如图乙所示,则曲线c所表示的温度为__350__℃。实际生产条件控制在250 ℃、1.3×104 kPa左右,选择此压强的理由是__250 ℃时,1.3×104 kPa下CO的转化率已经很高,如果增大压强,CO的转化率提高不多,而生产成本增加很多,得不偿失__。
③以下有关该反应的说法正确的是__AD__(填字母)。
A.恒温、恒容条件下,若容器内的压强不发生变化,则可逆反应达到平衡
B.一定条件下,H2的消耗速率是CO的消耗速率的2倍时,可逆反应达到平衡
C.使用合适的催化剂能缩短达到平衡的时间并提高CH3OH的产率
D.某温度下,将2 mol CO和6 mol H2充入2 L密闭容器中,充分反应,达到平衡后,测得c(CO)=0.2 mol·L-1,则CO的转化率为80%
(2)一定温度下,向2 L固定体积的密闭容器中加入1 mol CH3OH(g),发生反应:CH3OH(g)CO(g)+2H2(g)。H2的物质的量随时间变化的曲线如图丙所示。

①0~2 min内的平均反应速率v(CH3OH)=__0.125 mol·L-1·min-1__。
该温度下,反应CO(g)+2H2(g)CH3OH(g)的平衡常数K=__4__。
②相同温度下,若开始时加入CH3OH(g)的物质的量是原来的2倍,则__D__(填字母)是原来的2倍。
A.平衡常数
B.CH3OH的平衡浓度
C.达到平衡的时间
D.平衡时气体的密度
