VOL 3032

文丨赵文成
大米和小米东莞东城小镇中级康复师
教育学硕士(儿童心理发展方向)
前段时间,德国癌症研究中心Weigel等人在《自然》(Nature)发表了一篇名为“人类神经元和小鼠中的MYT1L单倍体功能不全导致自闭症相关表型,可以通过遗传和药物干预逆转”的研究论文。
研究指出:MYT1L基因突变会影响神经元细胞的发育和功能,并会在人类和小鼠模型中引起ASD相关表型,接受拉莫三嗪(lamotrigine,LTG)治疗的自闭症小鼠,并未表现出一些相关行为,这说明该药物可能有助于治疗人类自闭症。
自闭症谱系障碍(ASD)是一种常见的神经发育障碍,其特征之一是行为变化,包括社会模式的改变。ASD通常还伴随一些其他疾病,包括癫痫、智力障碍和多动症。
影响神经元通讯的基因突变,会增加ASD的风险,但也提供了可能的治疗靶点。
然而,ASD的遗传异质性是巨大的,目前已经发现了 91 种与ASD相关的染色质或基因调节因子。
1
什么是MYT1L
生物体的行为依赖于大脑复杂而多样的神经元网络。
转录因子决定神经元能否正常发挥作用,特别是神经元连接的特性,如树突形态、轴突靶向或突触特异性,最终启动神经元以整合到新兴电路中。
MYT1L就是一种转录因子,发现于 2 号染色体的短臂上,在遗传调控中起作用,它决定哪些基因在细胞中活跃,哪些不活跃。体内几乎所有的神经细胞,在整个生命周期都会产生MYT1L。MYT1L破坏通常与神经精神类疾病有关。
因此,MYT1L作为“神经元身份守护者(“guardian of neuronal identity”),可以通过抑制神经发育的负调节因子(如Notch和Wnt)来保护神经元细胞,其突变或缺失会严重影响神经元细胞的发育,损害大脑神经功能。
通俗的说,MYT1L就像是个大哥,管着哪些基因表达,哪些不表达。一旦大哥不在了,那些被管制的基因开始肆意表达,就会造成失调。
据报道,MYT1L在被诊断为智力障碍、精神分裂症、癫痫和ASD的患者中均发现突变,这表明由其介导的基因调节,可能对预防包括ASD在内的神经发育障碍很重要。
圣路易斯大学的Mansfield,华盛顿大学医学院精神病学和儿科系Constantino与Baldridge的联合报告中发现51例MYT1L基因突变的病例中,有50例被诊断为ASD、智力障碍或两者兼得。
除了行为特征外,一些有MYT1L突变的患者还表现出发育迟缓、肥胖、癫痫发作和大脑畸形。
2
研究结果
为了研究MYT1L在发育过程中的作用,并探索其与神经发育障碍的关系,研究人员使用了基因工程小鼠和人工诱导的神经元。
研究把小鼠分为了2个组:
实验组:MYT1L基因突变小鼠
对照组:MYT1L正常的小鼠
实验组和对照组小鼠,被安置在一个模拟日常环境的温控装置中,测试行为表现。结果发现:
神经发育:
1. MYT1L基因突变的小鼠大脑皮层变薄,脑重量下降,这种大脑结构异常,可能解释一些患者的大脑畸形。
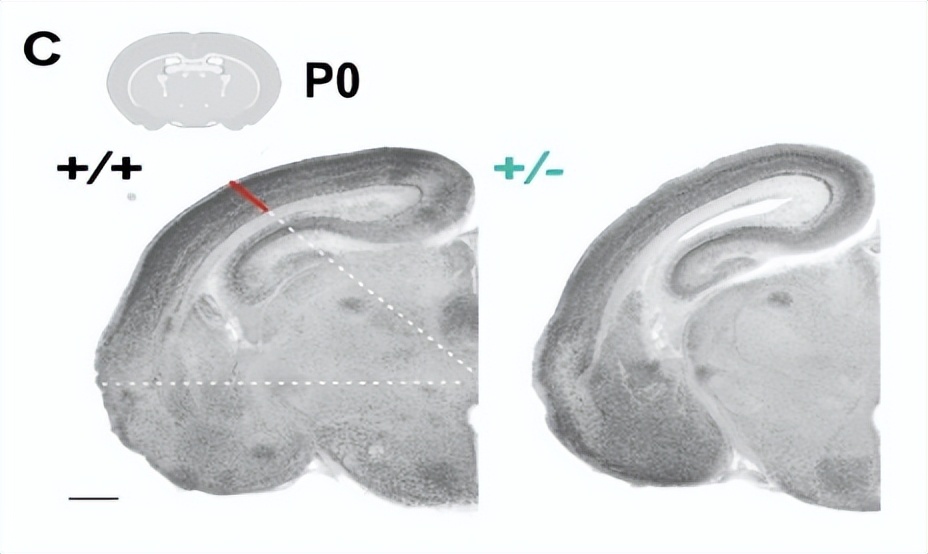
蓝色代表基因突变小鼠的皮质切面图
2. 突变小鼠还会出现神经发育迟缓和基因表达失调。而且这些失调的基因与癫痫、精神分裂症和ASD相关的基因在总体上富集。
行为表现:
在外显行为上,与对照组相比,MYT1L基因突变小鼠表现出多动和雄鼠特定社会缺陷。
具体体现在:
(1)小鼠叫声变多;
(2)成年小鼠在家笼中的运动增加;
(3)幼鼠在开放场地和高加迷宫试验中移动增加,呆在某一固定区域的时间明显延长,有时会突然张开前肢。
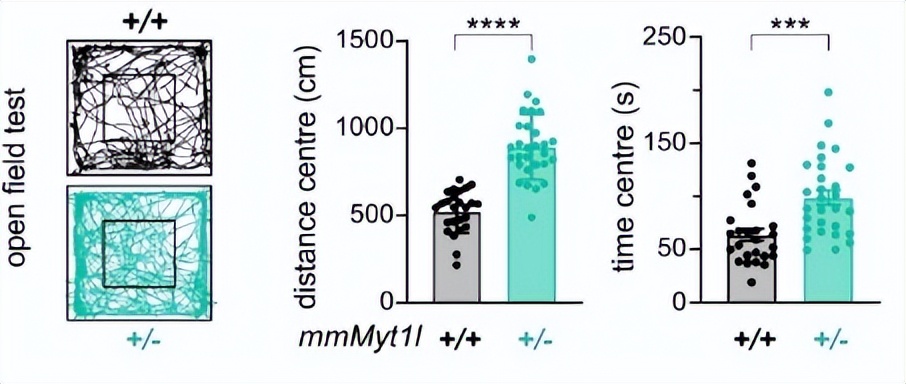
在开放区域的活动密度、偏离区域中心的距离、待在某一固定区域的时长
黑色正常小鼠,蓝色基因突变小鼠
社交实验:
(1)所有小鼠都表现出预期偏好,与空房间相比,更喜欢与同窝小鼠一起探索环境。也就是说,相对于一个空房间,小鼠更愿意走进有同窝小鼠的那个房间。
(2)正常小鼠和突变雌鼠都愿意和新加入的小鼠待在一个房间里,但突变雄鼠不愿意和新小鼠待在一起。
在人工诱导的神经元细胞发育期间,MYT1L的杂合子缺失会导致自闭症相关基因放松管制和非神经元靶基因激活,造成神经元发育迟缓。
Weigel等人的研究中突变小鼠表现出的神经发育结果和外在行为表现与 2021年圣路易斯华盛顿大学遗传学和精神病学副教授,首席研究员Dougherty及其团队的研究结果相似。
该团队首次介绍了MYT1L突变的小鼠,他们发现人类和小鼠神经元细胞受MYT1L突变的影响相似,因此小鼠是研究该基因的良好模型。
在他们的研究中,MYT1L单倍体不足的小鼠白质稀薄,体型肥胖,存在头部畸形。在行为测试中,幼鼠和成年鼠都过度活跃。成年雄鼠社会行为改变,不喜欢接触陌生老鼠。
3
药物作用
MYT1L缺失的神经元会产生过量的钠通道,通常表现在心肌细胞中。这些孔状蛋白质允许钠离子通过细胞膜,因此对电导率很关键,也对细胞的功能至关重要。如果神经细胞产生过多的这些通道蛋白,则可能导致电生理过度激活。
研究者发现MYT1L缺失的人类和小鼠神经元细胞中出现意想不到的电生理多动表型,还发现心脏电压门控钠通道SCN5A几乎增加了两倍。
在临床医学中,阻断钠通道的药物,比如拉莫三嗪已经使用了很长时间,它用于预防癫痫发作。
于是,研究者尝试使用拉莫三嗪来阻断钠通道。
当MYT1L缺失的神经元细胞和小鼠用拉莫三嗪治疗时,它们的电生理活动恢复正常。在小鼠中,该药物甚至能够抑制与ASD相关的行为,如多动症。
研究者认为即使在MYT1L缺失已造成大脑发育受损的情况下,药物治疗依然可以缓解脑细胞功能障碍,从而减少MYT1L突变小鼠的异常行为。
但当前的研究结果仅限于小鼠,尚未对患有自闭症谱系疾病的MYT1L异常患者进行临床研究。
因为拉莫三嗪已经被批准用于人体,该团队计划最早在明年开始在MYT1L突变人群中临床试验。
当前来说,还没有针对自闭症核心症状的特定药物。对MYT1l的研究为突破带来了希望,从本质而言,大多有关自闭症研究的投入都希望找到该病的遗传因素。
但需要注意的是,这种特殊的MYT1L基因突变可能只代表一些自闭症人群,还有很多自闭症人士并没有这种突变。即使发现这种药物有助于扭转自闭症的症状,它也可能只对具有该特定遗传变异的个体有效,而不一定对其他人有帮助。
例如在2001年一项小样本研究中对27名3-11岁自闭症儿童使用拉莫三嗪治疗,结果显示无效。另外重要的一点,研究人员当前还不确定这种药物的最终适用程度。
*本文经深圳市发育行为儿童专家与心理健康中心主任杨斌让审核后发布
参考文献:
1.Belsito KM, Law PA, Kirk KS, Landa RJ, Zimmerman AW. Lamotrigine therapy for autistic disorder: a randomized, double-blind, placebo-controlled trial. J Autism Dev Disord. 2001 Apr;31(2):175-81.
2.Chen J, Lambo ME, Ge X, Dearborn JT, Liu Y, McCullough KB, Swift RG, Tabachnick DR, Tian L, Noguchi K, Garbow JR, Constantino JN, Gabel HW, Hengen KB, Maloney SE, Dougherty JD. A MYT1L syndrome mouse model recapitulates patient phenotypes and reveals altered brain development due to disrupted neuronal maturation. Neuron. 2021 Dec 1;109(23):3775-3792.e14.
3.Mansfield P, Constantino JN, Baldridge D. MYT1L: A systematic review of genetic variation encompassing schizophrenia and autism. Am J Med Genet B Neuropsychiatr Genet. 2020 Jun;183(4):227-233.
4.Russ JB, Kaltschmidt JA. From induction to conduction: how intrinsic transcriptional priming of extrinsic neuronal connectivity shapes neuronal identity. Open Biol. 2014 Oct;4(10):140144.
5.Weigel, B., Tegethoff, J.F., Grieder, S.D. et al. MYT1L haploinsufficiency in human neurons and mice causes autism-associated phenotypes that can be reversed by genetic and pharmacologic intervention. Mol Psychiatry (2023).
编辑 | 夏天
封面图 | unsplash
