*仅供医学专业人士阅读参考
点击右上方“关注”, 准时接收每日精彩内容推送。
免疫诊治是一种新兴的具有高特异性和持久性的抗肿瘤方法,但由于肿瘤特异性抗原的低可用性和伤口边缘强烈的免疫抑制,阻碍了其在切除肿瘤中的应用。
为此, 陆军军医大学附属新桥医院骨科张瑗主任联合重庆大学罗忠教授 开发了一种纳米工程水凝胶,用于对切除的肿瘤诱导强大的协同铁死亡-免疫治疗效果 。β-环糊精(β-CD)通过席夫碱连接到氧化的海藻酸钠(OSA)上,可以捕获cRGD修饰的氧化还原反应Withaferin前药(WA-cRGD),获得水凝胶构建块(Gel@WA-cRGD)。在Ca2+介导的交联作用下,Gel@WA-cRGD快速形成生理稳定的水凝胶,其中多孔网络用于传递程序性细胞死亡配体1抗体(aPD-L1)。注射到术后伤口腔后,β-CD捕获的WA-cRGD被局部酸性分离,并被残留的肿瘤细胞内化,从而释放丰富的损伤相关分子模式(DAMPs)和肿瘤衍生抗原,激活抗原提呈递细胞介导的交叉呈递和下游细胞毒性T细胞(CTL)介导的抗肿瘤反应。此外,aPD-L1可以阻断PD-1/PD-L1的相互作用,增强CTL的效应功能,以克服肿瘤细胞介导的免疫抑制。 这种基于水凝胶的协同抗肿瘤铁死亡免疫治疗策略可能作为一种普遍适用的术后肿瘤管理方法。
相关研究内容以 “Injectable microenvironment-responsive hydrogels withredox-activatable supramolecular prodrugs mediate ferroptosis-immunotherapy for postoperative tumor treatment” 为题于2023年8月5日发表在 《Acta Biomaterialia》 。
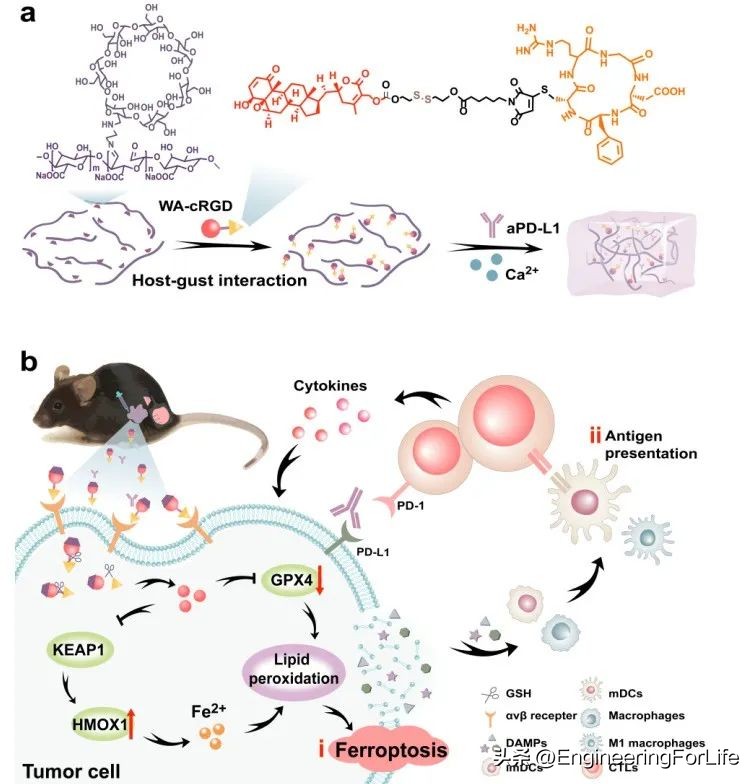
示意图 注射复合水凝胶诱导协同铁死亡免疫治疗术后肿瘤治疗
铁死亡性肿瘤细胞会将大量的DAMPs和肿瘤来源的抗原释放到伤口微环境中,然后被抗原提呈细胞(APCs),如树突状细胞(DCs)和巨噬细胞吞噬,以触发CTL激活的交叉提呈。aPD-L1可以阻断肿瘤细胞和CTL之间的PD-1/PD-L1的相互作用,从而减轻肿瘤细胞诱导的CTL抑制(示意图)。 这些优点不仅可以在伤口边缘建立抗肿瘤免疫微环境,消除残留的肿瘤细胞,还可以唤起全身抗肿瘤免疫,破坏远端肿瘤和转移。
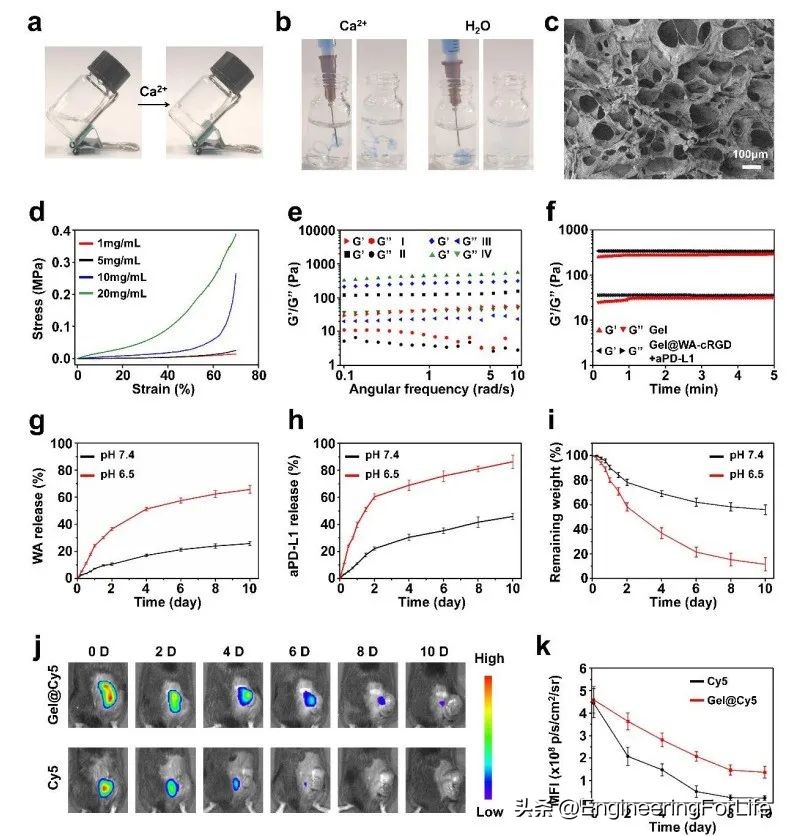
图1 复合水凝胶的理化表征
Gel@WA-cRGD溶液在没有添加CaCl2溶液的情况下仍 保持液态 (图1a、b)。获得的凝胶样品的扫描电镜图像显示了聚合物水凝胶材料的典型特征— 分散良好的多孔结构 (图1c)。在标准条件下获得的水凝胶的杨氏模量约为0.55 MPa,与活体组织相当,有望克服植入术后腔后复杂的力学挑战(图1d)。水凝胶在连续孵育后,存储模量(G')和存储模量(G'')保持在相同的水平(图1e、f), 表明其力学稳定性 。使用HPLC和ELISA测量了pH 7.4(模拟生理条件)和酸性pH 6.5(模拟酸性炎症伤口组织条件)下WA-cRGD和aPD-L1的释放谱,aPD-L1在酸性pH6.5的情况下释放速率更快,在仿生缓冲液中,WA-cRGD的释放率也稳定上升(图1g、h)。这些结果与凝胶在溶液中的降解速率一致(图1i),在pH为6.5下,复合水凝胶的降解速率快于7.4。含Cy5的水凝胶明显比Cy5溶液表现出更持久的荧光保留能力(图1j、k)。这些数据验证了 水凝胶的可降解性和微环境响应*药性**物给药性能,有利于术后伤口腔植入后实现可持续的抗肿瘤药物治疗 。
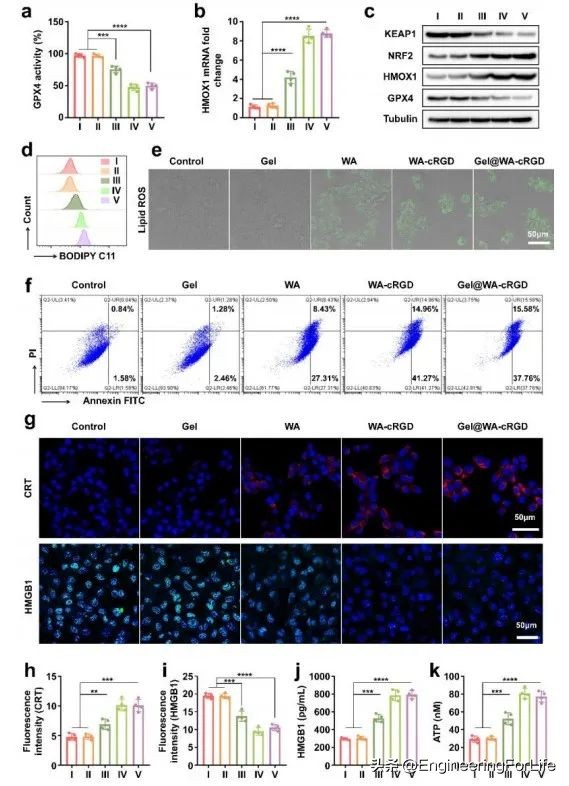
图2 复合水凝胶诱导铁死亡能力的评价
细胞谷胱甘肽过氧化物酶检测结果显示,Gel@WA-cRGD处理显著抑制了B16F10细胞中GPX4的活性,这是因为 WA-cRGD与未修饰的WA相比具有肿瘤靶向能力 (图2a)。Western blot结果显示,Gel@WA-cRGD组中GPX4的表达水平显著低于对照组(图2c)。Gel@WA-cRGD组HMOX1 mRNA水平是对照组的7倍(图2b), 证实了肿瘤细胞中KEAP1-NRF2-HMOX1信号的有效激活 。由于WA依赖的GPX4同时失活和Fe2+扩增,Gel@WA-cRGD组的肿瘤细胞的脂质ROS水平比对照组增加5倍,同时铁死亡标记基因PTGS2的表达水平增加了6倍(图2d、e)。流式细胞术分析显示,单独使用Gel@WA-cRGD处理可使B16F10细胞的存活率下降52%,这是由于其诱导铁死亡的能力(图2f)。WA、WA-cRGD和Gel@WA-cRGD处理的B16F10细胞CRT表达上调,但HMGB1水平降低,这是免疫原性细胞死亡(ICD)的典型特征(图2g、i)。使用ELISA和ATP测定不同组培养介质中HMGB1和ATP水平,观察到Gel@WA-cRGD组培养基中HMGB1和ATP丰度最高,进一步验证了HMGB1和ATP从死亡的铁死亡细胞向周围介质的转变(图2j、k)。
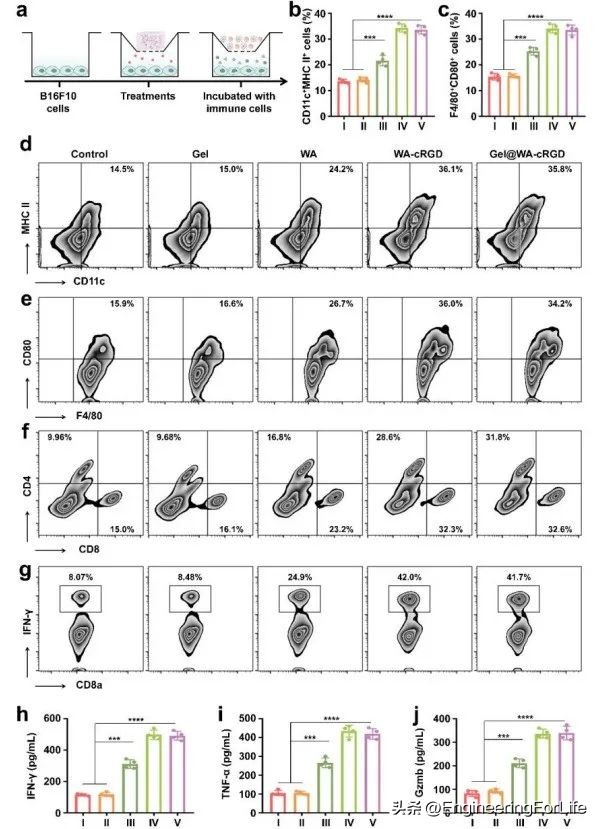
图3 Gel@WA-cRGD水凝胶免疫刺激能力的体外分析
本研究建立了一个跨孔共孵育系统来检测水凝胶激活抗原提呈细胞的能力,将肿瘤细胞置于底腔,将不同样本加入上腔,孵育1天后用脾免疫细胞替代(图3a)。流式细胞术分析表明,CD11+MHC-II+成熟树突状细胞的频率从对照组的14.5%增加到Gel@WA-cRGD组的35.8%,而M1样F4/80+CD80+巨噬细胞的频率从15.9%增加到34.2%(图3b-e)。Gel@WA-cRGD组显示CD4+和CD8+ T细胞显著扩增,其中CD4+ /CD8+ T细胞总频率比对照组高39%(图3f)。通过监测关键的促炎细胞因子和效应分子包括IFN-γ、TNF-α和Gzmb的分泌水平来测试它们的抗肿瘤活性,其中,Gel@WA-cRGD组的IFN-γ、TNF-α和Gzmb水平在各组中最高(图3g-j)。综上所述, Gel@WA-cRGD水凝胶可通过诱导肿瘤细胞发生铁死亡,诱发CTL介导的抗肿瘤免疫反应,有效抑制肿瘤细胞生长 。
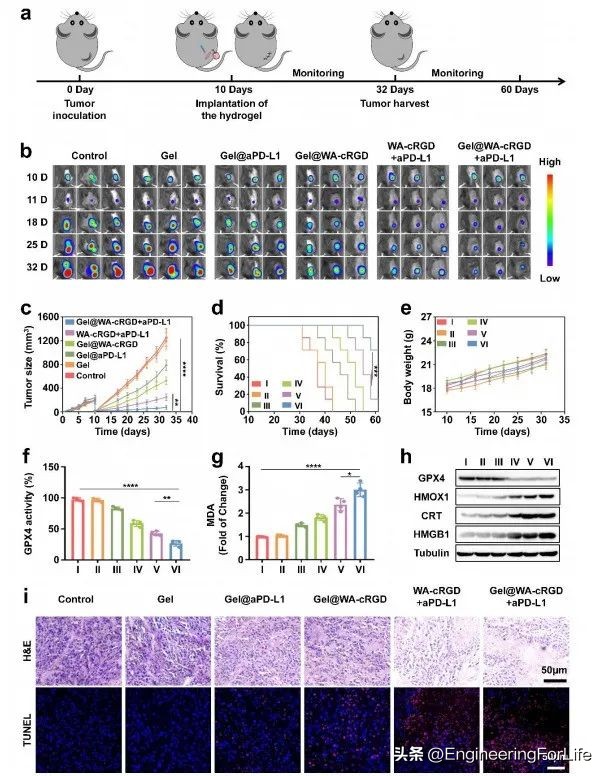
图4 Gel@WA-cRGD+aPD-L1水凝胶的体内抗肿瘤作用
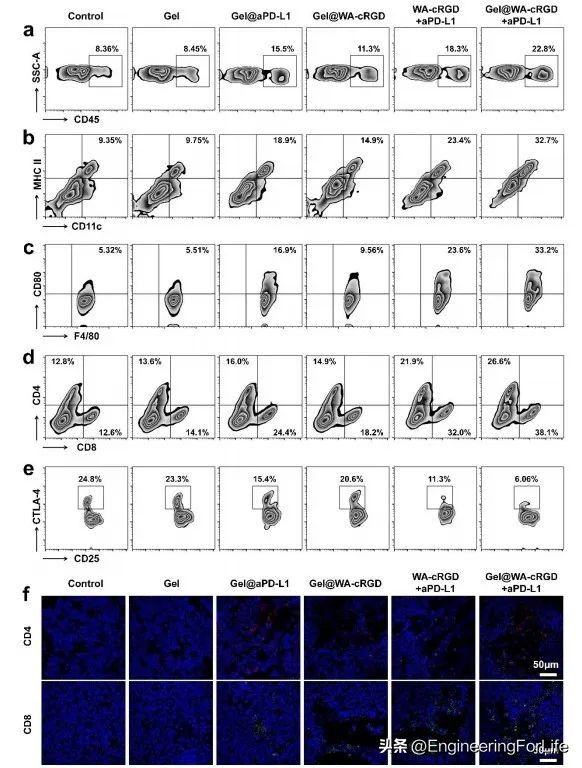
图5 水凝胶诱导体内抗肿瘤免疫反应
将水凝胶样品作为伤口敷料注入伤口腔(图4a)。Gel@WA-cRGD+aPD-L1水凝胶在所有组中显示出最大的肿瘤抑制作用(图4b)。其中Gel@WA-cRGD+aPD-L1组的最终肿瘤体积仅为75mm3左右,没有水凝胶保护的WA-cRGD+aPD-L1组达到248mm3,而对照组、WA-cRGD+aPD-L1和Gel组分别达到1253mm3、248mm3和1195mm3左右(图4c)。从不同组提取肿瘤组织进行H&E和TUNEL染色分析,发现Gel@WA-cRGD+aPD-L1治疗的肿瘤死细胞数量最大,即Gel@WA-cRGD+aPD-L1水凝胶能有效抑制肿瘤细胞生长和增殖,减轻术后肿瘤负担(图4i)。Gel@WA-cRGD+aPD-L1组小鼠在切除原发肿瘤长达60天后表现出最大的中位生存时间,而其他组小鼠由于肿瘤负荷在第60天前全部死亡(图4d)。通过监测体重变化研究水凝胶在体内的生物相容性,所有水凝胶组的平均体重与对照组保持在相同水平(图4e)。从Gel@WA-cRGD、WA-cRGD+aPD-L1和Gel@WA-cRGD+-GPD-L1组中提取的肿瘤组织GPX4表达显著降低,HMOX1表达的激活状态增强,丙二醛(MDA)的细胞丰度显著增加,表明封装的WA组分具有诱导铁死亡的作用(图4f、g)。由于水凝胶诱导的肿瘤细胞铁死亡,WB检测和免疫荧光成像均显示肿瘤微环境中HMGB1和CRT的急剧增加(图4h)。
用aPD-L1或含WA的水凝胶治疗切除的肿瘤,会导致淋巴细胞的整体浸润的增加(图5a)。Gel@WA-cRGD+aPD-L1导致成熟树突状细胞和M1巨噬细胞浸润频率增加最大,这归因于WA增强的肿瘤细胞免疫原性、aPD-L1依赖性的免疫抑制改善和水凝胶使药物缓释能力的共同作用(图5b、c)。Gel@WA-cRGD+aPD-L1组中肿瘤浸润的CD4+ /CD8+ T细胞显著扩张,进一步证实了肿瘤免疫微环境的改善(图5d、f)。Gel@WA-cRGD+aPD-L1水凝胶降低了肿瘤中Tregs的频率(图5e)。
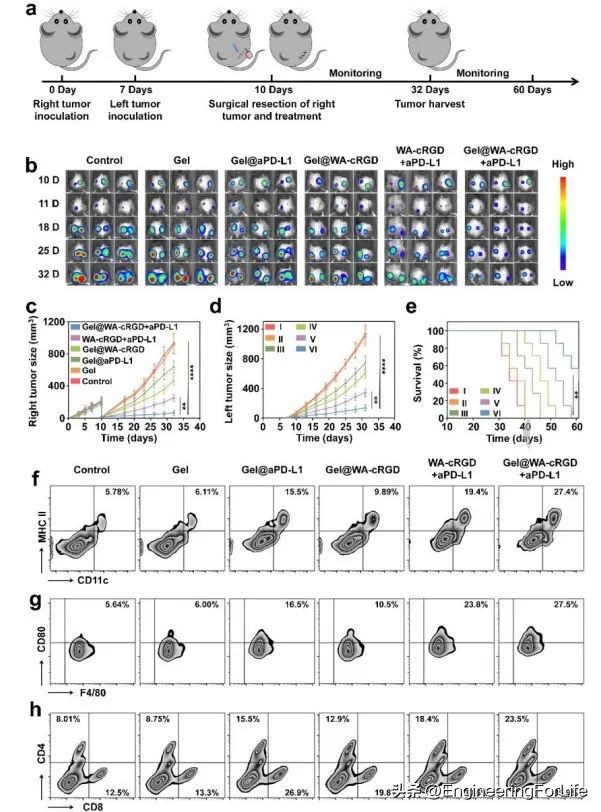
图6 水凝胶诱导全身抗肿瘤免疫反应,以消除远处肿瘤
为建立双侧B16F10肿瘤模型,B16F10细胞接种于小鼠右侧(原发肿瘤)皮下,7天后接种于对面的远端肿瘤,第10天将原发肿瘤部分切除,植入水凝胶开始抗肿瘤治疗(图6a)。Gel@WA-cRGD+aPD-L1水凝胶对原发肿瘤和远端肿瘤均有显著的抑制作用,WA-cRGD+aPD-L1、Gel@WA-cRGD和Gel@aPD-L1对远端肿瘤生长的抑制作用有限(图6b-d)。由于其明显抑制原发和继发肿瘤的能力,Gel@WA-cRGD+aPD-L1组小鼠在60天内生存时间最长(图6e)。Gel@WA-cRGD+aPD-L1治疗显著改善了远端肿瘤中成熟树突状细胞和M1巨噬细胞的浸润,同时远端肿瘤中CD4+ 和CD8+ T细胞的出现频率也明显增加(图6f-h)。 以上结果表明Gel@WA-cRGD+aPD-L1水凝胶可以诱导强大的全身抗肿瘤免疫反应来抑制远端肿瘤的生长。
综上, 本研究成功构建了一种具有协同铁死亡诱导和免疫调节作用的可注射性水凝胶,用于已切除的实体瘤的术后治疗 。该水凝胶通过Ca2+介导的天然海藻酸钠组分的交联构建,并与肿瘤靶向的WA-cRGD前药和aPD-L1进行纳米工程。水凝胶可以方便地注射到术后伤口腔内,并以微环境响应的方式降解,将WA-cRGD包埋的β-CD和aPD-L1释放到伤口边缘。WA-cRGD捕获的β-CD可以通过cRGD介导的靶向作用被肿瘤细胞选择性地吸收,并被其细胞质中过量的GSH激活,从而触发WA的铁死亡诱导作用,导致肿瘤源性免疫原性物种的释放,以识别和激活环境APCs。同时,aPD-L1进一步阻断肿瘤细胞与免疫细胞之间PD-1/PD-L1的相互作用,逆转TME中的免疫抑制。 本研究中的Gel@WA-cRGD+aPD-L1水凝胶能够诱导强大的全身抗肿瘤免疫,防止原发肿瘤复发,同时抑制远端肿瘤,可作为术后护理的多功能治疗平台。
了解更多
关注“EngineeringForLife”,了解更多前沿科研资讯~
