
撰文 | 胡小话
乳腺癌患者的脑转移发生率因疾病亚型不同而具有显著差异。比如说,HER2+及三阴性 (TN) 乳腺癌发生脑转移的风险要高于ER+/PR+乳腺癌。此外,根据转移灶出现时间的不同,HER2+乳腺癌的脑转移可分为同步性 (S-BM) ,潜伏性 (Lat) 和隐匿性 (M-BM) 三种 【1】 。为何同一类型的乳腺癌会具有不同的转移特征?这其中的分子基础目前尚不清楚。
2022年1月4日,来自德克萨斯大学西南医学中心的 Srinivas Malladi 教授领导的研究团队在 Cell Metabolism 上发表了题为 Metabolic diversity within breast cancer brain-tropic cells determines metastatic fitness 的研究文章, 揭示了乳腺癌的代谢多样性是决定其脑转移适应性的分子基础 。

作者通过在裸鼠中原位移植了两株乳腺癌患者来源的HER2+细胞 (HCC1954和SKBR3) ,并利用表型筛选的方式获取到基因型相同但脑转移特征不同的HCC1954 (S-BM,M-BM和Lat) 和SKBR3 (M-BM和Lat) 细胞系。有了这样的细胞工具,作者开始了后续的机制探究。
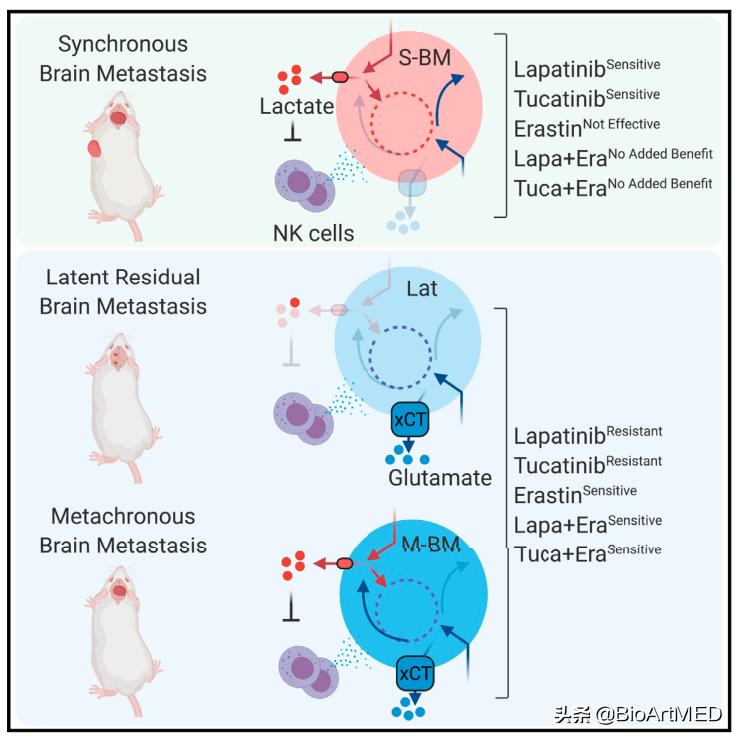
首先,通过对HCC1954来源的S-BM,M-BM和Lat细胞系进行RNA测序,作者发现Lat和M-BM的代谢特征与S-BM具有显著差异。通过代谢物分析,作者发现转移能力强的S-BM和M-BM排出的乳酸要高于Lat,而Lat和M-BM排出的Glutamate要高于S-BM。进一步,作者利用标记的13C6 glucose and 13C5 glutamine对这三类细胞进行了代谢流分析,结果再次证明这些细胞代谢Glucose和Glutamine的方式具有很大的不同,具体而言: 转移能力强的S-BM和M-BM利用Glucose和产乳酸的能力更强,而M-BM和Lat利用Glutamine和排出Glutamate的能力更强 。
胞外的乳酸既可以被肿瘤作为能源物质所利用,也可以重塑肿瘤的微环境来帮助肿瘤转移 【2】 。因此,为了探究外源性乳酸是否足以促进肿瘤的脑转移,作者对移植了HCC1954和SKBR3来源Lat细胞的裸鼠腹腔注射PBS、乳酸和乳酸钠处理,结果显示乳酸和乳酸钠处理会导致明显的脑转移,并降低荷瘤小鼠的总体生存率。进一步,作者发现荷瘤小鼠外周和转移灶中的NK细胞在乳酸处理组是显著减少的,这表明 外源乳酸会帮助潜伏期的乳腺癌细胞逃避由NK细胞介导的免疫监视 。
那么乳酸是如何帮助肿瘤逃避由NK细胞介导的免疫监视呢?通过功能研究,作者发现乳酸会抑制NK细胞的聚集和*伤杀**能力。体外的细胞*伤杀**实验结果也同样显示,与Lat细胞相比,S-BM和M-BM对NK细胞的*伤杀**具有更强的抗性,而外源添加乳酸或者用S-BM和M-BM细胞培养基处理Lat细胞都会增强其对于NK细胞的抗性。因此,这些实验结果表明: 潜伏期肿瘤细胞(Lat)会在NK细胞介导的免疫监视下保持平衡,但脑转移肿瘤细胞(S-BM和M-BM)产生的乳酸限制了NK细胞的功能从而逃避了先天免疫监视。
那么抑制乳酸的生成是否可以限制高侵袭性乳腺癌的脑转移呢?为了验证这一猜想,作者分别利用Oxamate (一种Pyruvate的类似物,可以抑制LDH的活性) 处理和敲低LDHA蛋白水平来去抑制肿瘤产乳酸的能力,结果显示这两种处理都可以抑制S-BM和M-BM的脑转移,但作者同时注意到一个有趣的现象: S-BM的响应程度要明显高于M-BM细胞 。通过进一步的机制研究 ,作者发现原来M-BM具有更强的应对氧化应激的能力 (与M-BM相比,S-BM和Lat细胞内GSH/GSSG水平更高,ROS水平更低) ,从而对LDHA的抑制具有更强的抗性。
以上的实验结果提示, S-BM和Lat细胞较强的抗氧化应激能力可能与其转移潜伏性相关, 并且作者发现胱氨酸/谷氨酸逆向转运蛋白xCT在S-BM和Lat细胞中是高表达的,而这一发现也与这此前观察到的更强的代谢Glutamine,排出Glutamate的表型相吻合。接下来,通过在S-BM和Lat细胞中敲低xCT,作者发现细胞内ROS水平显著升高,肿瘤的脑转移显著降低。 这些实验结果表明xCT介导了乳腺癌的潜伏性 。
最后,基于以上这些发现,作者考察了xCT与HERT2*制剂抑**联用对于潜伏性脑转移的治疗效果。结果显示xCT*制剂抑**Erastatin会显著增敏S-BM和Lat对于HERT2*制剂抑**lapatinib和tucatinib的响应。
综上,这项研究工作表明代谢多样性是导致HER2+乳腺癌细胞具有不同转移特征的分子基础。更为重要的是,这一发现有望在临床上帮助S-BM、Lat或M-BM脑转移的癌症患者制定更加精确的治疗方案。
原文链接:
https://doi.org/10.1016/j.cmet.2021.12.001
制版人:十一
参考文献
1. Kim, K., Marquez-Palencia, M., and Malladi, S. (2019). Metastatic latency, a veiled threat. Front. Immunol . 10, 1836.
2. Faubert, B., Solmonson, A., and DeBerardinis, R.J. (2020). Metabolic reprogramming and cancer progression. Science 368, eaaw5473.
转载须知
【原创文章】BioArt原创文章,欢迎个人转发分享,未经允许禁止转载,所刊登的所有作品的著作权均为BioArt所拥有。BioArt保留所有法定权利,违者必究。