关注公众号:佰傲谷BioValley,获取更多优质文章!
2019年5月,EMA批准了首款治疗β-地中海贫血(TDT)---LentiGlobin(商品名:Zynteglo)基因疗法上市,从此为该类患者带来了一次性的革命性疗法。此后,Bluebird公司给出了210万美元的定价,成为全球第二昂贵药物。
LentiGlobin是一款基于慢病毒的自体干细胞疗法,通过慢病毒载体将具备功能的人βA-T87Q-珠蛋白基因拷贝至取自患者体内的造血干细胞中,再将这些干细胞回输到患者体内,使其自主生成β-珠蛋白,从而消除或大幅降低继续输血需求。
基于同样的治疗原理,蓝鸟针对LentiGlobin开发了另一适应症镰状细胞病,2020年9月24日,LentiGlobin6已被EMA授予镰状细胞病的优先药物(PRIME)称号。
不过,受到近年来FDA对基因/细胞治疗CMC模块的严厉监管影响,这款疗法的上市进度遭受了延迟。2020年11月5日,FDA对该疗法的CMC提出新的要求,FDA指出,Bluebird需要提供用于试验的临床级/贴壁细胞和未来将使用的商业级/悬浮细胞之间的可比性数据。另外,FDA还提出,除了提供健康供体细胞外,Bluebird还需要提供GMP级慢病毒载体与该产品间的可比性分析数据,受此影响,该疗法原计划于2021年下半年提交的申请将被延迟到2022年底,LentiGlobin的上市进度总体后延一年。
LentiGlobin上市受延迟可能是对于蓝鸟来说还算是一个小打击,就在昨日(20221年2月17日),关于LentiGlobin传来了有一条恶讯,而这将直接决定LentisGlobin最终能否被批准进入市场。
据Bluebird官网公告披露,两名参加LentiGlobinⅠ期临床试验 (HGB-206)的镰刀状细胞贫血症(SCD)患者分别诊断出AML和骨髓细胞异常增生症(MDS),由此,Bluebird宣布终止LentiGlobin在镰状细胞病中的Ⅰ/Ⅱ,Ⅲ期临床研究,并且同时终止了Zynteglo的在市销售。受此影响,蓝鸟股价跌去38%。

目前公司正在调查患者的发病原因,以确定是否与此疗法所使用的慢病毒载体(BB305慢病毒载体)有关。由于已上市的Zynteglo也采用了BB305慢病毒载体,因此Bluebird决定在评估AML病例的同时暂时中止对Zynteglo的销售。
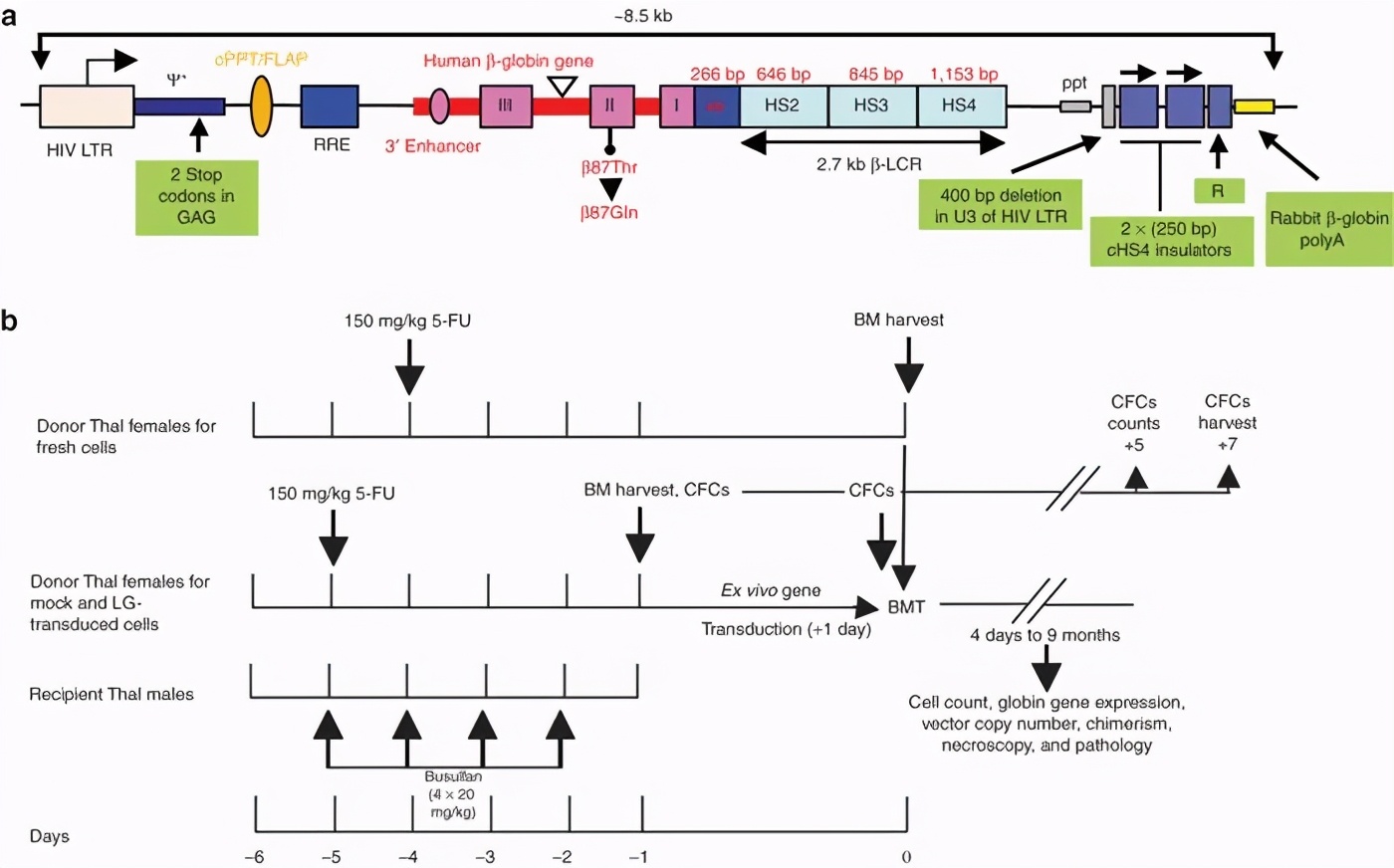
(a)人β-珠蛋白(βA)慢病毒载体(LentiGlobin)示意图,(b)治疗与移植方案
插入致癌
在某些情况下,病毒载体中的遗传物质会插入已知在细胞生长中起作用的基因附近,从而可能激活致癌基因,这种安全风险在基因治疗的早期临床研究就已有过报道。
2003年,一份来自伦敦和巴黎的报告声称,患有X-连锁重症联合免疫缺陷病”(SCID-X1)的5名儿童患者在接受基因治疗后患上了白血病。对这5位患者的分析结果显示,正是试验中采用的一种名为莫罗尼小鼠白血病病毒诱发了白血病,这种病毒有可能不小心插入和破坏一个名为LMO2的人类基因,LMO2的异常激活和人类白血病密切相关。
不过,蓝鸟生物公司告诉投资者,尽管他们的科学家已经发现病毒载体将DNA插入了接受治疗的镰状细胞患者的白血病细胞染色体中,但他们还不知道它的具体位置。将观察病毒DNA是否落在一个已知的促癌基因附近,也许是驱动其活动的原因。该公司表示,这些审查需要几周的时间。
而即便那些已经被批准进入市场的基因疗法,也暴露出了这种潜在的致癌风险。
2020年11月,Orchard Therapeutics收到了有关其已被批准用于治疗ADA-SCID(严重联合免疫缺陷症)的γ-逆转录病毒载体基因疗法Strimvelis不良事件的通知,一位最早于2016年接受了Strimvelis同情治疗的ADA-SCID患者被诊断患有T淋巴细胞白血病,初步发现,这位病例可能与Strimvelis所引入的插入事件有关,目前在接受白血病的针对性治疗。目前正在调查Strimvelis与T淋巴细胞白血病之间的联系,并宣布暂停Strimvelis销售。
另一家基因治疗公司uniQure的AMT-061被认为有机会成为第一个进入市场的B型血友病基因治疗药物,然而变数横生,还未到上市审评阶段,就在临床上遭受重挫。12月21日,uniQure宣布FDA已经叫停了其B型血友病基因疗法AMT-061的临床试验,原因是,一位接受AMT-061治疗的病人患上了肝细胞癌,目前初步临床诊断认为,该严重不良事件与AMT-061相关,目前,已经停止新患者入组。
结语
病毒作为天生的基因递送工具被广泛应用于基因治疗领域,成就了多款治疗遗传病的基因疗法。然而,长久存在的安全性隐患摆在基因治疗的最大障碍,过去一年内,多款基因疗法试验临床试验因出现严重不良事件/死亡被叫停。在这些临床研究中,病毒载体逐渐暴露出来的致命细胞因子风暴,高剂量毒副作用亦或是插入致癌等都给这些研究者敲响警钟。
在未来很长一段时间内,病毒载体仍将是主流的基因递送工具,面对这些不断浮出水面的安全性隐患,针对病毒载体的改良和优化将是研究者们工作的重中之重。
参考出处:
1. https://www.sciencemag.org/news/2021/02/gene-therapy-trials-sickle-cell-disease-halted-after-two-patients-develop-cancer
2. https://investor.bluebirdbio.com/news-releases/news-release-details/bluebird-bio-announces-temporary-suspension-phase-12-and-phase-3
3. https://www.barrons.com/articles/bluebird-bio-suspends-gene-therapy-trials-marketing-after-cancer-diagnosis-51613484672?siteid=yhoof2
版 权 声 明
欢迎个人转发分享。其他任何媒体、网站如需转载或引用本网版权所有内容须获得授权且在醒目位置处注明“转自:佰傲谷BioValley”。