*仅供医学专业人士阅读参考
点击右上方“关注”, 准时接收每日精彩内容推送。
口腔溃疡是一种常见的口腔黏膜炎性风疹,表现为炎症和口腔黏膜损伤,表现为疼痛。口腔潮湿和高度动态的环境使口腔溃疡的局部诊治具有挑战性。
近日,来自 苏州大学的郭江娜和冯岩教授团队 开发了一种基于聚离子液体的双氯芬酸钠(DS)负载口腔组织粘接贴剂(PIL-DS),该贴剂具有固有的抗菌、高湿环境粘接性能和抗炎活性,用于治疗口腔溃疡(方案1) 。PIL-DS通过抗菌和抗炎对金黄色葡萄球菌感染的口腔溃疡显示出显着的治疗效果,有望用于临床治疗口腔溃疡。相关论文“Antibacterial, Anti-inflammatory and Wet-adhesive Poly(ionic liquid)-based Oral Patch for the Treatment of Oral Ulcers with Bacterial Infection”于2023年5月13日在线发表于杂志《Acta Biomaterialia》上。

方案1 PIL-DS口腔组织粘连贴剂合成示意图及其在口腔溃疡伴细菌感染中的应用
1. PIL基贴片的制备和基础表征
首先,研究者 将含儿茶酚的离子液体(CIL)、丙烯酸(AA)和丙烯酸丁酯(BA)聚合,然后使用阴离子交换将CIL中的阳离子与活*药性**物成分阴离子(DS−)通过静电相互作用来构建PIL-DS(方案1)。 图1a显示了基于PIL贴片的化学结构,红外光谱、紫外可见峰、XPS和EDS能谱证实了PIL-DS的成功合成(图1b-e)。
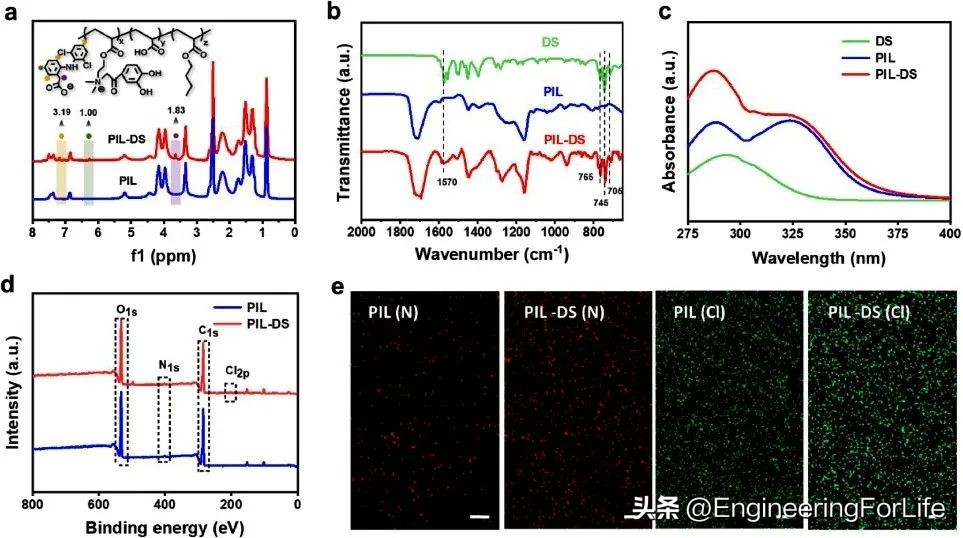
图1 PIL基贴片的基础表征
2. PIL基贴片的附着力和机械性能
研究者将罗丹明染色的PIL-DS贴片粘附在手指关节或潮湿的猪口腔粘膜上后, 由于羧基和儿茶酚基团与皮肤表面形成丰富的氢键,当手指弯曲或猪口腔粘膜折叠时,贴片仍然牢固地粘附在组织表面 (图2a)。PIL和PIL-DS贴片的搭接剪切强度分别为27.5和16.2 kPa(图2b)。 与市售口服贴剂相比,PIL基贴片的搭接剪切粘合强度显著较高(图2c)。 PIL-DS贴片可以有效地粘附在内脏组织上(图2d)。
此外, PIL基贴片在潮湿环境中能够实现自我修复(图2e),这可能是由阳离子-π相互作用、疏水缔合和氢键相互作用引起的 。如图2f所示,与耗散模量相比,更高的储能模量表明基于PIL的贴片保持稳定的凝胶状态,这是复杂多变的口腔环境所必需的。

图2 PIL基贴片的附着力和机械性能
3. 体外药物释放和抗菌性能
随后,研究者进行了体外药物释放测试。如图3a所示,DS−在8小时内从PIL-DS贴片中相对较快地释放,而后逐渐降低。 由于苯环和羧基的存在,加载的DS−不会完全释放,因为加载的DS−与CIL发生静电相互作用外,还可能与CIL和AA形成π-π共轭和氢键,从而限制了DS−的进一步释放。
抗菌实验中,与PIL贴片共培养32 h后,大肠杆菌、金黄色葡萄球菌和白色念珠菌的微生物活力分别降至99.1%、88.0%和88.2%(图3b、c)。 基于PIL的贴剂的抗菌特性可能来自疏水性BA和带正电荷的CIL。CIL中的阳离子可以通过静电相互作用吸附到带负电荷的细菌细胞膜上。同时,BA中的疏水烷基链可以进入细菌膜的脂质层,导致细胞质外渗和细菌死亡。 而与PIL-DS共培养后,大肠杆菌、金黄色葡萄球菌和白色念珠菌的微生物活力分别降至16.8%、0.1%和0.3%,差异显著,这与DS−和CIL的协同抗菌特性有关。 DS−通过干扰DNA合成对广谱微生物的增殖产生抑制作用。CIL的膜破坏机制可能会破坏细菌细胞膜,有利于DS−的进入并抑制所有基于DNA的过程。 活/死染色进一步证明了基于PIL的贴剂的抗菌性能(图3d)。膜流动性测试表明PIL基贴片对细胞壁稳定性的影响。
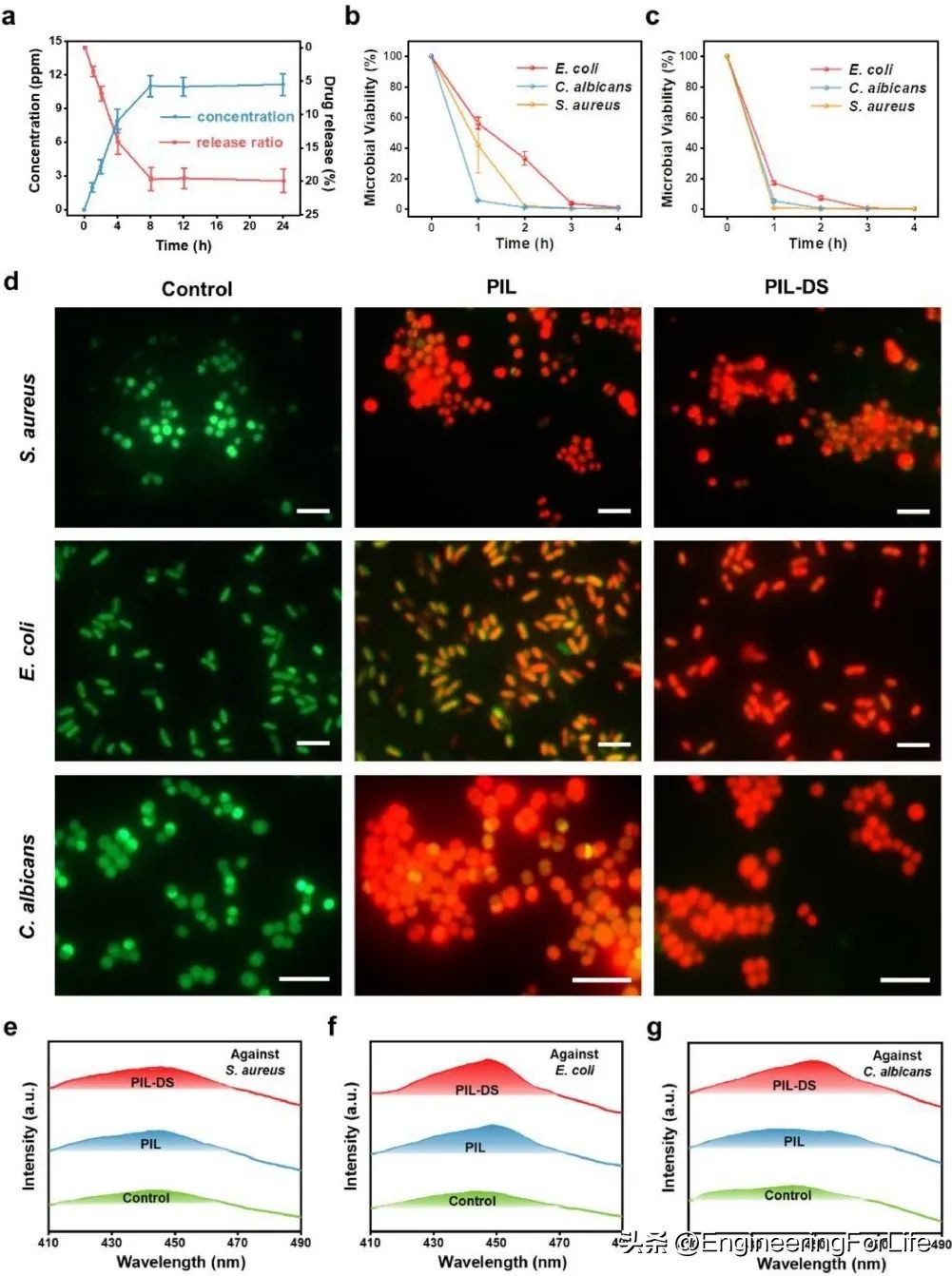
图3 PIL基贴片的体外药物释放和抗菌性能
4. 体外和体内的相容性和细胞相容性
通过溶血和细胞毒性测定进一步评估了基于PIL的贴剂的生物相容性。基于PIL的组没有溶血作用。图4a显示PIL组和PIL-DS组的溶血率分别为0.4%和0.53%。此外,基于PIL的基团显示出良好的细胞相容性。图4b显示,3T3细胞与PIL和PIL-DS条件培养基孵育24 h后的活力分别为95.26%和90.2%,表明基于PIL的基团具有低细胞毒性。这些结果表明, 基于PIL的贴片具有良好的生物相容性,使其适用于医疗应用 。

图4 体外和体内的相容性和细胞相容性
5. 抗炎评估
双氯芬酸属于一类对COX-1和COX-2酶均具有抑制作用的非甾体抗炎药。在图4c,d中,LPS刺激的RAW 264.7细胞表现出促炎细胞因子IL-6和IL-1β的过表达,而促炎细胞因子的表达在PIL-DS处理的细胞中受到抑制, 表明DS−的释放在PIL-DS中可以有效地保护细胞免受炎症 。
6. PIL基贴片对小鼠粘膜愈合的影响
文章最后,研究者建立了口腔粘膜缺陷(4 mm2)的小鼠模型产生并感染金黄色葡萄球菌。图5a显示了金黄色葡萄球菌诱导的口腔溃疡在第1、2、3和5天的代表性图像。 用PIL和PIL-DS贴片治疗的口腔溃疡比阳性对照组愈合得更好,表明伤口愈合促进作用 (图5b)。PIL和PIL-DS处理组的细菌活力分别约为8.3%和1.67%,表明P IL-DS在体内具有优异的杀菌效果 (图5c)。HE染色显示:PIL-DS组和阴性对照组之间的炎症细胞浸润没有差异,这表明P IL-DS贴片由于唐氏综合征而发挥有效和有力的抗炎作用(图5d,e) 。炎症因子表达的结果显示出相似的炎症变化(图5f,g)。
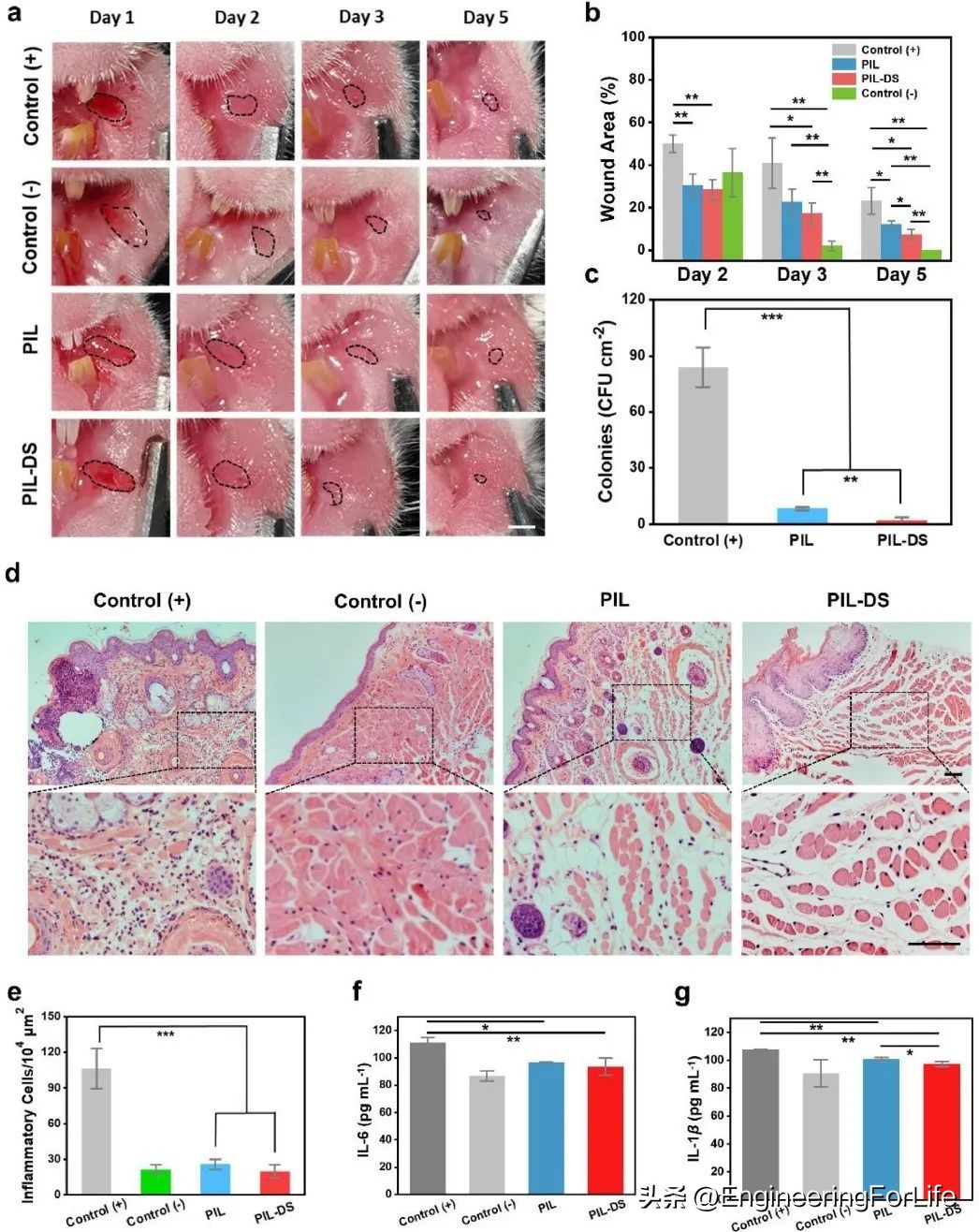
图5 体内应用基于PIL贴片促进小鼠模型中的粘膜缺损愈合
此外,CD11b染色测定揭示了PIL和PIL-DS贴片的抗炎反应。与对照组的炎症相比,由于贴片和抗炎DS−的抗菌能力,观察到几乎没有CD11b(图6a)。免疫荧光染色在基于PIL的组中表现出更高的愈合效率(图6b),并且在对照组中上皮覆盖不完全。
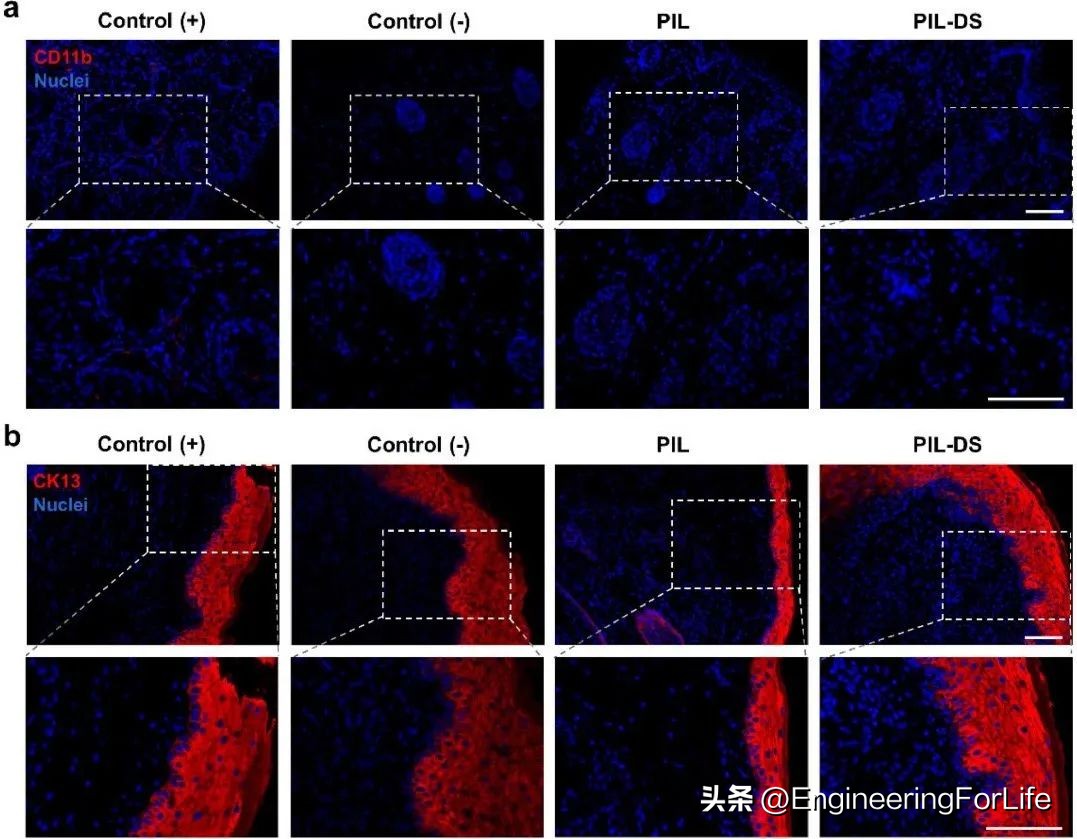
图6 体内抗炎反应
综上,本文制备了基于PIL的双氯芬酸钠负载颊组织粘附贴剂(PIL-DS)用于治疗口腔溃疡伴细菌感染。 所得的PIL-DS兼具载体和药物,具有较强的湿粘附性、良好的杀菌性能、促进溃疡愈合和抗炎活性。此外,拉伸性(延伸至1100%)和自愈特性使PIL-DS贴片能够适应复杂的口腔环境并保护溃疡表面。 因此,它作为治疗感染性溃疡的口服抗菌贴片具有巨大的潜力。
了解更多
关注“EngineeringForLife”,了解更多前沿科研资讯~
