
阻塞性睡眠呼吸暂停(obstructive sleep apnea,OSA)与胃食管反流病(gastroesophageal reflux disease,GERD)是临床常见疾病,目前已有大量研究证实OSA与GERD显著相关[1-4]。二者有许多共同危险因素,如性别、年龄、肥胖等[5-6]。但目前关于二者的因果关系仍存在争议。OSA患者中GERD、咽喉反流病(laryngopharyngeal reflux disease,LPRD)患病率均会显著增高[7-8],提示OSA可能是患者出现反流的危险因素。也有研究发现,GERD与OSA之间并不存在关联,呼吸暂停与反流事件没有同时或先后发生,提示GERD和OSA之间没有因果关系[9]。目前关于OSA与GERD的因果关系仍存争议。有研究指出,经持续正压通气(continuous airway positive pressure,CPAP)治疗后OSA患者Epworth嗜睡量表(ESS)评分和夜间反流症状均得到改善,而且CPAP的依从性越好,症状改善越明显[1,10]。但也有研究发现,CPAP治疗OSA合并GERD患者时,患者可能因为张口呼吸吞气而引起或加重GERD,而且吞气症状越明显,反流频率越高[11-12],
提示CPAP治疗不仅不能改善GERD,反而会加重GERD。为了探究CPAP治疗对于OSA合并GERD患者的疗效,以及进一步验证OSA能否引起或加重GERD,本研究对OSA合并GERD的患者进行了8周的随访。
1 对象与方法
1.1 研究对象及纳排标准 本研究于2020年9月—2023年1月连续入选就诊于北京大学人民医院老年科及呼吸内科完善多导睡眠监测(polysomnography,PSG)、初筛便携式诊断(portable monitoring,PM)、胃食管反流病问卷(Gastroesophageal Reflux Disease Questionnaire,GERDQ)的OSA合并GERD患者为研究对象。
纳入标准:呼吸暂停低通气指数(AHI)≥5次/h诊断为OSA;按《胃食管反流病基层诊疗指南(实践版·2019)》[13]将GERDQ得分≥8分诊断为GERD。本研究经北京大学人民医院医学伦理学委员会批准(伦理审批号:JKCJ202102),患者均知情同意。
排除标准:(1)合并活动性恶性肿瘤、急性感染期、严重心肺功能障碍、帕金森病、甲状腺功能减退或其他影响神经肌肉功能的疾病。(2)既往和当前诊断消化性溃疡、上消化道肿瘤、幽门梗阻等。(3)既往诊断OSA或GERD,入组时已经进行CPAP治疗或质子泵*制剂抑**(PPI)抑酸治疗。(4)临床相关数据不全。
1.2 分组 本研究使用观察性队列研究,将患者分为有CPAP者和无CPAP者,以α=0.05(单侧),把握度80%利用SAS软件估计总样本量为150例。纳入OSA合并GERD患者共192例,首先根据患者是否接受PPI分为有PPI者(n=85)和无PPI者(n=107),再根据是否行CPAP将有PPI者分为CPAP+PPI组(n=38)和PPI组(n=47),无PPI者分为CPAP组(n=48)和无治疗组(n=59)。在患者治疗4周时评估患者CPAP或PPI治疗依从性,每夜规律佩戴CPAP>4 h则认为CPAP依从性合格,遵医嘱使用PPI治疗则考虑PPI治疗依从性合格,自行停用或加用CPAP、PPI治疗者出组。8周后,本研究共出组10例,失访患者13例,最终CPAP+PPI组32例、PPI组41例,CPAP组43例、无治疗组53例。然后对CPAP+PPI组与PPI组,CPAP组与无治疗组GERD缓解情况、停药率等指标进行比较。
1.3 资料收集 收集患者一般资料,包括性别、年龄、身高、体质量、BMI、吸烟/饮酒史(本研究将连续或累积吸烟/饮酒时长≥1年认为具有吸烟/饮酒史)、治疗前GERDQ评分、睡眠监测指标〔AHI、氧减饱和指数(ODI,ODI3指夜间ODI下降>3%的次数)、夜间最低血氧饱和度(LSpO2)、夜间平均SpO2(MSpO2)〕,并在治疗2、4、6、8周时电话随访患者GERDQ、PPI停药时间、CPAP和PPI依从性等指标。按照《胃食管反流病基层诊疗指南(实践版·2019年)》[13]中GERDQ<8分、阳性症状或阴性影响<1分定义为GERD缓解,以GERD症状缓解或治疗8周作为随访终点。
1.4 统计学方法 数据处理使用SPSS 26.0软件系统,计量资料如果满足正态分布,则以(x±s)表示,正态性和方差齐性条件的组间比较采用两独立样本t检验;不满足正态分布的以M(P25,P75)表示,组间比较则采用秩和检验;CPAP组和无治疗组8周GERDQ得分,阳性症状得分比较采用协方差分析。计数资料以相对数表示,组间比较采用χ2检验。探讨CPAP治疗对OSA合并GERD患者的影响时,以8周或者GERD症状缓解为终点,采用Kaplan-Meier法绘制GERD患者的生存曲线图,计算各组累积GERD缓解率,并采用Log-rank法进行组间检验。采用Cox比例风险回归模型分析CPAP治疗与GERD缓解之间的关联,计算风险比(HR)及其95%CI。以P<0.05为差异有统计学意义。
2 结果
2.1 CPAP组与无治疗组患者疗效比较
2.1.1 CPAP组与无治疗组患者治疗前一般资料比较 CPAP组患者男性、饮酒史比例、基线阳性症状得分、AHI、ODI3高于无治疗组,差异有统计学意义(P<0.05);CPAP组患者年龄、基线GERDQ得分、LSpO2、MSpO2低于无治疗组,差异有统计学意义(P<0.05);两组BMI、吸烟史比例比较,差异无统计学意义(P>0.05),见表1。
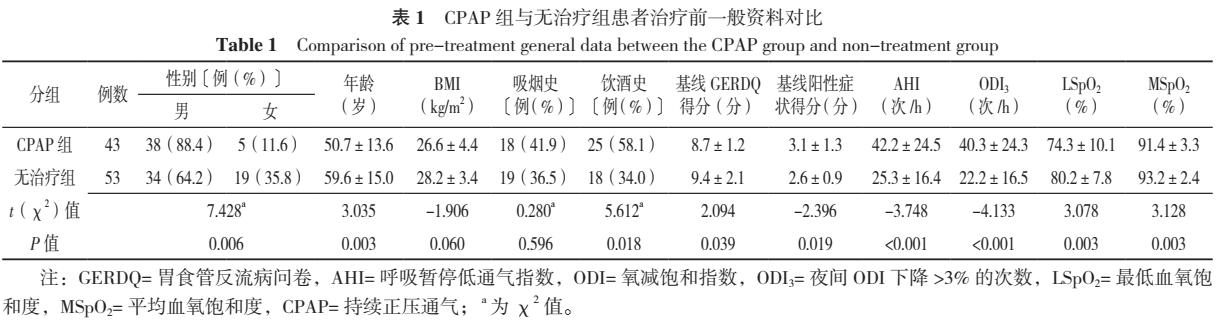
2.1.2 CPAP组与无治疗组患者治疗后缓解情况比较 两组2周GERD缓解率比较,差异无统计学意义(P>0.05);校正基线GERDQ得分、年龄、性别、AHI、饮酒史,协方差分析结果显示,CPAP组8周GERDQ得分低于无治疗组(P<0.05);校正基线阳性症状得分、年龄、性别、AHI、饮酒史,协方差分析结果显示,CPAP组8周阳性症状得分低于无治疗组(P<0.05);4周、6周、8周GERD缓解率高于无治疗组,差异有统计学意义(P<0.05),见表2。
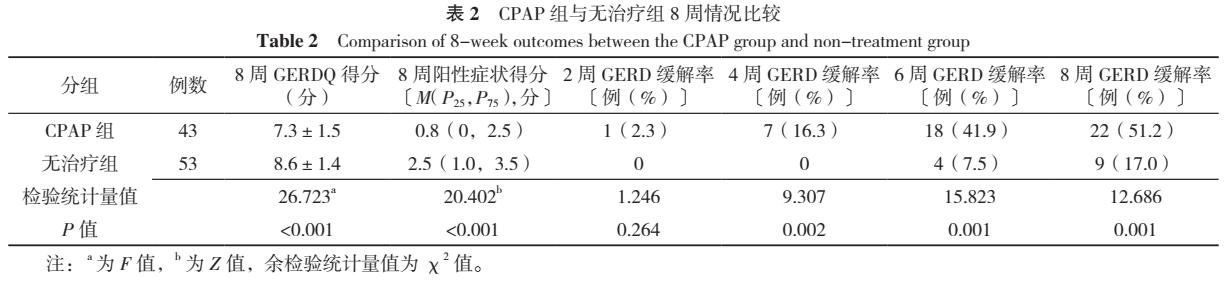
2.1.3 生存分析 以GERD缓解或8周为终点,绘制Kaplan-Meier生存曲线比较CPAP组与无治疗组疗效,CPAP组中位缓解时间为6周,无治疗组为7.5周;CPAP组GERD缓解率高于无治疗组(χ2=4.182,P=0.041),见图1。
2.1.4 未使用PPI的OSA合并GERD患者GERD缓解影响因素的多因素Cox比例风险回归模型 以GERD是否缓解(否=0,是=1)作为因变量,以是否使用CPAP(否=0,是=1)作为自变量,以性别(女=0,男=1)、年龄(<60岁=0,≥60岁=1)、BMI(<28 kg/m2=0,≥28 kg/m2=1)、AHI(<30次/h=0,≥30次/h=1)、吸烟史(否=0,是=1)、饮酒史(否=0,是=1)作为调整变量,进行多因素Cox比例风险回归分析,结果显示:CPAP治疗是未使用PPI的OSA合并GERD患者GERD缓解的影响因素〔B=0.859,SE=0.416,Waldχ2=4.254,HR=2.360,95%CI(1.044,5.338),P<0.05〕。
2.2 CPAP+PPI组与PPI组患者疗效比较
2.2.1 CPAP+PPI组与PPI组患者治疗前一般资料比较 CPAP+PPI组和PPI组患者性别、年龄、BMI、吸烟史比例、饮酒史比例、基线GERDQ得分、AHI、ODI3、LSpO2、MSpO2比较,差异无统计学意义(P>0.05),见表3。
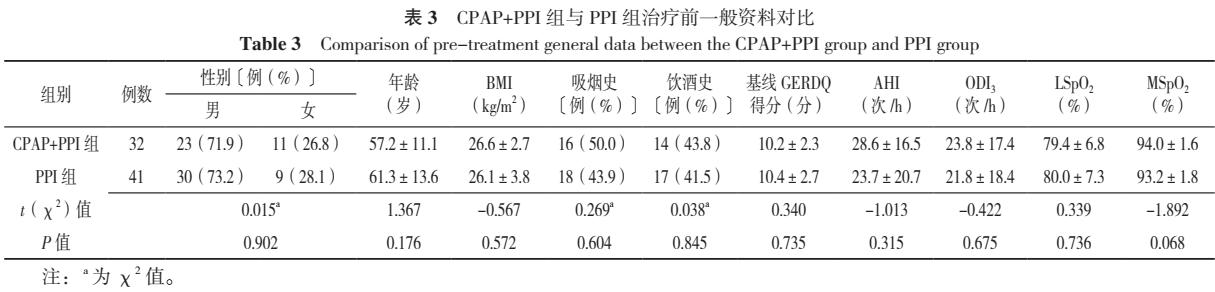
2.2.2 CPAP+PPI组与PPI组患者GERD缓解情况比较 两组患者8周后GERDQ得分、阳性症状得分比较,差异无统计学意义(P>0.05);但CPAP+PPI组2周、4周、6周GERD缓解率高于PPI组,且8周后停药率较PPI组增高,差异有统计学意义(P<0.05),见表4。
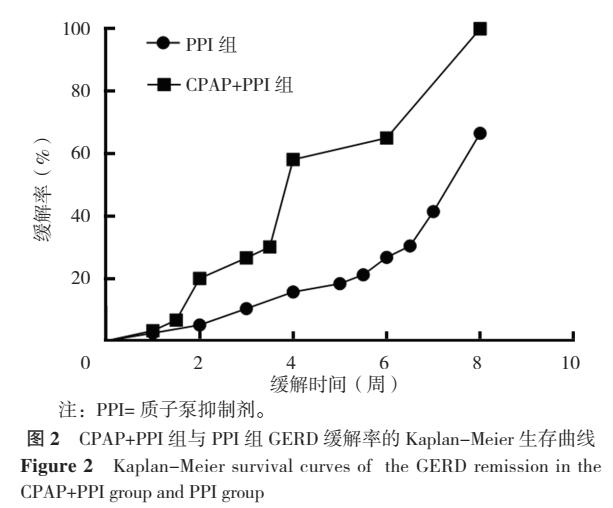
2.2.3 生存分析 按上述定义,以GERD缓解或8周为终点,绘制Kaplan-Meier生存曲线比较CPAP+PPI组与PPI组疗效,CPAP+PPI组中位缓解时间为3.9周,PPI组为6.1周;CPAP+PPI组累积GERD缓解率高于PPI组,差异有统计学意义(χ2=14.333,P<0.001),见图2。
2.2.4 使用PPI的OSA合并GERD患者GERD缓解影响因素的多因素Cox比例风险回归模型 以GERD是否缓解(赋值:否=0,是=1)作为因变量,以是否联用CPAP(赋值:否=0,是=1)作为自变量,以性别(赋值:女=0,男=1)、年龄(赋值:<60岁=0,≥60岁=1)、BMI(赋值:<28 kg/m2=0,≥28 kg/m2=1)、AHI(赋值:<30次/h=0,≥30次/h=1)、吸烟史(赋值:否=0,是=1)、饮酒史(赋值:否=0,是=1)作为调整变量,进行多因素Cox比例风险回归分析,结果显示,CPAP治疗是使用PPI的OSA合并GERD患者GERD缓解的影响因素〔B=1.812,SE=0.445,Waldχ2=16.612,HR=6.123,95%CI(2.562,14.635),P<0.05〕。
3 讨论
目前研究认为OSA与GERD相互影响,互相加重,形成恶性循环,治疗一种疾病可以对另一种疾病产生积极影响[14]。CPAP常作为OSA的首选治疗方法[15]。然而,CPAP治疗对OSA患者反流的影响仍存在争议。本研究证实在OSA合并GERD患者中,CPAP治疗能改善GERD症状。2021年国内一项Meta分析纳入了2个GERD症状评分及4个pH监测指标,证实CPAP治疗在改善OSA的同时,对反流相关的各项指标均有改善[16],本研究结果与之一致。KERR等[17]研究也显示经CPAP治疗后OSA患者的反流症状减轻。这种效应与通过CPAP治疗增加胸腔内压力、继发于正压的吸气压力减少、食管压力增加导致的气道阻塞减少有关,进而导致觉醒和运动频率减少,胃食管反流(gastroesophageal reflux,GER)风险降低。也有研究在同时接受了多导睡眠图、食管阻抗和pH监测的患者中发现夜间GER事件主要发生在夜间觉醒之后,CPAP治疗改善上气道阻塞之后,减少了患者的夜间觉醒,从而减少了患者反流事件[18]。JUNG等[19]研究指出,CPAP治疗后反流的改善继发于食管压力和食管下括约肌(low esophageal sphincter,LES)压力增加,因此其对OSA患者不具有特异性,对非OSA患者也有效。与之相反,KERR等[17]指出LES压力在GER降低中并不重要。夜间CPAP治疗减少了患者酸接触时间,这表明CPAP对GER有独立的积极影响[20]。也有研究指出,CPAP可以将一过性食管下括约肌松弛(transient lower esophageal sphincter relaxation,TLESR)频率降低近一半,而不会改变基线管腔食管压力或LES压力[21]。此外近年有研究指出,CPAP治疗不仅能改善OSA患者GER症状,同时还能缓解GERD相关的慢性咳嗽、改善咽喉反流等[22]。但另一些研究指出CPAP治疗增加了GER。WATSON等[23]研究在22例OSA患者中观察到CPAP治疗的患者GER频率增加,这种GER频率的增加可能与治疗过程中的吞气相关。SHEPHERD等[11]在对259例接受CPAP治疗的OSA患者研究中发现,吞气症患者的GER频率很高,而CPAP治疗会导致吞气症。有学者认为,吞气症可能通过胃扩张加剧短暂的下食管松弛而导致GER,尤其是夜间GER[11,23]。睡眠导致上食管压力降低,在CPAP期间,空气更容易随着压力向下移动到食管[24];增加的上食管腔内压力可能触发非吞咽性食管蠕动和空气向胃移动[25]。此外,空气存在时的食管扩张已被证明会触发LES松弛,进一步促进空气进入胃,由此产生的胃扩张可触发迷走神经介导的TLESR。众所周知,GER事件主要发生在TLESR增加期间;因此,吞气症引起的GER增加可能是由TLESR增加引起的。与之相反,BREDENOORD等[26]探究了在胃腔充气前后监测患有和不患GERD患者的食管阻抗、pH值和压力,发现空气灌注增加了气体反流的发生率;然而,胃酸反流事件并没有增加。SIFRIM等[27]也发现,GER的液体成分是作为主要事件发生的,与气体无关,吞气症可能并不会导致GERD发生。OZCELIK等[28]研究比较了在 CPAP前后平均LES压力、平均DeMeester评分,没有发现显著差异(P>0.05),认为CPAP治疗不会引发GERD。
本研究发现,CPAP治疗后的主观反流症状能明显改善,且所需时间更短,8周后PPI停药率更高。就反流症状改善及药物停用方面而言,CPAP联合PPI治疗显著优于单用PPI治疗,单独使用CPAP治疗也能改善甚至治愈部分GERD。
但是,本研究有一定的局限性。首先,同时合并2种疾病的患者治疗方案都是由医生沟通后患者自行选择,所以入组的患者基线资料并不完全匹配。患者可能由于胃肠胀气、口咽干燥、无法入睡、无法坚持佩戴、自觉OSA未明显影响生活等原因拒绝CPAP治疗而单独选用PPI治疗;也有部分患者因为反流、胃灼热等症状仅在饮酒、不当饮食等情况后出现,或者希望使用更加温和的胃酸中和剂而拒绝PPI治疗,单独使用CPAP治疗;还有部分患者可能因为OSA和GERD严重程度较轻、试图自行控制体质量、饮食来改善GERD和OSA而同时拒绝CPAP和PPI治疗。这种基线资料的差异可能影响研究的效果。其次,本研究主要以问卷形式展开,基于反流问卷的主观标准评估患者,没有客观参数如治疗前后食管内压力、pH值变化分析进行评估,需要大样本、前瞻性的研究对客观研究指标进一步验证。
综上所述,CPAP治疗能改善OSA合并GERD患者反流症状,同时增加PPI停药率。在OSA合并GERD患者中CPAP联合PPI治疗显著优于单用PPI治疗,CPAP组GERD症状改善也显著优于无治疗组患者。临床上OSA合并GERD时,应积极加用CPAP治疗,以便更好、更快缓解GERD症状。
本文无利益冲突。
参考文献略
本文来源:邓晶晶,李夏,薛倩,等. 持续正压通气治疗对阻塞性睡眠呼吸暂停合并胃食管反流患者的疗效观察研究[J]. 中国全科医学, 2023, 26(30): 3753-3758. DOI: 10.12114/j.issn.1007-9572.2023.0151.(点击文题查看原文)