关注公众号:佰傲谷BioValley,获取更多优质文章!
近日(2020年12月28日),Astellas宣布FDA解除了X-连锁肌小管性肌病(XLMTM)基因疗法AT132的临床搁置,而此前已经报告了3起死亡病例。
AT132
AT132来自于去年底安斯泰来与Audentes的并购交易。2019年12月2日, 安斯泰来溢价110%,耗资约30亿美元收购了这家基因疗法公司,AT132是该公司最重要的资产。今年初,安斯泰来正式完成了对Audentes收购。
XLMTM是一种严重的、威胁生命的罕见神经肌肉疾病,其特征是极端的肌肉无力、呼吸衰竭和早期死亡。XLMTM是由MTM1基因突变引起肌管蛋白缺乏或者功能障碍,而MTM1基因对于肌肉细胞成熟及保护是必需的。
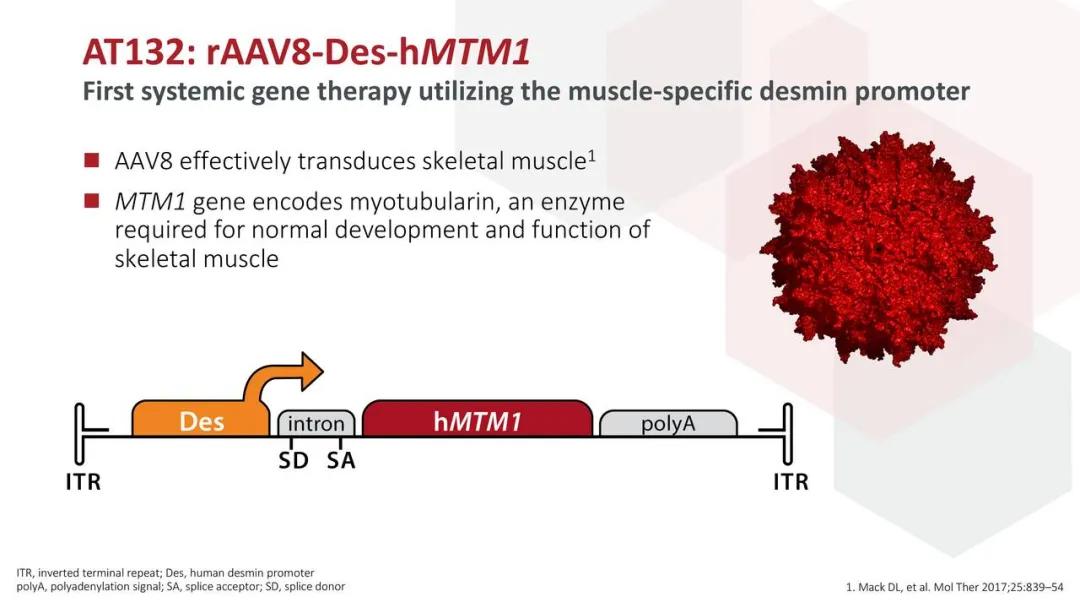
AT132使用AAV8载体将肌管蛋白1基因拷贝至患者肌肉细胞,并改善了疾病症状。日前,AT132已被FDA授予RMAT、罕见儿科疾病、快速通道和孤儿药称号,同时也被EMA授予PRIME指定以及孤儿药称号。
三起死亡案例
约一个月前,Audentes向患者社区告知了第一名患者死亡的消息。一位患者在接受AT132治疗后,出现了肝功能衰竭的严重不良反应,最终死于败血症。

一个月后(6月23日),Audentes又报告了AT132第二起患者死亡案例,这次Audentes在声明中报告了第二名患者死亡情况的详细细节,初步发现表明,死亡的最直接原因是败血症。
8月22日,Audentes报告了AT132(Resamirgene bilparvovec)研究中第三位患者死亡。
这三位患者均采用3×1014 GC/kg的高剂量治疗。并具有明显相似特征,包括年龄较大,体重较重,以及具有肝胆病史,并且均为AT132(3x1014 vg /kg)高剂量组患者。值得注意的是,在接受低剂量AT132(1x1014 vg/kg)治疗的6例患者中,尽管其中有4位有肝胆疾病史,但并未有一例经历过肝SAE。
基于AT132多次导致患者死亡的严重不良事件,Audentes已经放弃了今年申请批准计划。
心思难测的FDA
最近几年,FDA对新药的审批态度上似乎显得颇为柔和,很少拒绝新药上市申请、特别是那些高度创新药物。这一包容态度体现在DMD基因疗法尤为突出,NS Pharma公司开发的53号外显子跳跃疗法viltolarsen同样在疗效还未得到确切验证的情况下被FDA批准上市。
但业界还在认为FDA似乎放宽审批的时候,大约一周后,FDA出人意料的拒绝了BioMarin的A型血友病基因疗法valoctocogene roxaparvovec (商品名valrox)上市申请,原因是现在的Ⅲ期临床与Ⅱ期临床差别过大、FDA无法判断这个疗法的持久性。FDA要求BioMarin对所有Ⅲ期临床患者至少观察2年,而最后一名患者要到明年11月才满2年,所以valrox上市也至少要2022年以后的事情。这个消息令BioMarin下滑35%。
而随着valrox这一备受瞩目的基因疗法拒批之后,这个领域坏消息不断,多款基因疗法试验临床试验因出现严重不良事件/死亡(高剂量毒性、插入致癌等)被叫停,不少已经提交上市申请的基因疗法产品收到CRL,在市产品惨遭下架。与此同时,不仅仅临床开发受到了更严格管控,CMC方面也被加大了监管。
相较于其他在临床阶段被叫停的基因疗法,VY-HTT01连临床大门尚未迈进。10月12日,Voyager 的亨廷顿舞蹈症基因治疗(VY-HTT01)IND申请被FDA拒之门外,FDA认为Voyager需要解决某些CMC问题。Voyager也在申明中表示,在CMC问题得到解决前,VY-HTT01的临床*锁封**都不会解除。
10月17日,一名患有IIIA型粘多糖贮积症的五岁小女孩在参加Lysogene公司LYS-SAF302的AAV基因疗法的的II/III 期临床试验中去世。Lysogene在声明中表示,致死的直接原因尚不清楚,目前也没有证据表明患儿的死亡与LYS-SAF302的治疗有关,目前该公司还在收集更多信息。
10月30日,基因疗法公司Axovant推迟了其帕金森氏症基因疗法AXO-Lenti-PD的II期临床研究。原因是负责该基因疗法生产的Oxford Biomedica在10月中旬推迟了关键制造数据的生成,并且表示生产过程中“fill/finish”步骤存在问题。
11月2日,Orchard Therapeutics宣布暂时下架其已被批准用于治疗ADA-SCID(严重联合免疫缺陷症)的γ-逆转录病毒载体基因疗法Strimvelis,原因是Orchard几天前收到了与Strimvelis有关的不良事件通知,一位最早于2016年接受了Strimvelis同情治疗的ADA-SCID患者被诊断患上了T淋巴细胞白血病,初步发现,这位病例可能与Strimvelis所引入的插入事件有关,目前在接受白血病的针对性治疗。该公司已经表示:已将此事件告知了EMA以及其他监管部门,在此调查完成之前,不会再有其他患者接受Strimvelis的治疗。
11月5日,Bluebird bio基因疗*L法**entiGlobin(bb1111)治疗镰状细胞病的BLA被推迟了一年时间。根据公司申明,FDA希望获得更多有关该基因疗法用于商业化批量生产的精细工艺信息。简而言之,Bluebird需要证明该疗法从临床到商业级生产的“分析可比性(analytical comparability)”。受此影响,该疗法原计划于2021年下半年提交的申请将被延迟到2022年底。
11月10日,赛诺菲与合作伙伴健赞因已确定其针对血友病RNAi疗法fitusiran新的不良事件,目前已暂缓其全剂量的临床开发计划 。基于此次新出现的不良事件,赛诺菲表示他们已自愿暂停正在进行的fitusiran临床研究,并对该试验中患者非致命性血栓事件进行调查。
12月21日,uniQure宣布FDA已经叫停了其B型血友病基因疗法AMT-060的临床试验,原因是,一位接受AMT-060治疗的病人患上了肝细胞癌,目前初步临床诊断认为,该严重不良事件与AMT-060相关,该公司表示不再招募新患者入组。受此消息影响,该公司股价当日下跌超20%。
12月23日,FDA 叫停了 Voyager 的一项针对帕金森病基因疗法 NBIb-1817(VY-AADC)的临床试验。Voyager 公布了最新的临床试验暂停进展。其合作伙伴 Neurocrine 提交了一份参加 RESTORE-1 研究受试者磁共振成像出现异常的安全性研究报告。也就是这份报告,FDA 宣布暂停针对 VY-AADC 的 RESTORE-1 临床试验。Voyager 在一份申明中指出,这项观察的临床意义目前尚不清楚,正在评估其意义。
由此,在我们以为FDA似乎高悬明镜的时候,它总是做出令你大跌眼镜的决定。在AT132已经报告了三例死亡的严重不良事件的情况下,FDA还解除了临床*锁封**,这实在是令人小编费解,至今,安斯泰来也没有给出为何被解除临床*锁封**的明确解释。
虽然被叫停临床试验并不完全意味着被判死刑,也不是没有重新解冻的可能,但这么高发的严重不良事件已经足以警醒研究者们更为谨慎。而对于监管部门而言,如何做到松弛有度,既能在推动基因治疗临床转化应用的步伐同时,又能对基因治疗产品进行合理的监管,这需要找到平衡。
参考出处
1.https://www.businesswire.com/news/home/20201224005205/en/Audentes-Therapeutics-Announces-FDA-Lifts-Hold-on-ASPIRO-Clinical-Trial-of-AT132-for-Treatment-of-X-Linked-Myotubular-Myopathy-XLMTM
2.https://www.biospace.com/article/releases/audentes-therapeutics-announces-fda-lifts-hold-on-aspiro-clinical-trial-of-at132-for-treatment-of-x-linked-myotubular-myopathy-xlmtm-/
3.https://www.biospace.com/article/fda-lifts-hold-on-audentes-trial-of-x-linked-myotubular-myopathy-drug/
4.https://ir.voyagertherapeutics.com/news-releases/news-release-details/voyager-therapeutics-provides-regulatory-update-vy-htt01-program
5.https://www.biospace.com/article/voyager-shares-fall-after-fda-places-a-clinical-hold-on-phase-ii-gene-therapy-trial-for-parkinson-s-disease/
版 权 声 明
欢迎个人转发分享。其他任何媒体、网站如需转载或引用本网版权所有内容须获得授权且在醒目位置处注明“转自:佰傲谷BioValley”。