曲妥珠单抗是1990年开发的首个HER2抗体,其在临床上的应用促进了其他HER2靶向药物的发展,过去二十年里,HER2抗体联合化疗药物的发展也取得了临床成功,并极大改善了HER2阳性乳腺癌的预后。尽管如此,耐药仍然最常见并具挑战性,尤其在晚期乳腺癌中,阐明耐药机制将为有效疗法的开发奠定基础。本文总结了HER2靶向治疗的耐药机制以及HER2双靶向新辅助或辅助治疗研究进展。
HER2信号通路及相关耐药机制
HER2阳性(HER2+)占所有乳腺癌的15%~20%,以HER2过表达或ERBB2扩增为特征,HER2是酪氨酸激酶受体家族的四成员之一:HER1(也称EGFR)、HER2、HER3、HER4。当被激活时,HER蛋白发生自体二聚化或异体二聚并激活信号通路级联反应,包括PI3K-AKT和RAS-MAPK (ERK)通路,这些通路在细胞增殖和生存、肿瘤细胞转移方面发挥重要作用(图1a)。
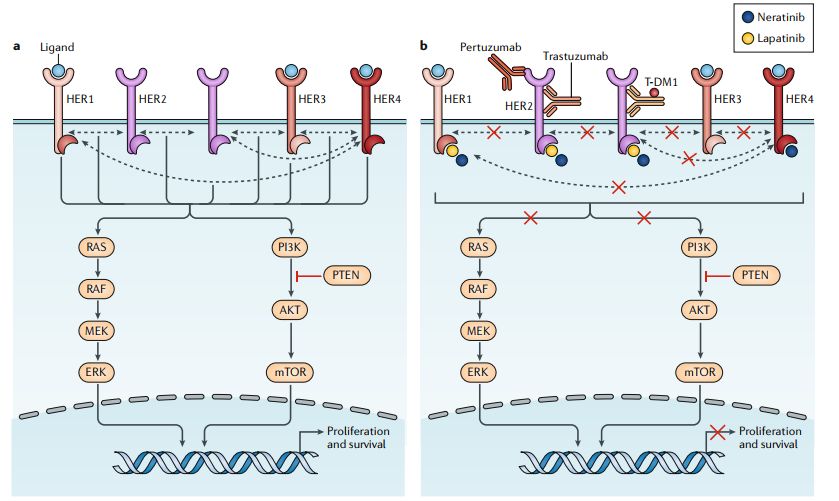
图1 HER家族成员和信号通路
当HER2被有效抑制时,HER2靶向治疗的耐药主要有机制:一是下游信号通路的失控导致HER信号通路的组成性激活;二是ER信号通路和其他转录因子双向交叉对话;三是替代信号通路的上调而刺激细胞增殖(图2)。
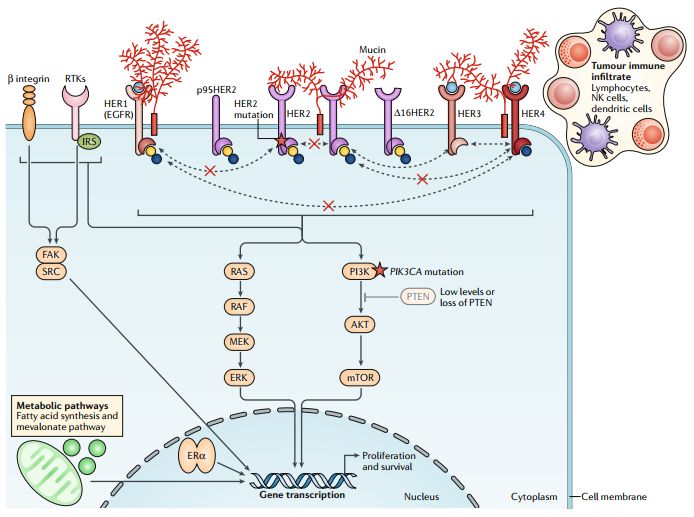
图2 耐药机制图示
HER2靶向药物
目前开发的HER2靶向药物见表1,主要分三类:HER2单克隆抗体例如曲妥珠单抗帕妥珠单抗等;小分子酪氨酸激酶*制剂抑**例如拉帕替尼、阿法替尼等;抗体药物偶联物(ADC)例如T-DM1(图1b)。目前,曲妥珠单抗、帕妥珠单抗、拉帕替尼、来那替尼和T-DM1已获FDA和EMA批准用于HER2+乳腺癌的治疗,几种新型药物正在临床验证中,例如margetuximab、tucatinib、pyrotinib和trastuzumab deruxtecan(表1)。
表1 已获批HER2靶向药物和新型药物
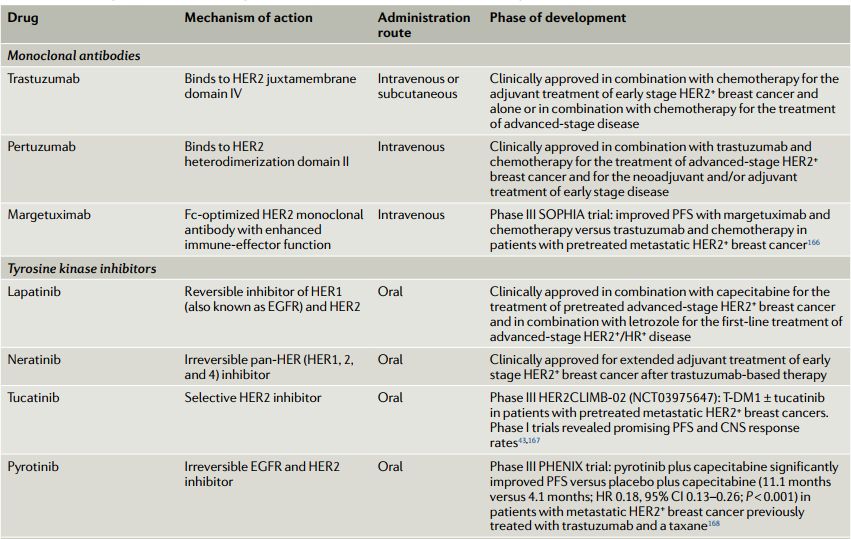
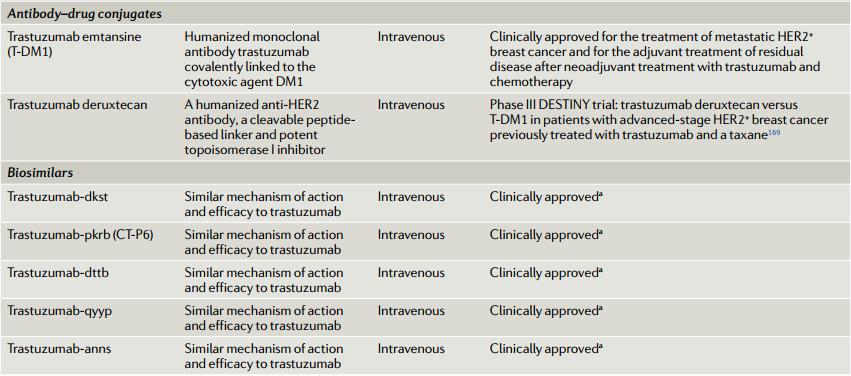
双靶向HER2新辅助治疗
临床前研究显示,HER2靶向药物的联合应用优于单一HER2靶向治疗。而HER2双靶向联合治疗在新辅助治疗、辅助治疗和转移性患者中都表现出优势。
早期HER2+患者虽接受了曲妥珠单抗+化疗,但15%-20%的患者仍会疾病复发,部分原因可能是对HER受体的抑制不完全。HER2双靶向治疗的疗效首次在CLEOPATRA研究中发现,帕妥珠单抗加入到曲妥珠单抗+多西他赛显著延长了转移性乳腺癌患者的OS达15.7个月,两组OS分别为56.5个月和40.8个月(P < 0.001),随后,为改善患者的pCR率,在多项研究中探索了双靶向治疗在新辅助治疗中的疗效(表2)。
表2 双靶向治疗在新辅助治疗中的pCR率
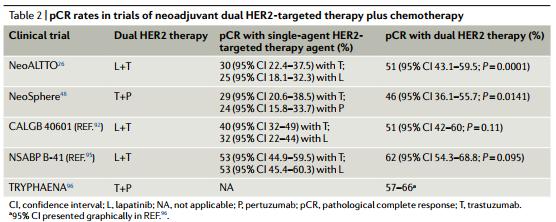
帕妥珠单抗获批用于新辅助治疗基于NeoSphere研究,该研究证实了帕妥珠单抗加入到曲妥珠单抗+多西他赛新辅助治疗可显著改善pCR率,两组分别为45.8%和29%(P=0.014)。
NeoALTTO研究显示,拉帕替尼+曲妥珠单抗+多西他赛显示出更优的pCR率(51.3% vs 29%,P=0.0001),更新数据显示,与曲妥珠单抗组相比,HER2双靶向治疗组6年的无事件生存率(EFS)和OS在数值上更高,分别为74% vs 67%(HR=0.81,P = 0.35), 85% vs 79% (HR =0.72,P = 0.26),HR-亚组的6年EFS率分别为74%和63%(HR=0.81,P=0.52),无统计学差异。但是,与未达到pCR的患者相比,获得pCR患者的6年EFS率有显著提高,分别为77%和65%(HR=0.54,P=0.005)和6年OS率分别为89%和77%(HR= 0.43,P = 0.005)。
双靶向HER2辅助治疗
研究者也探索了HER2双靶向辅助治疗的疗效。首先在ALTTO研究中进行了探索,但结果却令人失望。ALTTO研究6年随访结果并未证明拉帕替尼+曲妥珠单抗+化疗在DFS方面优于曲妥珠单抗+化疗,6年DFS率分别为85%和82%,OS率分别为93%和91%。
APHINITY研究旨在评估帕妥珠单抗+曲妥珠单抗+化疗在辅助治疗中的疗效,结果显示,3年iDFS率有所改善,两组分别为94.1%和93.2%(HR=0.81,P=0.045),高危、淋巴结阳性患者获益最大,3年iDFS率分别为92.0%和和90.2%(HR=0.77,P=0.02),近日,在SABCS大会上,APHINITY研究公布了6年随访结果,发现淋巴结阳性患者仍能从双靶向辅助治疗中获益。结果提示,辅助治疗中帕妥珠单抗的加用对高危亚组更有效。值得注意的是,化疗用于辅助治疗中可能“稀释”了拉帕替尼或帕妥珠单抗加入曲妥珠单抗中产生的协同作用,事实上,化疗对某些肿瘤细胞有效,因此,在减少化疗使用的情况下,拉帕替尼或帕妥珠单抗的获益人群可能会扩大。
那么通过不同的“联合”方式是否能改善结果呢?ExteNET研究探讨1年曲妥珠单抗标准治疗基础上序贯1年来那替尼(不可逆泛HER*制剂抑**)的疗效。结果显示,1年来那替尼治疗导致了适度但有意义的改善,5年iDFS的绝对获益为2.5%,来那替尼组和安慰剂组分别为90.2%和87.7%(HR=0.95,P= 0.0083)。值得注意的是,HR+亚组的获益更多,5年iDFS分别为91.2%和86.8%(HR=0.60),HR-组为88.8%和88.9%。在ExteNET研究的亚组分析中,4个或以上淋巴结阳性患者从这种HER2靶向治疗方案中获益最大。各治疗组的5年DFS率(91.6% vs 89.9%,P=0.065)和CNS复发率(1.3% vs 1.8%,P=0.333)无差异。来那替尼已获FDA批准用于任何早期HER2+乳腺癌辅助治疗后的扩展治疗,而EMA则限制来那替尼用于HER2+/HR+亚组患者。
虽然新辅助治疗的pCR率为30%-60%(见表2),但手术时有残留病灶的患者仍有很高的疾病复发和死亡风险。III期KATHERINE研究评估了14个周期T-DM1对比1年曲妥珠单抗用于早期HER2+乳腺癌辅助治疗的疗效,中位随访41个月时,T-DM1组降低了50%的疾病复发或死亡风险,3年iDFS率分别为88.3%和77%(HR=0.5,P<0.001),并降低了5.4%的远处复发风险(10.5% vs 15.9%)。值得注意的是,T-DM1的获益与临床病理特征无关,包括疾病状态和HR状态,即使是微小残留病变(≤1cm)和新辅助双HER2靶向治疗队列也能从治疗中获益。T-DM1在手术时处于较高病理学疾病状态、淋巴结阳性、HR-患者中均观察到T-DM1能带来获益,与曲妥珠单抗疗效相当的是中枢神经系统的复发率,两治疗组均为5%左右。总之,KATHERINE研究确立了新辅助治疗及手术后仍有残留病灶患者的辅助治疗新标准。
参考文献:
Goutsouliak K, Veeraraghavan J, Sethunath V, et al. Towards personalized treatment for early stage HER2-positive breast cancer [published online ahead of print, 2019 Dec 13]. Nat Rev Clin Oncol. 2019;10.1038/s41571-019-999.doi:10.1038/s41571-019-0299-9.