-
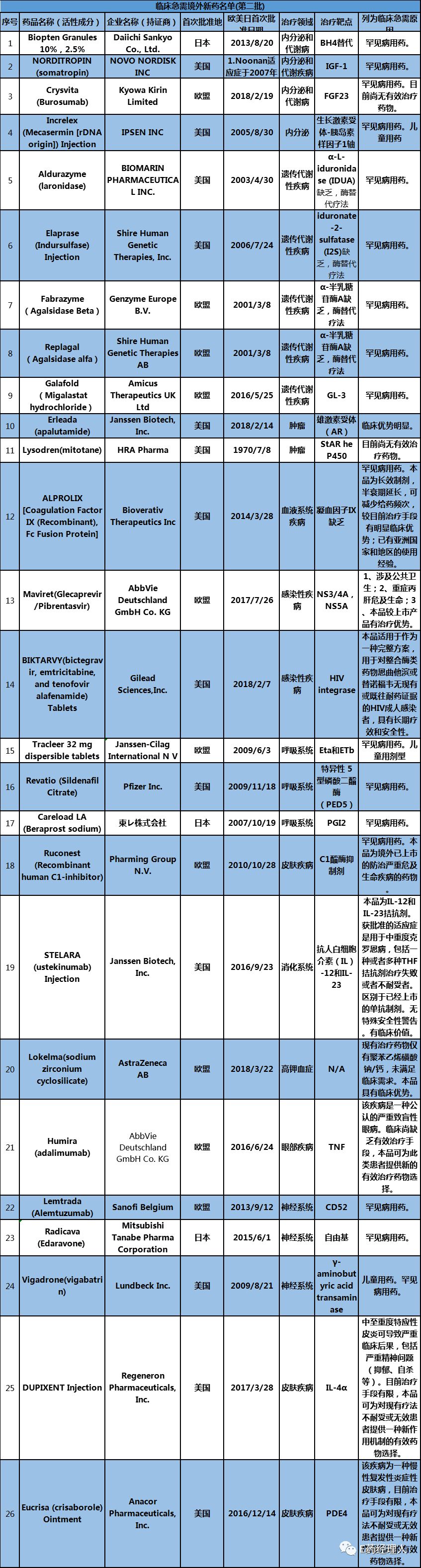
5月29日,国家药品监督管理局药品评审中心(CDE )公布了第二批临床急需境外新药名单,共包括 26 个品种。与公示阶段的 30 个品种相比,新增一个罕见病品种药品,相对原名单中药品减少了5个。

第二批名单主要以罕见病为主,26 个药品中,罕见病药品有 17 个。涵盖了高苯丙氨酸血症、Noonan 综合症、Prader-Willi 综合症、高胆固醇血症、肺动脉高压、克罗恩病(CD)、多发性硬化(MS)、遗传性血管性水肿、肌萎缩侧索硬化(ALS)在内的十余种罕见病。
据E药经理人的统计,此次进入名单的产品,从产品首次在欧美日等国家获批,到以临床急需境外新药的形式进入中国,平均所需时间为8年7个月。其中,从获批到进入此次名单时间最长的是HRA制药的密妥坦。自1970年上市后,到目前为止密妥坦依旧是唯一被批准治疗肾上腺皮质癌的靶向药物。而时间最短的一个药则为阿斯利康的Lokelma,其2018年3月22日最早在欧盟获批,用于高钾血症的成年患者的治疗,而国内现有治疗药物仅有聚苯乙烯磺酸钠/钙,未满足临床需求。
值得关注的是,全球“药王”修美乐也在这批名单中,但是是以新适应症入围。艾伯维5月20日宣布,FDA已授予修美乐治疗非感染性中、后或泛葡萄膜炎或慢性非感染性前葡萄膜炎的孤儿药地位。而随着新适应症的获批,此前被认为是“廉颇老矣”的修美乐或将迎来一个新的增长点。
其中,已经在国内上市的诺和诺德地特胰岛素注射液(Levemir Insulin Detemir [rDNA origin] Injection)退出公示名单,取而代之是 NORDITROPIN (somatropin) injection,用于治疗罕见病Noonan 综合症和Prader-Willi 综合症。Insight 数据库显示,该药已经在国内获批进口,商品名为诺泽。
除了地特胰岛素注射液之外,退出这一批名单的还有4个品种:日本第一三共株式社会用于治疗和预防 A 型和 B 型流感病毒感染的 Inavir (laninamivir octanoate hydrate),现阶段暂未在国内申报;日本盐野义制药和罗氏联合申报的用于治疗甲型和乙型流感的Xofluza (巴洛沙韦),目前处于临床实验中;
赛诺菲用于治疗高胆固醇血症的 Praluent Alirocumab,目前已经在国内开展临床;Santen OY 公司用于治疗 4 岁以上儿童及青少年严重性春季角膜结膜炎(VKC)的 Verkazia(ciclosporin)暂未在国内申报。
截至目前,在CDE 发布的两批临床急需境外新药名单中,包括 74个新药,全部都是国内缺乏的救命新药,主要针对罕见病、国内尚无有效治疗手段的药品、与现有治疗手段相比具有明显临床优势的新药。在 2018 年 11 月 1 日,CDE 公布第一批名单的同时宣布,已经有 8 个在我国获批上市。据 Insight 数据库统计,到目前为止,第一批名单48个品种中已经有15个品种获批上市。
根据第一批名单中每个品种在中国的审评时长统计发现,除了赛诺菲和吉利德的两个品种分别于 2014 年和 2016 年申报上市外,其余品种均为 2017 年及以后开始报产,从申报上市到获批上市平均时长为 9.9 个月。而这在很大程度上得益于国家对罕见病、重大疾病等的药品政策红利,努力缩小国内与全球用药可及性的差距。
*本文版权均属E药经理人所有,如需转载请在后台留言,经允许后方可转载,并在文首注明来源、作者。