肺癌临床诊疗指南(2021版)(以下简称“指南”)于2021年6月22日发表于《中华医学会杂志》 。该指南共33页,涵盖筛查、诊断、病理学评估、分期治疗原则、治疗、随访共6部分内容,内容全面,以下将对6部分进行解读。
病理学评估
病理学评估包含三部分内容:病理学亚型、免疫组织化学检测和分子病理学检测。
1.病理学亚型
目的 :明确病变性质并为临床病理分期提供相关信息,同时包含分子检测标本的质量控制。
标本类型 :活检标本、细胞学标本、手术切除标本及拟进行分子检测的其他标本。
病理组织学分型 :采用2021年版WHO肺肿瘤组织分型标准,不同标本的诊断原则不同;
组织标本诊断原则 :
a.鳞癌
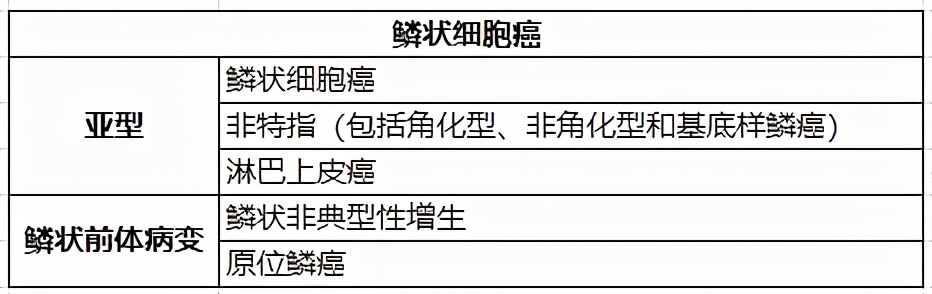
鳞状细胞癌:出现角化和(或)细胞间桥或表达鳞状细胞分化标志的上皮性恶性肿瘤;
淋巴上皮癌:低分化的鳞状细胞癌伴有数量不等的淋巴细胞、浆细胞浸润,EB病毒常常阳性,需注意与鼻咽癌鉴别
b.腺癌

PS: 这里面变化最大的当属“原位腺癌”,被踢出肺恶性肿瘤,作为腺样前体病变,对患者最大的影响可能是保险公司的理赔条款进行相应的调整。对于浸润性非黏液腺癌来说,更细分的病理类型使得预后更精准,同时也可以进一步指导治疗。
c.腺鳞癌:
指含有腺癌和鳞状细胞癌2种成分,每种成分至少占全部肿瘤的10%。
PS: 对于指导治疗来说,含有腺癌成分就有可能出现敏感基因突变,所以这部分患者也需要进行基因检测,进而指导后续治疗。
d.神经内分泌肿瘤:
神经内分泌肿瘤的亚型情况如下图所示,其中有3种复合型肿瘤:
复合型SCLC: SCLC合并NSCLC的任何一种组织学类型;
复合型LCNEC:LCNEC 伴其他NSCLC 成分;
复合型SCLC/LCNEC或SCLC/LCC(大细胞癌):合并大细胞并且大细胞成分占比≥10%。

核分裂和坏死指标是区分4种神经内分泌肿瘤类型的主要病理指标。常见的指标包含核分裂数、有无坏死及ki-67指数建议标注。
e.大细胞癌:
大细胞癌是一种未分化非小细胞癌,以排除性诊断方式进行确诊。
f. 肉瘤样癌:包含多形性癌、癌肉瘤和肺母细胞瘤等。
多形性癌:包含10%梭形或巨细胞成分的NSCLC;
梭形细胞癌或巨细胞癌:几乎只含有梭形或巨细胞成分;
癌肉瘤:混合肉瘤成分的NSCLC;
肺母细胞瘤:包含胎儿型腺癌及原始间充质成分的双向分化性肿瘤。
g.其他上皮源性肿瘤
胸部SMARCA4缺失未分化肿瘤:高级别恶性肿瘤,主要累及成年人胸部,表现为未分化或横纹肌样表型并伴有SMARCA4 缺失。细胞毒性化疗通常对该肿瘤无效;
NUT癌:低分化癌,有15q14的NUTM1基因重排,表达*丸睾**核蛋白(NUT)。NUT癌极具侵袭性,大多数化疗方案无效,靶向BRD4的BET小分子*制剂抑**治疗NUT癌的临床研究正在进行。
h.转移性癌
肺是全身肿瘤的常见转移部位,应注意除外转移性肿瘤,免疫组化有助于鉴别组织来源,如

细胞学标本诊断原则:
a.尽量少使用非小细胞癌非特指型(NSCC-NOS)诊断;
b.当有配对的细胞学和活组织检查标本时,应综合诊断以达到一致性;
c.肿瘤细胞或可疑肿瘤细胞的标本,均应尽可能制作细胞学蜡块;
d.细胞学标本分型不建议过于细化,仅作腺癌、鳞状细胞癌、神经内分泌癌或NSCC-NOS分型即可。
2.免疫组织化学检测
原则 :对于小活检标本谨慎使用免疫组织化学染色,以便保留组织用于治疗相关检测。
形态学不明确的肺癌 :活检标本使用 1个腺癌标志物TTF‑1和1个鳞状细胞癌标志物(P40) 可以解决绝大部分NSCLC的分型问题。
晚期NSCLC :应检测PD-L1的表达情况。
3.分子病理学检测
标本类型 :除酸处理的标本外,甲醛固定、石蜡包埋标本、细胞块和细胞涂片均适用于分子检测。所有待检测组织学和细胞学标本需经过病理医师质控,评估肿瘤类型、细胞含量、坏死率,筛选适合分子检测的组织学类型,并确保有足量肿瘤细胞提取DNA或RNA。如具备条件可进行肿瘤富集操作。
基本原则 :
a.标本常规组织学诊断后尽量保留足够组织进行分子生物学检测,根据分子分型指导治疗。晚期NSCLC组织学诊断后需保留足够组织进行分子生物学检测,根据分子分型指导治疗;
b. 含腺癌成分的NSCLC ,无论其临床特征,应常规行表皮生长因子受体(EGFR)、间变性淋巴瘤激酶(ALK)、ROS1和RET分子生物学检测。 ⅠB~Ⅲ期术后患者 建议手术病理标本行EGFR 检测。检测方法应选择经国家官方批准的试剂和平台设备,也可使用获官方批准的二代测序(next generation sequencing,NGS)检测试剂平台。组织有限和(或)不足以进行分子生物学检测时,可利用血浆游离DNA检测EGFR突变。
c. NSCLC 检测推荐必检基因为EGFR、ALK、ROS1,扩展基因为BRAFV600E突变、MET扩增和MET14外显子跳跃突变、人表皮生长因子受体2、KRAS、RET等。采用NGS可同时检测全部必检基因和扩展基因,也可在常规检测EGFR、ALK、ROS1基因阴性之后,再应用NGS检测扩展基因;若组织标本不可及,可考虑利用血浆循环肿瘤DNA(ctDNA)进行检测。
d. 对于EGFR‑酪氨酸激酶*制剂抑**(TKI)耐药患者,建议二次活组织检查进行继发耐药EGFR T790M检测;对于无法获取组织的患者,可用ctDNA 行EGFRT790M检测。当ctDNA 阴性时,仍应建议患者行组织检测以明确EGFR T790M突变状态。
e.原发肿瘤和转移病灶均适于靶向驱动基因检测,液态活检也适用;
f.肿瘤免疫治疗患者的筛选方法:(1)免疫组化检测NSCLC的PD‑L1表达情况可发现 可能 对免疫治疗有效的患者。免疫组化检测PD‑L1有多种克隆号的抗体,对应不同的治疗药物,判定标准需参阅各试剂盒的使用说明,负责诊断的病理医师须通过相应的判读培训。(2)肿瘤突变负荷(tumor mutation burden,TMB)可能是预测免疫治疗效果的又一标志物。目前,在TMB检测方法及阈值的选择上还无统一的标准。
PS:1.肿瘤是三维结构,而平时的病理观察的切片是二维结构,并不能将所有肿瘤标本进行切片对肿瘤中所有成分进行定量检测,因此肿瘤的病理学亚型更多的是给肿瘤定性;而像新辅助靶向治疗中MPR的这种定量检测很难做到。
2.很多医院分子检测和病理检测在不同的科室,对于肿瘤标本较少时,两个科室的密切配合至关重要。
3.随着检测市场的不断壮大,相信基因检测技术也会进院进入医保,确保人们得到规范的检测,而不是盲目的筛查。
4.目前靶向药物的研发越来越多,但是令人不安的是很多药物出来并没有确定哪种检测方式可以更好的知道治疗,以met扩增为例,目前多个met相关*制剂抑**,但是NGS和免疫组化哪个结果更具有指导价值并没有定论,所以药品上市的前提至少应解决这一问题。而对于免疫治疗来说同样需要解决这一问题。
5.肿瘤异质性使得肿瘤治疗变得异常复杂,所以我们发现研究中的结果跟现实存在很大的差异,以EGFR突变为例,有的人可以活20年,而有的人直接是原发性耐药。所以客观看待研究结果,并不是所有人都会取得如研究一样的结果。