患者孙女士来自山东,本人和她先生均是高级知识分子,去年8月底诊断急性髓系白血病(AML),在山东省血液科最权威的医院进行全面评估和治疗。虽然初诊的全面检查并未发现明确的高危染色体或基因,但接受了一个标准剂量的化疗后白血病下降不明显,换新药联合方案再化疗一疗程后,仍然剩下37%白血病细胞,于是转到全国最权威的医院,换用新药组合方案,不幸还是没有完全缓解。
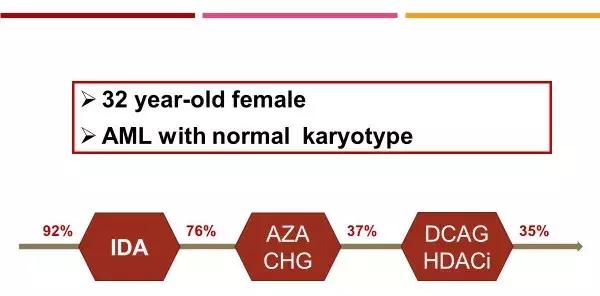
孙女士入院前治疗
这种情况放在以前,唯一的路只有挽救性移植,也就是带着肿瘤做移植。
虽然挽救性移植是难治复发AML唯一获救的途径,但是由于移植前持续存在的肿瘤,移植后仍有较高的复发风险,而移植过程中为了降低复发风险,不得不采用较标准剂量更强的预处理,导致放化疗相关的毒性如器官损伤和粘膜损伤增加,感染和移植物抗宿主病(GVHD)的风险也大大增加,从而增加移植相关死亡(TRM)。此外,移植后为了减少复发,医生会主动诱发移植物抗白血病效应(GVL),而GVL和GVHD经常相伴而存,不可避免部分患者会诱发出严重GVHD导致早期死亡或后期生活质量下降。综合因素决定了挽救性移植生存率不超过30%,花费也通常高于常规移植。
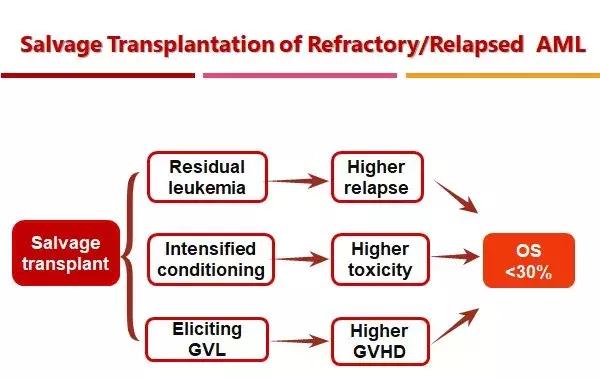
挽救性移植存在的问题
最近更新的国际骨髓移植研究中心(CIBMTR)总结报告,展示了从2006年到2016年期间13118例同胞全相合移植和21103例非亲缘移植治疗AML的结果,其中接受挽救性移植者3年生存率分别为27%和26%。
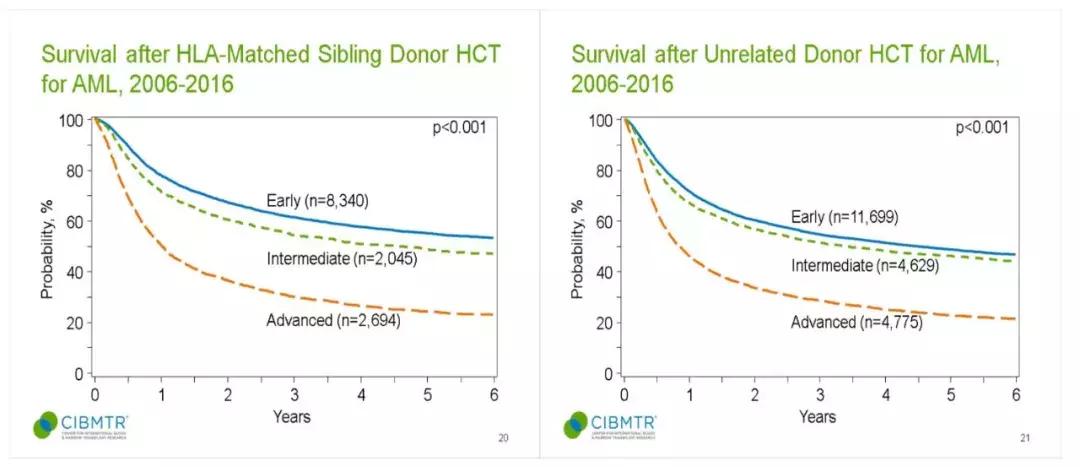
CIBMTR最新数据,挽救性移植(橙色曲线)治疗AML 3年生存仅27%和26%
患者了解到了挽救性移植的风险和困难,开始在网络上寻求帮助,了解到我们正在开展针对难治复发AML的CD33-CLL1双靶点复合CAR-T细胞治疗临床试验,并取得了较好的前期疗效。但是因为我们只是一个西部地区的小医院,在全国病人心中的位置远不及北上广的大医院,她非常担心我们处理问题的综合能力,从而犹豫不决,不知如何决策。
在一个血液病患者集中的网络平台,我们一个已故患者亲属看到了她的求助贴。虽然她的妹妹已经因挽救性移植去世,仍然对我们团队非常了解和信任,于是不厌其烦地劝孙女士来我们医院参加临床试验。经过一个多月的平衡和纠结,这对八零后夫妻终于痛下决心,抱着对未来的美好期望和将信将疑,从北京首都来到我们这个地处二线城市城乡之交的医院。
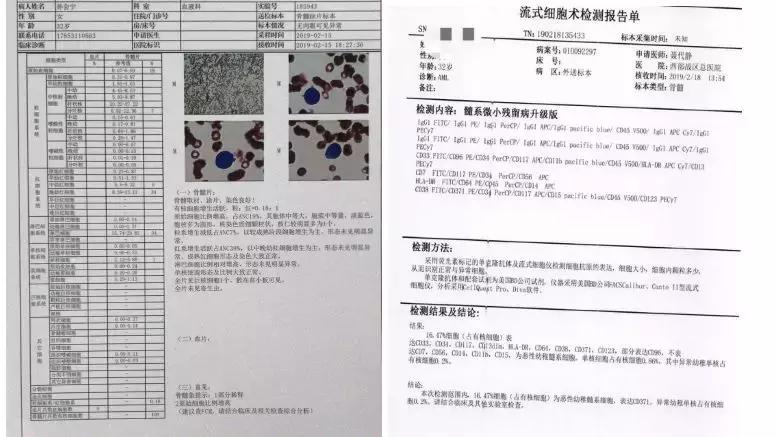
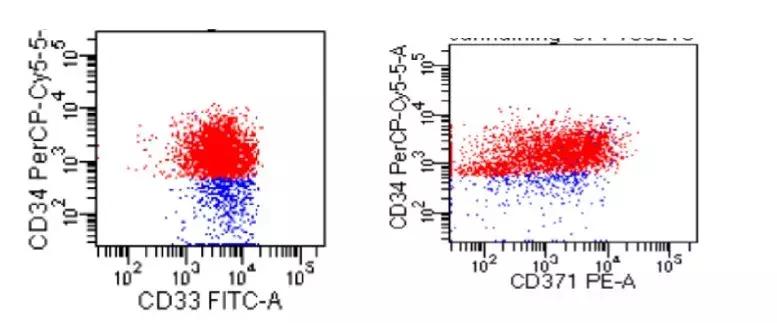
入院后我们对孙女士进行了全面的病情评估,骨髓形态显示仍然有35%的白血病细胞。免疫表型显示两个靶点中只有CD33全部表达,而CLL1(CD371)只是部分表达。由于双靶点复合CAR可以克服单靶点表达不完全的缺点,两个靶点只要任意一个表达就满足入组条件,其他条件也完全满足,于是顺利入组。
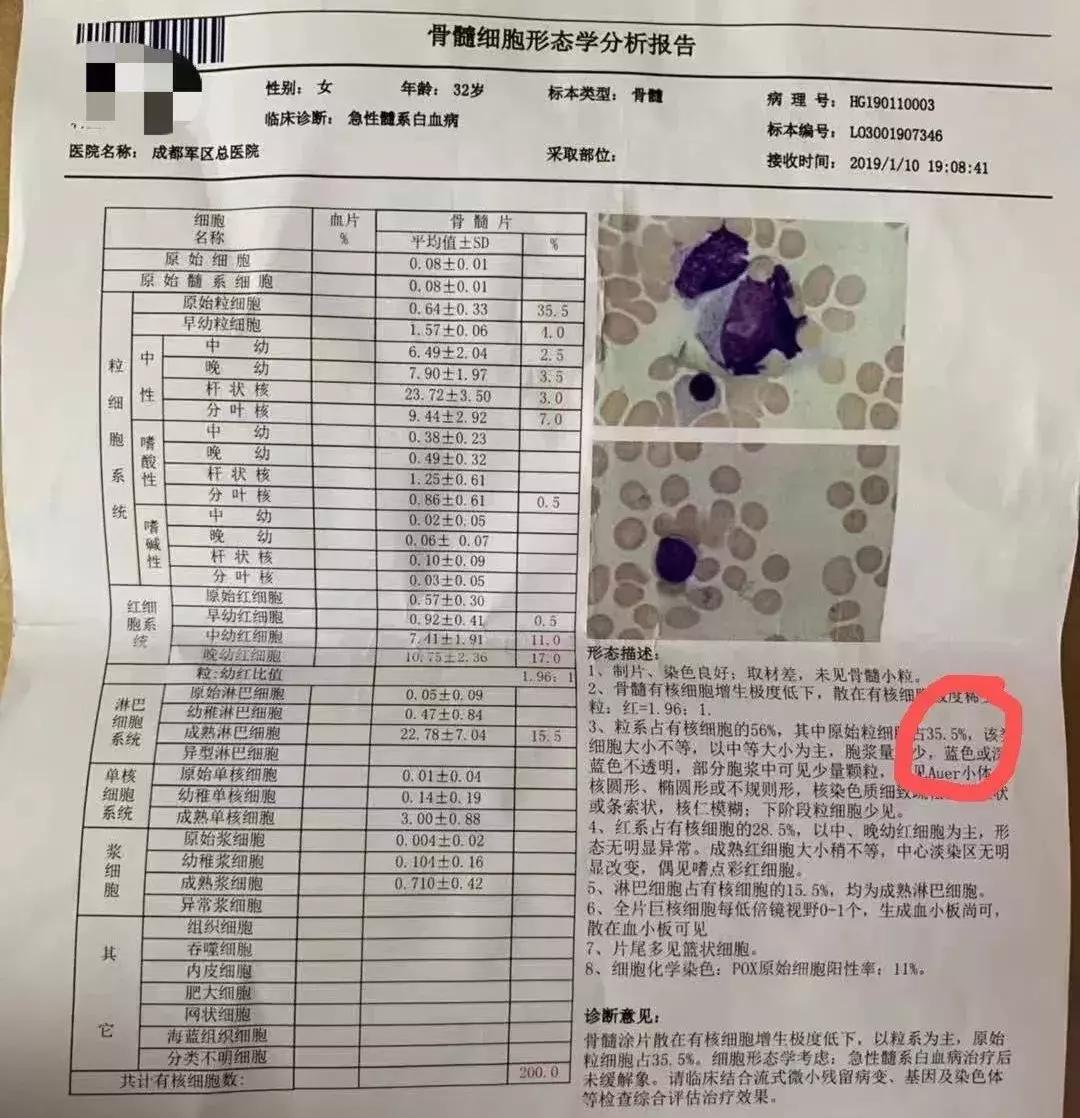
入院时的骨髓形态
经过实验室一个月的细胞培养,终于为她培养出一份合格的CAR-T细胞,体外共培养试验显示出强大的*伤杀**能力。
治疗前再次评估骨髓,在取材部分稀释情况下形态仍然有19%原始细胞,流式免疫残留检测到16.47%恶性髓系幼稚细胞。
2.28日,在经过几天简单的预处理后,我们连续两天为她输注了两个剂量的CAR-T细胞。
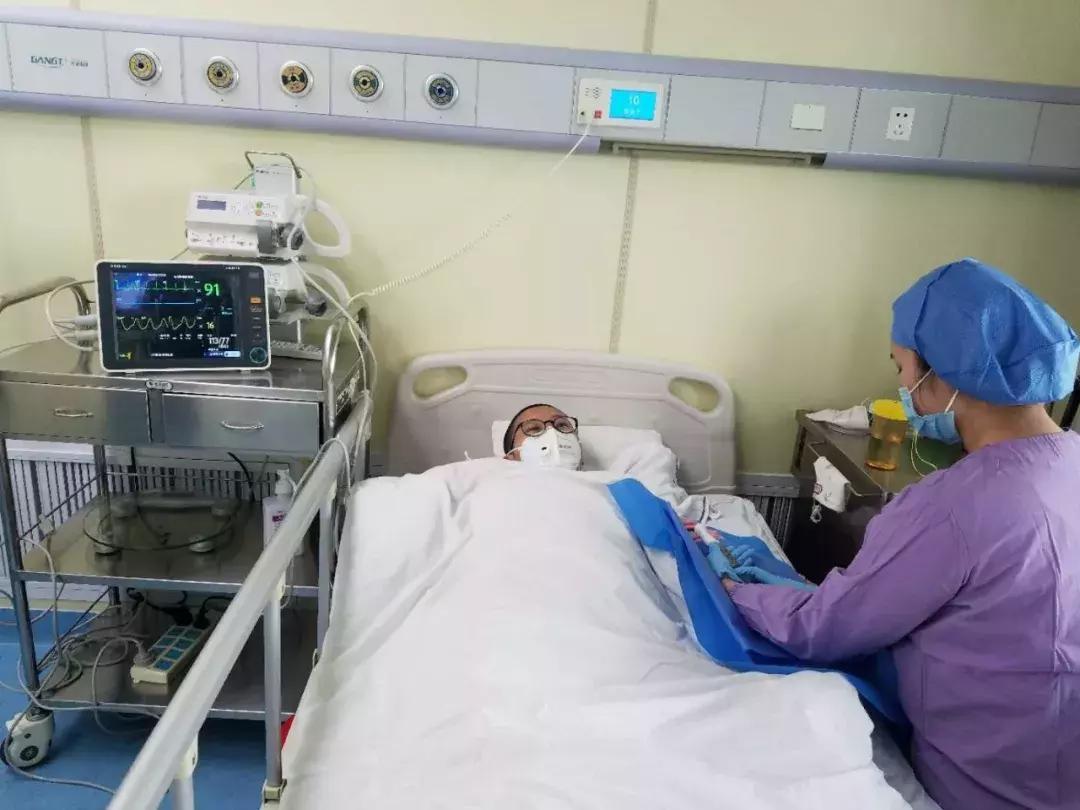
孙女士正在接受CAR-T细胞输注
细胞输注后,我们时刻做好应对并发症的准备。
我们知道,细胞因子释放综合征(CRS)是CAR-T细胞治疗后常见的并发症,其原理是CAR-T细胞*伤杀**肿瘤细胞过程中大量释放细胞因子,攻击组织器官而导致的全身性器官损伤。普通的CRS发几天烧就自己过去了,而严重CRS尤其考验临床医生应变能力,如果干预过早,会影响CAR-T细胞的扩增,从而影响疗效和持久性,而干预稍微延迟,则很快会出现翻天覆地的病情变化,很可能短期内病情迅速恶化,甚至死亡。平衡活性和风险,则需要医生有丰富的临床经验以及一定的胆识和担当。
和既往接受髓系CAR-T治疗的患者不同,孙女士CRS比任何人都来得更早更凶猛。在输注细胞的第3天就出现发热,进行全面抗感染治疗后体温仍居高不下,随后出现细胞因子急骤升高,很快就突破了实验室的检测红线,同时伴随轻度低血压,少尿,全身水肿。由于临床表现还只是一般表现,并未出现危及生命的情况,为了让CAR-T细胞多作用一些时间,产生更深更持久的效果,我们仅仅给了简单的对症处理。
可接下来几天,我们真实体验到了什么是心惊肉跳和生死搏斗。
短短的3天,她的肺由干净透明变成了白茫茫一片,需要高流量吸氧尚能维持呼吸,以这种发展速度,很可能短期内发展为严重呼吸衰竭甚至危及生命。
一波未平一波又起,出现肺部症状的第二天,孙女士出现了神经系统的异常状况:反复癫痫发作,记忆力丧失,经常莫名其妙发脾气,把家人精心做好热腾腾的饭菜一下倒在地上,在家人眼里简直判若两人,让人哭笑不得。
实验室检查,除了细胞因子明显升高,我们在她身上还观察到了其他病人从未出现的情况—淋巴细胞(大部分是CAR-T细胞)大量增值,尽管我们已经使用了大剂量激素和免疫*制剂抑**,可是疯狂的CAR-T细胞仍然以12小时翻倍的速度快速增长!
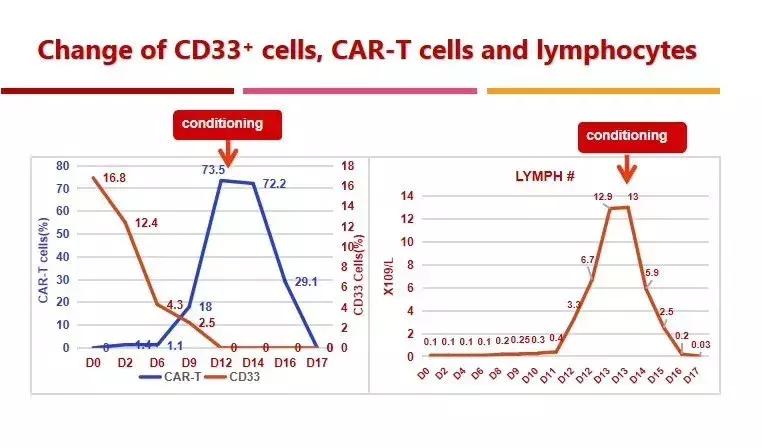
CD33+细胞,CAR-T细胞比例以及淋巴细胞数量的变化
这一切排山倒海的并发症简直给了我们一个措手不及,还好,我们有实力雄厚责任心强的医疗和护理团队,我们在前期CAR-T治疗的患者中积累了丰富的经验,经过十天单枪匹马的战斗(未请呼吸心脏及ICU会诊),孙女士终于转危为安:体温下降,水肿消失,精神恢复,间断脱离吸氧,肺部CT恢复了干净透明。
在判断CAR-T细胞反应的时间足够后,我们分两个时间点在两个不同部位的为她进行了骨髓穿刺,显微镜下只看到大量的淋巴细胞,几乎未见任何阶段的造血细胞和肿瘤细胞,两家单位的流式细胞检测均达到了微小残留白血病阴性。

治疗后的两次微小残留白血病检测结果均阴性
接下来我们须尽快用异基因造血干细胞移植挽救被CAR-T细胞清除的造血。
由于CD33-CLL1双靶点cCAR除了靶向白血病细胞,还可以靶向髓系造血细胞,我们推测,该CAR-T细胞治疗还有一定程度的清髓作用,可以在后续的移植中减轻移植预处理的强度。这个理念在前面两个接受双靶点CAR-T的病人进行了尝试并获得了成功:首例髓系CarT 治疗难治型CML桥接非清髓移植半年,髓系双靶点复合CAR-T再传喜讯。
由于孙女士体内出现的反应更强烈,且出现CAR-T明显扩增,我们推测,她体内的CAR-T细胞清髓作用应该更彻底,因此在前两例患者移植预处理剂量基础上,我们又大胆地进行了减量。
虽然供者是中年的姐姐,HLA配型只是单倍体相合,我们仅采用单纯的外周血作为干细胞来源,采集到的干细胞数量也明显低于平均线,但是在植入问题上却丝毫没让我们操心。在移植后第8天,白细胞就开始蠢蠢欲动,第9天,就达到了完全植入标准,早于其他患者的平均水平,第11天,外周血T细胞就达到100%嵌合,这是恶性病的非清髓移植比较难见到的!
而其他接受单倍体移植患者出现的常见问题,如预处理后的粘膜损伤,免疫低下期的病毒血症,细菌真菌感染,膀胱炎肠炎等,均没有一天困扰她,甚至连最常见的移植后发热都未曾光顾,让她轻松快乐地度过了移植后最艰难的第一个月。一个月后只发生了轻度的GVHD,经过药物治疗后很快控制。
移植后40多天,发生了一件让所有人惊喜的事情:在没有任何药物作用下,孙女士自己来了月经,这是其他骨髓移植的年轻女白血病患者未出现过的现象!
为了搞清是真月经还是异常子宫出血,我们特地给她查了一个性激素水平,并请教了妇科专家,被告知的确是真月经而不是子宫异常出血!
我们知道,高危白血病患者为了降低复发率,最好接受清髓移植,而无论放疗清髓还是药物清髓,均会导致生育损伤,尤其是成年女性,90%以上会产生不可逆的卵巢功能受损,激素达绝经期水平,无法再生育,且需要长期激素替代治疗。年轻女患者为了保命,往往不得不作出生活质量上甚至家庭的牺牲。
孙女士因为接受的非清髓预处理,减少了对卵巢的损伤,才如此迅速地恢复了月经,保留了生育功能(妇科专家提示:FSH大于25提示卵巢功能不全,大于40ng/ml提示卵巢功能衰竭。),她的FSH 18(对比另一清髓患者116)在正常水平。

孙女士和另一清髓移植患者雌激素水平对照
移植后我们为她进行了两次原发病评估以及供受者嵌合的检测,均显示骨髓微小残留白血病阴性,T细胞嵌合100%供者型,表明持续保留无白血病且稳定植入。
出院前的残留及嵌合检测报告
短短的3个月,孙女士夫妻的心态也发生了巨大变化,从一开始的半信半疑,纠结观望,到把生命交给我们和我们并肩作战,最后对我们团队由衷地崇拜和佩服,成为我们的铁杆粉丝,四面八方为我们介绍病人。

治疗后孙女士再次在网络平台谈自己的就医体会
经历了CAR-T治疗以及骨髓移植九九八十一天的战斗,孙女士终于盼来了出院的日子,出院当天要求和我们合影留恋,体贴周到的丈夫在朋友圈里用短短的文字表达了这八十多天的不易和对我们的感激。
出院当天孙女士丈夫的朋友圈
孙女士治疗的成功再次让我们信心倍增,积累了更多的经验,让我们的治疗体系更加成熟,处理并发症也更得心应手,为以后救治更多的患者创造了条件。
用低毒方式治愈白血病,达到高质量生存,将是血液科医生和科研工作者的终极目标,为了达到这个目标,我们会继续努力!
- end -
