在射血分数降低的心力衰竭(HFrEF)患者中,心脏性猝死(SCD)是重要的死亡原因,占30%–50%。收缩功能障碍是心脏性猝死的主要危险因素。了解HFrEF猝死背后的原因具有重要的临床意义,但其具体的发生机制目前还不明确。近日,美国贝勒大学医学中心的Milton Packer博士在European Heart Journal发表了一篇综述,对HFrEF患者心脏骤停的机制进行了讨论,并提出了新的观点。
医脉通编译整理,未经授权请勿转载。
心力衰竭与心脏性猝死
心脏性猝死定义为在出现新的心脏症状后1小时内死亡,用以区别没有已知心脏病的普通人群的猝死事件。但这种方法不适用于已确诊且症状持续的HFrEF患者。当HFrEF患者的症状近期没有恶化,且无法确定引起心脏骤停的其他原因,则可认定为猝死。因此,HFrEF患者猝死的特征不是突然发生,而是意外发生。
大型试验中的裁决委员会认为,对于因HFrEF而预期寿命极为有限的患者,不适用猝死。只有在预期患者可以存活数月或数年的情况下,才能确定是否会猝死。如果死亡是预料之中的,那么死亡可以归因于已经存在的机制。相反,如果死亡是意料之外的,就会假定出现了一种新的机制,但这在临床上很少见。
冠脉缺血事件会导致心衰患者猝死吗?
三十年前,猝死常归因于急性冠状动脉栓塞。猝死HFrEF患者的尸检表明,急性血栓栓塞可能是最终的触发因素。如果是这样,那么,如何避免斑块破裂或血栓栓塞的发生,应是临床医生比较关注的问题。然而,HFrEF相关的临床试验显示,使用他汀类药物稳定斑块或应用阿司匹林或口服抗凝药预防冠脉血栓形成并不能降低猝死风险(表1)。冠脉血运重建降低了新发心肌梗死的风险,但带来的猝死相关获益甚微,且需要数年的时间才显现出来。因此,冠脉血栓形成在HFrEF猝死发生中的作用很小。
表1 药物、器械和手术干预对左室收缩功能不全患者猝死风险的影响

备注:ACEI,血管紧张素转化酶*制剂抑**;CRT,心脏再同步治疗;HFrEF,射血分数降低心衰;ICD,植入式心脏复律除颤器;LVD,左心功能不全。
与急性缺血无关的室性心动过速是猝死的机制吗?
室性心动过速和房颤是HFrEF患者重要的终末心律失常类型,可以通过ICD来防止猝死(表1)。尽管非缺血性心肌病的风险降低幅度要小于缺血性心肌病(40%-50% vs 60%-70%),但ICD对前者的获益表明,室性心动过速可在无冠脉疾病或急性闭塞的情况下导致猝死的发生。
如果室性心动过速在猝死原因中所占比例很大,则用ICD来预防猝死可带来全因死亡率的降低。然而,相关研究显示,ICD植入在那些有进展性症状或共病的患者中并未带来预期的获益。相反,在症状轻微或终末器官功能不全的患者中,ICD降低了全因死亡率。更重要的是,临床试验中30%-70%的HFrEF患者的猝死不能通过ICD预防,且随着心功能从II级发展到III级,ICD可预防的猝死比例从60%-70%下降到25%-40%(表1)。
急性机械衰竭是猝死的机制吗?
猝死发生期间的心电图监测显示,许多HFrEF患者猝死时没有室性心动过速。在40%~60%的心脏骤停中,心电图在死亡前和死亡时表现为电机械分离、心脏停搏或末期缓慢性心律失常。这些发现在非缺血性心肌病患者中尤其常见,尤其是那些有症状的患者。器械并不能阻止这些终末事件,这反映了突发的心脏机械事件可能是心脏骤停的直接原因。
有趣的是,即使心电图显示室性心动过速或房颤,急性收缩衰竭也可能是猝死的潜在机制。在一些植入ICD的患者中,室性心动过速在反复放电后立即复发或持续存在。急性机械衰竭是循环支持突然停止的原因;观察到的快速性心律失常是一种附带现象。这些事件在临床上表现为ICD无法预防的猝死。
心室重构的自组织临界性和级联衰竭
重构过程的特点是心肌细胞的缓慢丢失,心室壁的逐渐拉伸和心肌纤维化的逐渐积累。但大多数医生们并不认为这种缓慢的渐进过程会突然终止,而是认为猝死需要一种触发机制。
自组织临界性是一个复杂系统的属性,在这个系统中,由于元素之间微妙的相互依赖,小事件可触发大灾难。近来,自组织临界的概念也被用于了解生物医学事件,如蛋白质与蛋白质间的相互作用、癌症、神经退行性疾病、遗传和代谢级联,以及细胞和机体衰亡等。
HFrEF患者的心室重构过程是一个高度脆弱相互依赖的自组织系统。心室心肌的“自组织临界状态”依赖于对心肌细胞压力和拉伸的复杂适应,这种适应可能会突然终止(“级联衰竭”),从而导致在没有新的触发事件的情况下发生急性循环衰竭(即猝死)。严重心室重构的级联衰竭可以通过电的方式(如室性心动过速)或机械的方式(如心脏停搏、缓慢性心律失常或电机械分离)表现出来。尽管ICD反复放电,但室性心动过速依然持续存在,也反映了级联机械衰竭。由于这些节律与机械活动无关,ICD无法防止这一致命后果。
心肌纤维化和几何结构的有害变化与内源性神经激素系统(去甲肾上腺素、血管紧张素II、醛固酮和中性溶酶)的激活有关。这种作用可能解释了各种神经激素拮抗剂在梗死后左心功能不全(LVD)或HFrEF患者中将猝死风险降低20-40%的能力(表1)。有趣的是,β受体阻滞剂降低猝死风险的作用大于血管紧张素转化酶*制剂抑**(ACEI)的作用,这可能是因为它们对心室重构的作用更为明显。盐皮质激素受体拮抗剂在猝死中增加的获益可能与其抗纤维化作用有关,在接受β受体阻滞剂的患者中尤为明显(图1)。
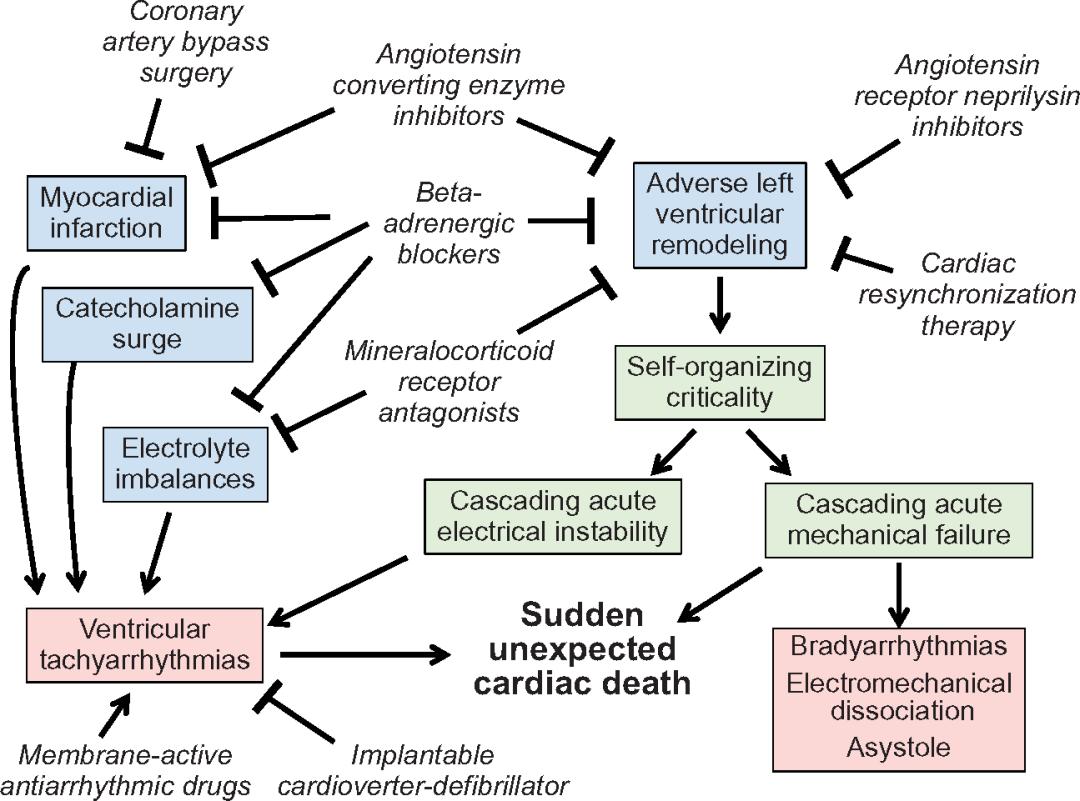
图1 药物、器械和手术降低慢性心衰猝死风险的机制
逆转重构可防止急性级联机械衰竭
HFrEF患者的大规模试验中有关心脏再同步和中性溶酶抑制的最新经验支持心室重构是级联衰竭和猝死的直接原因这一观点。
首先,心脏再同步在不影响神经激素系统的情况下对心室重构具有显著益处。当心脏再同步引起显著的逆向重构时,用于急性电级联反应的底物会减少(图1); 无ICD的患者猝死风险降低约50%,主要与心室容量明显减少的患者,其致命性室性快速性心律失常的发生率降低有关(表1)。相比之下,对于症状严重、心脏持续扩张和纤维化的患者,在心脏再同步化后,猝死的风险仍然很高,而且ICD并不能降低猝死风险。
其次,使用沙库巴曲/缬沙坦治疗HFrEF患者的研究支持了心室重构与导致猝死的急性机械衰竭之间的关系。抑制脑啡肽酶对心室重构具有良好的作用,可以减少导致室性心动过速的底物(图1)。沙库巴曲/缬沙坦降低心脏性猝死风险的作用在既往植入ICD的患者中最为显著(风险降低>50%)(表1)。
在过去的10-15年中,HFrEF的猝死发生率一直在下降,与此同时,左心室的大小也在减小。这种下降的发生与ICD的使用无关,但与神经激素拮抗剂和心脏再同步治疗的使用增加有关。
结论
一些病理生理机制(如冠脉血栓性缺血事件、激素-电解质失衡)可以引发猝死,但最常见的,心脏骤停是由心室重构和纤维化的急性电或机械衰竭引起的。神经激素拮抗剂和心脏再同步的抗重构和抗纤维化作用可以预防猝死,无论是否植入ICD。“自组织临界性”理论表明,在心室重构最容易逆转的疾病早期进行治疗,对延长慢性心衰患者的寿命可能会产生重大影响。
文献索引:Milton Packer. What causes sudden death in patients with chronic heart failure and a reduced ejection fraction? European Heart Journal. 2020; 41(18): 1757–63.