二次电池的分析思路

(2017· 全国卷 Ⅲ ) 全固态锂硫电池能量密度 高、成本低,其工作原理如图所示,其中电 极 a 常用掺有石墨烯的 S8 材料,电池反应 为 16Li + x S8==8Li2Sx(2 ≤ x ≤ 8) 。下列说法错误的是 ( D )
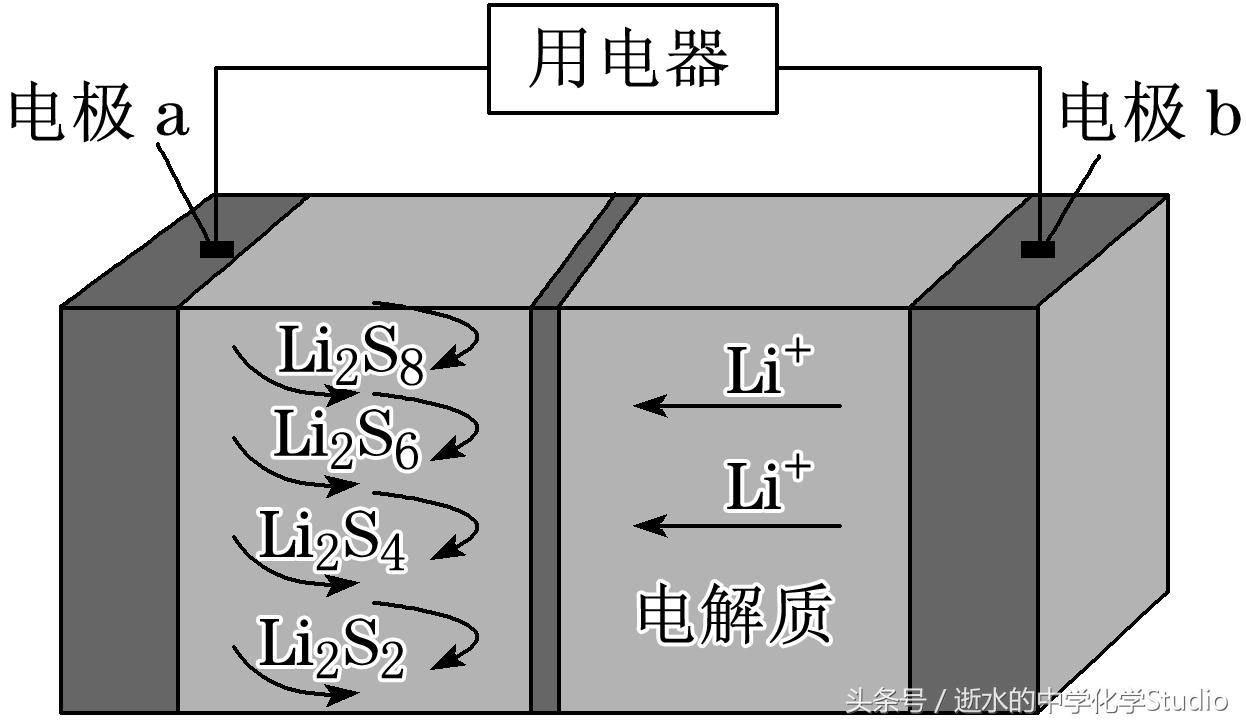
A .电池工作时,正极可发生反应: 2Li2S6 + 2Li + + 2e - = =3Li2S4
B .电池工作时,外电路中流过 0.02 mol 电子,负极材料减重 0.14 g
C .石墨烯的作用主要是提高电极 a 的导电性
D.电池充电时间越长,电池中Li2S2的量越多
解析:
A项,原电池工作时,正极发生一系列得电子的还原反应,即:Li2S8→Li2S6→Li2S4→Li2S2,其中可能有2Li2S6+2Li++2e-===3Li2S4,正确;
B 项,该电池工作时,每转移 0.02 mol 电子,负极有 0.02 mol Li( 质量为 0.14 g ) 被氧化为 Li + ,则负极质量减少 0.14 g ,正确;
C 项,石墨烯能导电,利用石墨烯作电极,可提高电极 a 的导电性,正确;
D项,充电过程中,Li2S2的量逐渐减少,当电池充满电时,相当于达到平衡状态,电池中Li2S2的量趋于不变,故不是电池充电时间越长,电池中Li2S2的量越多,错误。

(2016· 全国卷 Ⅲ ) 锌-空气燃料电池可用作电动车动力电源,电池的电解质溶液为 KOH 溶液,反应为 2Zn + O2 + 4OH - + 2H2O===2Zn(OH) 。下列说法正确的是 ( C )
A .充电时,电解质溶液中 K + 向阳极移动
B .充电时,电解质溶液中 c (OH - ) 逐渐减小
C .放电时,负极反应为 Zn + 4OH - - 2e - == =Zn(OH)
D.放电时,电路中通过2 mol电子,消耗氧气22.4 L(标准状况)
解析:
A项,充电时装置为电解池,溶液中的阳离子向阴极移动,错误;
B项,充电时的总反应为放电时的逆反应:2Zn(OH) ==2Zn+O2+4OH-+2H2O,c(OH-)逐渐增大,错误;
C项,放电时负极失电子发生氧化反应,由放电时的总反应可知,负极反应式为Zn+4OH--2e-===Zn(OH) ,正确;
D项,由放电时的总反应可知,电路中通过2 mol电子时,消耗0.5 mol O2,其体积为11.2 L(标准状况),错误。

(2016· 四川高考 ) 某电动汽车配载一种可充放电的锂离子电池,放电时电池总反应为 Li1 - x CoO2 + LixC6===LiCoO2 + C6(x < 1) 。下列关于该电池的说法不正确的是 ( C )
A .放电时, Li + 在电解质中由负极向正极迁移
B .放电时,负极的电极反应式为 LixC6 - x e - == =xLi + + C6
C .充电时,若转移 1 mol e - ,石墨 (C6) 电极将增重 7x g
D .充电时,阳极的电极反应式为 LiCoO2 - x e - == =Li1 - x CoO2 +xLi+
解析:
A项,原电池中阳离子由负极向正极迁移,正确;
B项,放电时,负极发生氧化反应,电极反应式为LixC6-xe-===xLi++C6,正确;
C项,充电时,若转移1 mol 电子,石墨电极质量将增重7 g,错误;
D项,充电时阳极发生氧化反应,电极反应式为LiCoO2-xe-===Li1-xCoO2+xLi+,正确。