Photofrin®光动力疗法即使用Photofrin®进行光动力治疗的方法,这种方法是使用光敏剂Photofrin®、大功率半导体激光治疗仪DIOMED 630 PDT Laser和OPTIGUIDE®光纤来进行的。Photofrin®(Porfimer Sodium)是一种用于肿瘤光动力治疗的光敏剂,是FDA目前批准的唯一可应用于恶性肿瘤治疗的光敏剂。
Photofrin®为红褐色*干粉冻**剂,是一种从牛血中提取并进行化学改性的、以醚键或酯键连接的卟啉低聚体混合物。常温贮存,有效期5年。
该药于1984年在美国Roswell Park癌症研究所开发成功(曾用名Photofrin II,DHE),1993年在加拿大首先批准上市,其后相继在荷兰(1994)、日本(1994)美国(1995)、法国(1996)、德国(1997)等国也获政府药管部门批准。截止2016年10月,全球范围内相继已有28个国家和地区批准上市。
1998年1月,Photofrin®进入美国医疗保险与医疗补助服务中心(The Centers for Medicare and Medicaid Services,CMS)医保体系,HCPCS(Healthcare Common Procedure Coding System) 代码为:J9600。其后,Photofrin®又被英国国家药典(British National Formulary),马丁代尔大药典(Martindale)等国际权威药典收录。
2000年6月30日,DIOMED 630 PDT Laser及与其配套使用的OPTIGUIDE®光纤获得美国FDA批准,用激发Photofrin®进行肿瘤光动力治疗,这也是目前FDA唯一批准用于肿瘤光动力治疗的大功率半导体激光治疗仪及光纤。
上市23年来,由于疗效明确、品质稳定、能持续保持供应、容易贮存及运输,Photofrin®光动力疗法已治疗了大量肿瘤患者,取得了海量的临床数据,根据公开发表的文献统计,各国已批适应证和超说明书使用已超过30多种肿瘤。该疗法的安全性、有效性已得到充分证明,是全球医学界公认的用于光动力治疗的经典方法和行业标准。
二、全球各国批准情况
截止2016年10月,Photofrin®光动力疗法全球范围内已批准国家和地区有:
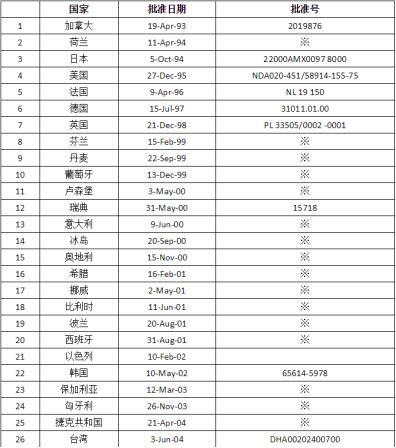

欧盟国家执行Mutual Recognition and National Procedure,上市
三、部分已批准适应证
美国
原发移行性细胞膀胱癌(孤儿药,1989年)
食管癌辅助性治疗(部分或完全性梗阻)(1996年)
微侵袭性非小细胞肺癌(不适宜手术或放疗者)(1998年)
梗阻性非小细胞肺癌的辅助治疗(1998年)
Barrett食管的不典型性增生(2003年)
胆管癌(孤儿药,2004年)
恶性胸膜间皮瘤(孤儿药,2011年)
欧洲
食管癌和肺癌的辅助治疗(法国、荷兰)(1994年)
早期肺癌的根治(德国)(1997年)
日本
早期肺癌(1997年)
浅表食管癌(1997年)
浅表胃癌(1997年)
早期宫颈癌和异性增生(1997年)
加拿大
部分梗阻性食管癌(1993年)
早期非小细胞性肺癌(1993年)
Barrett食管的不典型性增生(2003年)
韩国
晚期肺癌和食道癌(2002年)