中国杭州和绍兴,2023年5月2日--歌礼制药有限公司(香港联交所代码:1672,“歌礼”)宣布,同类首创、每日一次、口服脂肪酸合成酶(FASN)*制剂抑**ASC40(Denifanstat)治疗*疮痤**II期临床试验达到主要及关键次要终点。
ASC40是一种口服、选择性小分子FASN*制剂抑**。ASC40治疗*疮痤**的机制是:(1)通过抑制*皮人**脂细胞的脂肪酸从头合成(DNL),直接抑制面部皮脂生成;和(2)通过减少细胞因子分泌和Th17分化来抑制炎症。
该项II期研究是一项在中国开展的随机、双盲、安慰剂对照、多中心的临床试验,旨在评估ASC40治疗中度至重度*疮痤**患者的安全性和有效性。入组的180名患者被按照1:1:1:1的比例随机分配进入三个活*药性**物组和一个安慰剂对照组,并接受每日一次口服ASC40(25毫克、50毫克或75毫克)或安慰剂治疗,为期12周,其中179名患者至少服用了一次ASC40或安慰剂。
表1总结了顶线疗效数据。
表2比较了使用50毫克ASC40口服、每日一次的治疗与外用1%的clascoterone乳膏(Winlevi®),每日两次的治疗。Clascoterone是一种外用的雄激素受体*制剂抑**,于2020年8月获美国食品药品监督管理局批准上市。
表1. 口服25毫克、50毫克和75毫克ASC40,每日一次、用药12周(对比安慰剂)的主要和关键次要疗效终点(n=179)
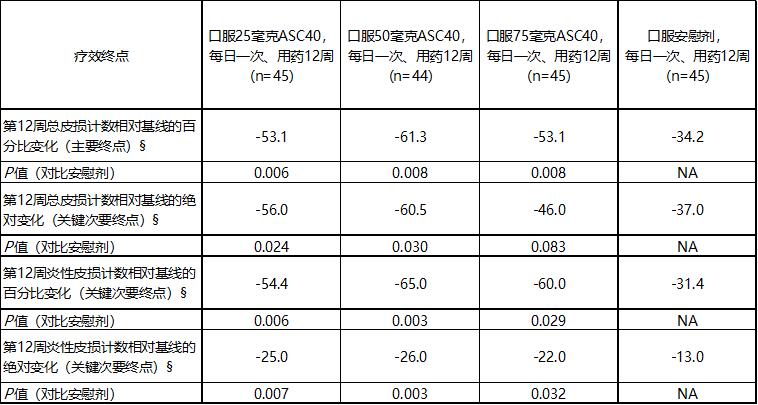
注释: § 数据为中位数。
表2. 口服50毫克ASC40,每日一次、用药12周对比外用1%的clascoterone乳膏(Winlevi® )每日两次、用药12周(非头对头比较)
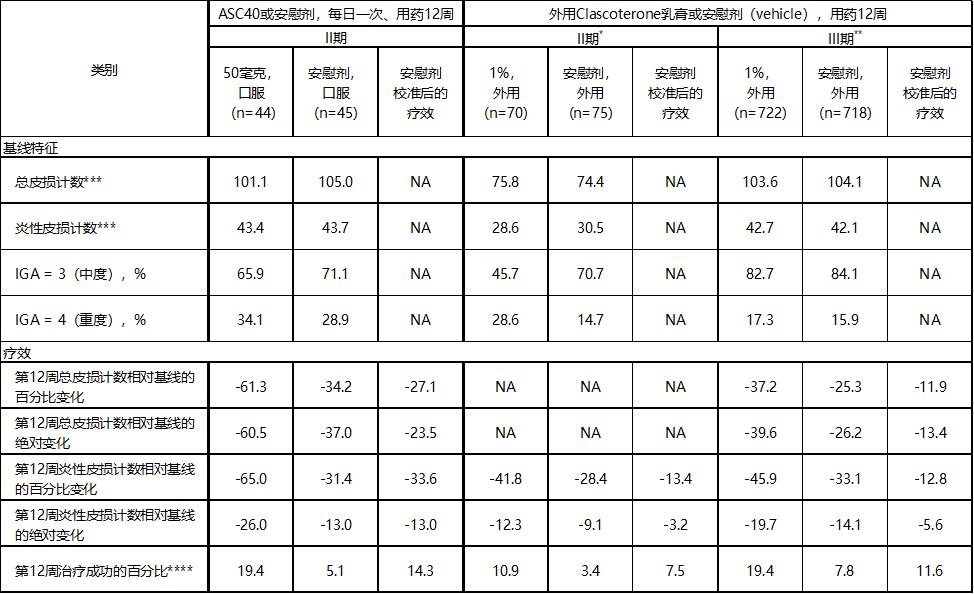
注释:
IGA:研究者整体评估。
* 表2中clascoterone乳膏(1%)的II期数据出自www.clinicaltrials.gov网站上的 NCT01631474的研究结果 。除了中度和重度*疮痤**患者外,该项 II 期临床试验还分别入组了25.7%和14.7%的轻度*疮痤**患者(IGA = 2)至clascoterone乳膏(1%)组和安慰剂组。
** 表2中clascoterone乳膏(1%)的III期数据结合或平均了发表在以下文章中的两项 III 期临床试验的数据:Hebert A, Thiboutot D, Gold L S, et al. Efficacy and Safety of Topical Clascoterone Cream, 1%, for Treatment in Patients with Facial Acne: Two Phase 3 Randomized Clinical Trials [J]. JAMA Dermatology, 2020, 156(6)。
*** 数据为平均值。
**** 治疗成功是指第12周时IGA评分较基线至少降低2分且IGA评分为0或1。
ASC40在口服12周、每日一次的所有剂量下的安全性和耐受性良好。25毫克(1级 = 28.9%;2级 = 20.0%)、50毫克(1级 = 36.4%;2级 = 11.4%)、75毫克(1级 = 44.4%;2级 = 17.8%)ASC40和安慰剂(1级 = 35.6%;2级 = 13.3%)的试验药物相关不良事件发生率相当。在所有治疗组中,与试验药物相关的最常见的不良事件是眼睛干涩,其发生率在25毫克(1级 = 17.8%;2级 = 6.6%)、50毫克(1级 = 22.7%;2级 = 2.3%)、75毫克(1级 = 15.5%;2级 = 11.1%)ASC40和安慰剂(1级 = 28.9%;2级 = 6.6%)中相似。无与ASC40相关的3级和4级不良事件,且无与ASC40相关的严重不良事件。无死亡病例报告。
根据疗效和安全性评估,口服50毫克,每日一次为III期临床试验的推荐剂量,该III期临床试验预计将于2023年下半年启动。仍在进行评估另外两种剂量是否为III期试验的剂量。
在此前开展的治疗非酒精性脂肪性肝炎(NASH)患者的IIa期临床试验中,50毫克ASC40,口服、每日一次、用药12周后,61%的患者显示出具有临床意义和统计学上显著的肝脏脂肪降低。此外,在第12周还观察到统计学上显著的相对基线的总胆固醇、低密度脂蛋白胆固醇(LDL-C)和谷丙转氨酶(ALT)/丙氨酸转氨酶(AST)的降低[1]。
*疮痤**是全球第八大常见疾病,影响全球超过6.4亿人[2]。与口服药物相比,外用疗法的依从性更低:据估计,约有30%至40%的患者不能遵医嘱完成外用治疗[3]。目前,有效的口服*疮痤**药物主要是异维A酸,其可能会导致许多严重的不良事件,如肝毒性、听力障碍和抑郁症等。ASC40有望成为同类首创、每日一次、疗效显著、患者依从性高、安全性好的口服*疮痤**药物。
复旦大学附属华山医院皮肤科主任医师、复旦大学皮肤病学研究所常务副所长、中国医师协会皮肤科医师分会副会长及ASC40中重度*疮痤**适应症II期临床试验主要研究者项蕾红教授表示 : 脂肪酸合成酶*制剂抑**ASC40是一种全新机制的同类首创候选药物,在II期临床试验中表现出了显著的疗效和良好的安全性。我希望尽快开展III期临床实验。
歌礼创始人、董事会主席兼首席执行官吴劲梓博士表示: 我为如此优异的II期临床数据感到振奋。脂肪酸合成酶抑制是治疗*疮痤**的新机制,ASC40是该机制的同类首创候选药物,歌礼再次展现了针对未满足的医疗需求开发创新药物的强大研发能力。我期待着在2023年下半年启动*疮痤**的III期临床试验。
[1] Loomba R, Mohseni R, Lucas K J, et al. TVB-2640 (FASN inhibitor) for the treatment of nonalcoholic steatohepatitis: FASCINATE-1, a randomized, placebo-controlled Ph2a trial [J]. Gastroenterology, 2021.
[2] Tan J K, Bhate K. A global perspective on the epidemiology of acne [J]. Br J Dermatol 2015, 172 Suppl 1(3-12). DOI: 10.1111/bjd.13462.
[3] Purvis CG, Balogh EA, Feldman SR. Clascoterone: How the Novel Androgen Receptor Inhibitor Fits Into the Acne Treatment Paradigm. Ann Pharmacother. 2021;55(10):1297-1299. doi:10.1177/1060028021992055.