2017年被认为是“CAR-T疗法元年”。美东时间7月12日,美国FDA肿瘤药物专家咨询委员会(ODAC)召开针对诺华(Novartis)CAR-T疗法CTL-019(tisagenlecleucel)的评估会议,最终以10:0的投票结果一致推荐批准此疗法上市,是为全球首次。按照计划,FDA预计将于10月3日前依据专家意见做出最终审批决定。FDA 的这一决定比预定的审批期限提前了 1 个月。
而在8月30日,我们迎来了喜大普奔、激动人心的历史时刻。FDA已经批准诺华的CAR-T疗法,用来治疗罹患B细胞前体急性淋巴性白血病(ALL),且病情难治,或出现二次及以上复发的25岁以下患者。此外在CAR-T产品的定价方面,诺华最近给出了47.5万美元的高昂定价范围,这是参照美国骨髓移植的费用而制定的价格。
海外相关概念股已涨上了天
值得一提的是,六岁的艾米丽·怀特海德(Emily Whitehead)是全球第一位接受试验性 CAR-T 疗法的儿童患者。2012年生命垂危之际,她接受了CAR-T疗法。 而现在她不仅完全痊愈,现在已经茁壮成长到 12 岁了。而艾米丽所接受的就是诺华的这款 CTL019 疗法产品。

另外,就在前几天另一则新闻也刷屏业界,世界领先的美国生化制药公司 Gilead 宣布欲投资 119 亿美元收购 Kite,双方董事会已经达成最终收购协议,吉利德将以每股180美元的现金价格收购Kite,溢价29%。该项交易金额约为119亿美元,预计整个交易将在2017年第四季度完成。当天Kite公司股价大涨28%,受Kite公司被收购刺激,另一个CAR-T疗法巨头Juno Therapeutics当天股价也大涨20%。
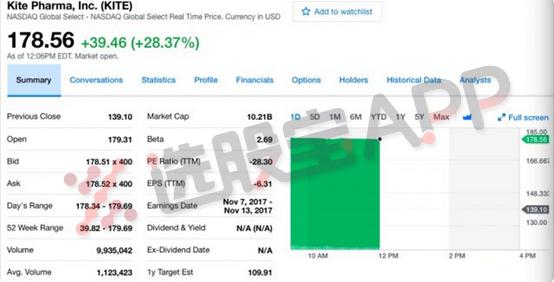

美国时间周一早 9:19 分,美股开盘前,Gilead 股价上涨 0.6%至 74.21 美元。Kite 公司跳涨至 179.69 美元。Kite 被收购的消息传出后带动同行Juno Therapeutics制药公司股价飙升。
目前,Kite所开发的CAR-T疗法(KTE-C19)正处于FDA审评阶段,PDUFA预定审批期限是2017年11月29日。之前,Kite Pharma原本在与诺华的竞争中处于领先地位,然而Kite Pharma的KTE-C19在4月底出现1例患者死亡。
原本, KTE-C19预期于11月29日获批,然而这次FDA不对axicabtageneciloleucel进行ODAC审评将加快最终审批决定,这意味着FDA对CAR-T产品的认可,将加速CAR-T产品的上市。
一般拥有核心专利项目的创新药公司在纳斯达克单独上市,经历上市融资,研发,又被医药巨头高价收购时,都说明公司项目产品已接近成熟,已达到投放市场的审批条件。因为医药巨头们都相对成熟强大的运营,市场渠道优势。能够快速将产品投放市场,产生现金流,巩固竞争优势。这也从一个侧面印证了kite的CAR-T治疗项目已快要投放市场,业内预期信心强劲。
什么是 CAR-T ?
CAR-T,全称是 Chimeric Antigen Receptor T-Cell Immunotherapy,嵌合抗原受体 T 细胞免疫疗法。这是一个出现了很多年,但是近几年才被改良应用到临床上的新型细胞疗法。和其它免疫疗法类似,它的基本原理就是利用病人自身的免疫细胞来清除癌细胞,但是不同的是,这是一种细胞疗法,而不是一种药。
它在急性白血病和非霍奇金淋巴瘤的治疗上有着显著的疗效,被认为是最有前景的肿瘤治疗方式之一。
CAR-T 首次临床应用的报道是 2008 年,在 Nature medicine 上报道了使用 CAR-T 细胞治疗 11 例儿童成纤维神经瘤,6 例出现好转。
2016 年 4 月 26 日,美国著名癌症研究中心 Fred Hutchinson Cancer Research Center(弗雷德·哈金森癌症研究中心)的报道更加增长人们的信心。29 名晚期急性淋巴细胞白血病(ALL)患者,经过 CAR-T 治疗,其中 27 名病情完全缓解,缓解率高达 93% 。这个实验数据结果让业界震惊,他们的临床试验结果刊登在著名临床研究杂志 JCI 上。
CAR-T 的治疗步骤:

- 从癌症病人身上分离免疫 T 细胞;
- 利用基因工程技术,通过逆转录病毒和慢病毒载体、转座系统(如 SB 转座系统)或直接将 mRNA 转导到 T 细胞内,使 T 细胞表面表达嵌和抗原受体(CAR),即成为 CAR-T 细胞;
- 体外扩增 CAR-T 细胞,一般一个病人需要几十亿,乃至上百亿个 CAR-T 细胞(体型越大需要细胞越多);
- 把扩增好的CAR-T细胞输回病人体内;
- 严密监控病人,尤其是控制前几天身体的剧烈反应。
AR-T 的靶向免疫疗法的原理,就好比*警武**在繁忙的大都市里试图清除叛乱的暴徒和他们的据点,在这里,CAR-T 就是*警武**,暴徒就是癌细胞,据点就是肿瘤所在的微环境,而繁忙的大都市就是我们的身体。首先,想要在繁忙的大都市里找到暴徒,需要的就是识别这些暴徒,也就是我们说的靶向。在 CAR-T 里,我们让 T 细胞通过 CAR 来识别癌细胞表面表达的特定的结构(抗原)。
理想情况下,这个靶点需要是一个只在癌细胞表面表达(或高度表达),而在其它正常的体细胞上是不表达(或者表达非常低)(理论上找到一个靶点已经可以是一个专利,你可以拿这个靶点去做抗体药物,进行临床测试,很有机会可以出任 CEO ,迎娶白富美,走上成功的巅峰了)。
为何CAR-T 在目前技术基础上只对血液肿瘤治疗有突破?
CAR-T 细胞免疫疗法目前主要应用于血液肿瘤,如急性白血病和非霍奇金淋巴瘤。之所以血液肿瘤可以被 CAR-T 治愈,有一个原因就是被 CAR 改造的 T 细胞发挥作用的地方是病人体内的淋巴和血管中,这些地方都是血液细胞经常所处的环境,有足够的资源供它们存活和攻击暴徒。
在血液肿瘤中,就像*警武**对付那些在高速公路上移动的暴徒(血液癌),*警武**可以进行追逐,封路甚至直升机追寻等等方法捉到他们。而在实体瘤中,癌症处在特别的微环境中,这样让 CAR-T 有些束手无策。在实体癌中,暴徒们都藏在了据点里,易守难攻。
CART-T疗法全球竞争格局:
诺华、Kite 、Juno,:三巨头领跑全球 CAR-T 治疗:

诺华:主打产品 CTL019成为第一个上市的 CAR-T 产品,诺华成立于 1996 年,是一家国际性制药及生物技术公司,由 Ciba-Geigy 和 Sandoz 合并而成,总部位于瑞士巴塞尔。2012 年,诺华与 CAR-T 细胞治疗的领头羊-宾夕法尼亚大学合作,斥资 2000 万美元建立实验室开始了 CAR-T 的研发。诺华目前在 CAR-T 治疗领域主打产品为 CTL019(Tisagenlecleucel-T)已通过FDA审批。
Kite Pharma:针对 NHL 的 KTE-C19 已提交 BLA 申请,有望紧随 CTL019 上市,Kite 制药成立于 2009 年,是一家致力于新型肿瘤免疫治疗的生物制药公司,总部位于加州 Santa Monica。Kite 制药是全球唯一拥有美国国立卫生研究院(NIH)许可的药物公司,与美国国家癌症研究所(NCI)与 NIH 都建立了广泛的合作关系。Kite公司主要有 CAR-T 与 TCR-T 两个系列产品,均处于临床研发阶段。2016 年 Kite 将主打产品 KTE-C19 的日本市场权利转让给第一三共,并在2017 年初与复星医药成立合资公司——复兴凯特生物。
Juno :“火箭头坠落”,首推产品 JCAR015 被终止:Juno 成立于 2013 年,是由 Fred Hutchinson 癌症中心、斯隆-凯特琳癌症中心以及西雅图儿童研究机构合作成立的生物制药企业,总部位于美国华盛顿州西雅图。公司最初以 CD19 靶向的 CAR-T 产品有三个:JCAR014、JCAR015 与 JCAR017,主要针对血液肿瘤,原本进展最快、有希望成为 Juno 第一个上市的 CAR-T 产品 JCAR015,因治疗过程中出现多名患者脑水肿死亡被 FDA 叫停, 2017 年 3 月 Juno 正式宣布终止 JCAR015 的Ⅱ期临床试验。目前 Juno 进展最快的品种为 JTCR016,该产品已开展针对急性髓性白血病、非小细胞肺癌、间皮瘤三个适应症的Ⅰ/Ⅱ期临床试验。2016 年 4 月,药明康德与 Juno 合作成立上海药明巨诺生物科技有限公司.
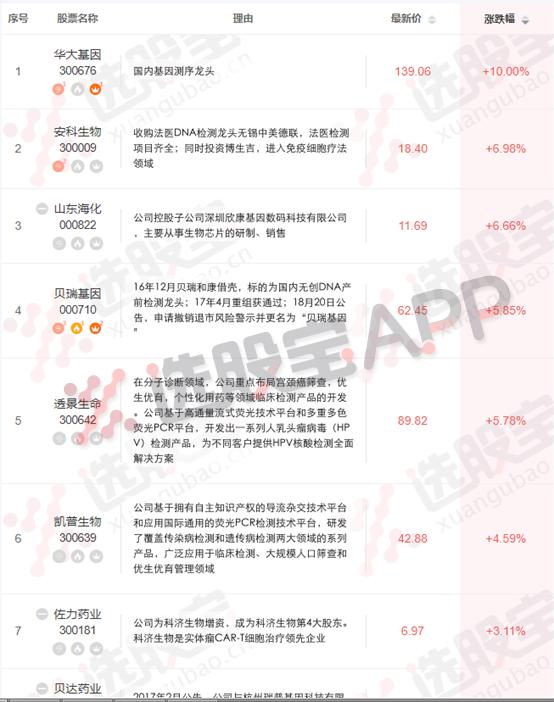
本次诺华首款癌症治疗方案获FDA审批,也让国内相关板块和概念股走势活跃。截止2017年8月31日发稿前,国内基因龙头华大基因,贝瑞基因,精准医疗概念龙头安科生物,创新药龙头贝达生物都有不俗涨幅,走势活跃。
更多基因测序主题标的,参见选股宝主题库APP(https://xuangubao.cn/theme/129)
*免责声明:文章内容仅供参考,不构成投资建议