患者为男性, 64 岁,2019 年 06 月因腹胀 6 天、肛门停止排气排便 3 天在外 院就诊,CT 检查提示空肠恶性肿瘤及双侧肾上腺占位。2019 年 06 月 25 日在首 都医科大学附属北京世纪坛医院全麻行腹腔镜下小肠部分切除术,术后病理示:小肠低分化癌,淋巴结转移灶符合低分化腺癌。(部分小肠及肿瘤)结节样肿瘤 组织,瘤细胞圆形、卵圆形,胞浆红染,核重度异型,部分核偏位,核仁明显, 核分裂易见。呈实性片状排列,伴大片坏死,瘤组织累及黏膜下层、肌层及浆膜 层,局部累及黏膜层;两端切缘未见肿瘤,可见脉管癌栓,未见神经侵犯;肠周 淋巴结转移性肿瘤(2/12),(肠系膜淋巴结)淋巴结未见转移性肿瘤(0/1);免 疫组化结果:(B4)CK(+), VIM(+), CD117(-), CD34(-), Dog-1(-), SDHB(+), SMA(-), Desmin(-), S-100(-), SOX-10(-), HMB45(-), MelanA(-), Myoglobin( 部 分 +), Ki-67(90%), P53( 个别阳 性 ), PD-L1(SP142)(TC 70%, IC5%+), PD-1(UMAB199)(个别阳性), CD21(-)。基因检测:KRAS, EP300, SMARCA4, KEAP1, GEN1, TGFBR2, WRN, SLX4, STK11 基因存在有意突变;MSI 状态:MSS;肿瘤突变负荷 17.4mut/Mb。术后恢复可,现来我院继续治疗。个人史、既往史、家族史无特殊。2019 年 7 月 22 日术后复查 CT 可见双侧肾上腺转移,腹膜后淋巴结多发转移。
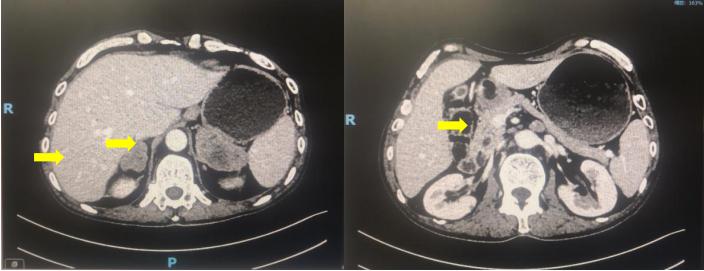
诊断
主要诊断:小肠腺癌,病理分期:pT3N1M1(IV 期),UICC 第 8 版分期。
一线方案选择
根据 NCCN 治疗指南及临床研究证据,在 2019 年 07 月 30 日至 2019 年 11 月 18 日给予患者 6 周期 Xelox 方案(奥沙利铂+卡培他滨)化疗。治疗 6 周期后患者出现 II 度奥沙利铂相关周围神经毒性,其他不良反应包括轻度食欲下降、乏 力伴头晕。
疗效评估 :一线 Xelox 方案化疗 2 周期后肾上腺肿瘤明显退缩,腹膜后淋巴结明显缩小,疗效评估(PR),一线方案治疗 6 周期后疗效评价(SD),肿瘤稍增大;一线治疗 4 周期后血 CA199 出现回升,6 周期治疗后 CA199 明显升高。
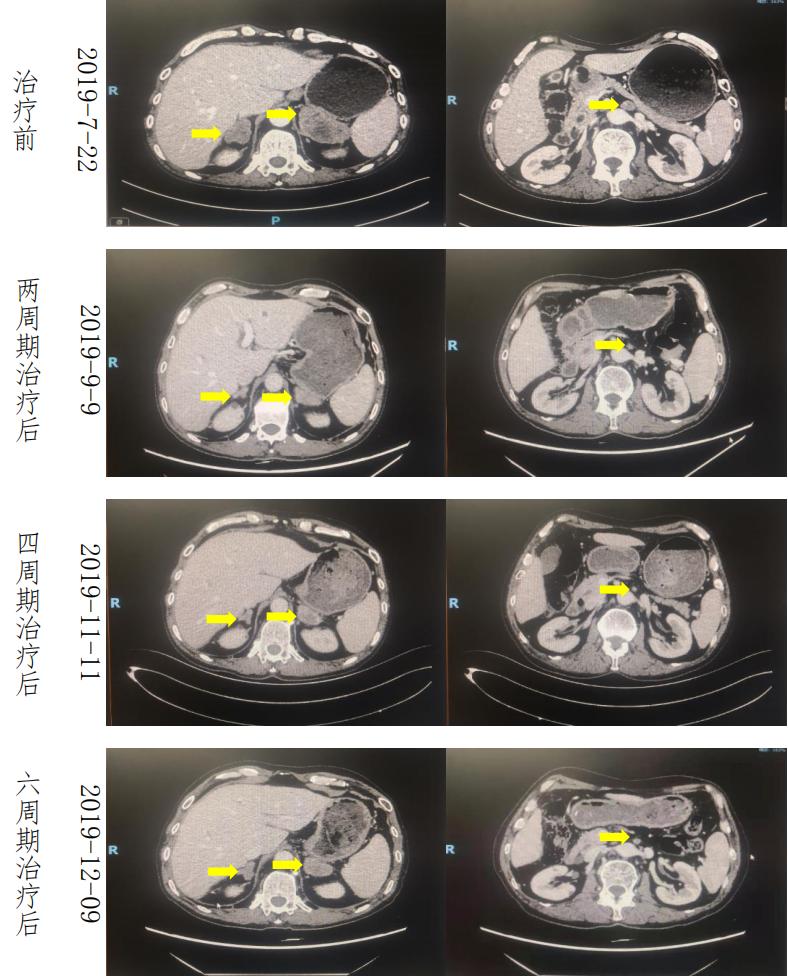
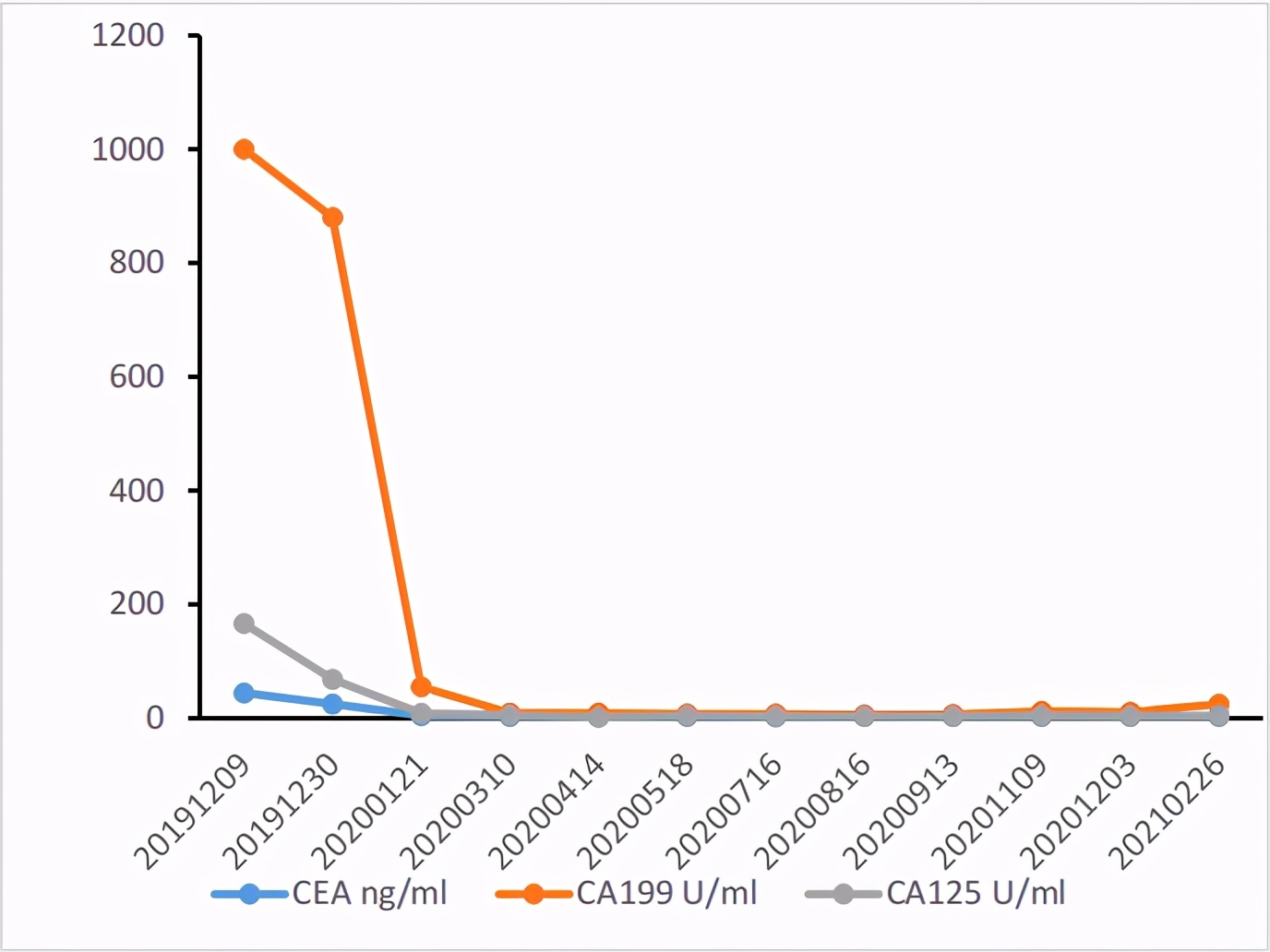
肿瘤标记物:标记物在化疗前 2 周期明显降低,4 周期之后 CA199 回升明显。
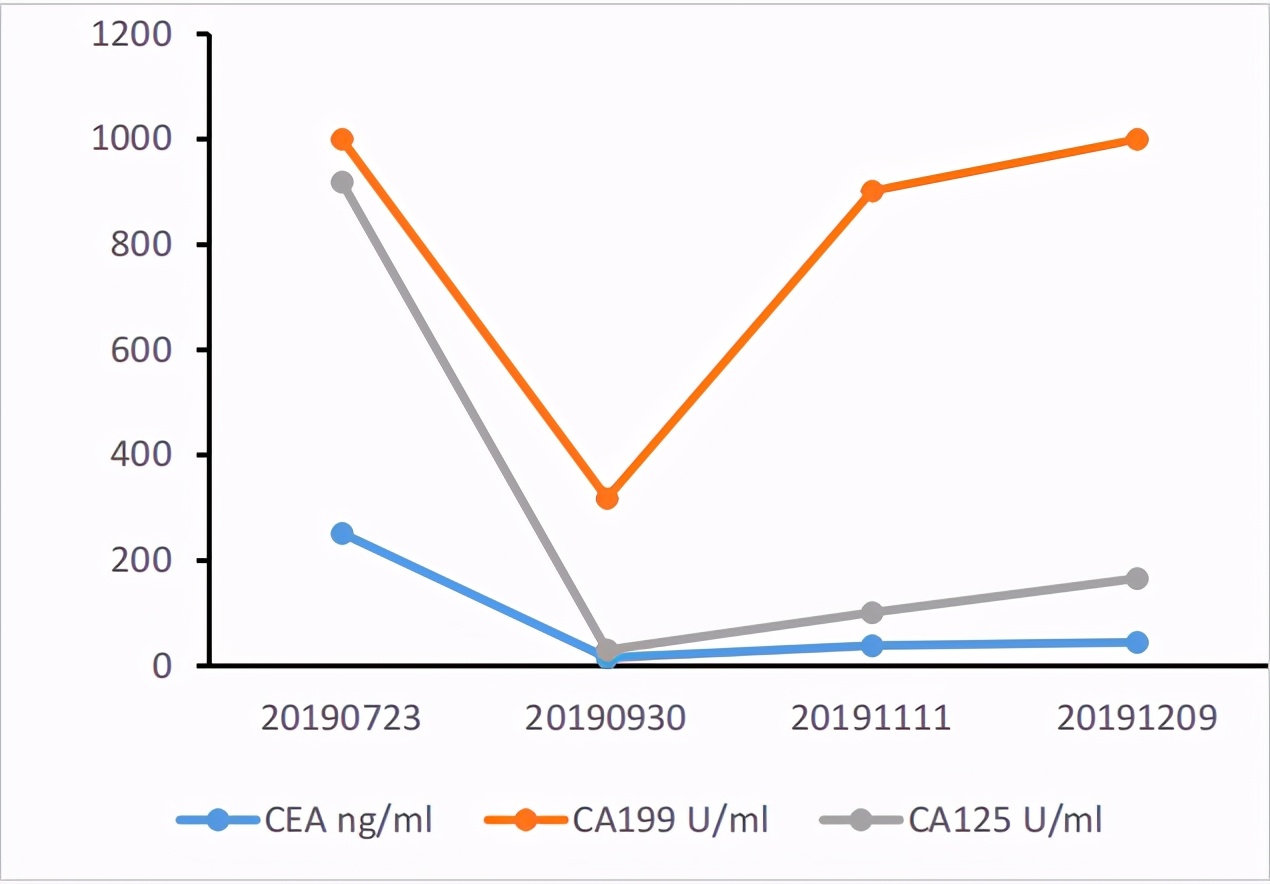
二线方案选择
患者经一线 Xelox 方案化疗 6 周期后,肿瘤体积对比基线缩小,但 6 周期评 估时,肿瘤较 4 周期评估时肾上腺肿块稍增大、标记物 CA199 升高且出现奥沙利 铂相关神经毒性;考虑到患者后期对 Xelox 方案耐受差,且获益有限,我们决定 更改后续治疗方案。鉴于患者肿瘤突变负荷相对较高,且组织中肿瘤细胞 70%表 达 PD-L1。于 2019 年 12 月 10 日至 2020 年 05 月 19 日改行二线化疗联合免疫(伊立替康+卡瑞丽珠单抗)治疗 6 周期。2020 年 06 月 12 日至 2021 年 02 月 26 日 予以 7 周期卡瑞丽珠单抗维持治疗。不良反应:治疗 4 周期后患者腹部、颜面部出现卡瑞利珠单抗相关反应性毛细血管增生。
疗效评价 :二线化疗联合免疫(伊立替康+卡瑞丽珠单抗)治疗 4 周期后肾 上腺及腹膜后病灶明显缩小,联合方案治疗 6 周期后疗效评价(PR),后续予以卡瑞丽珠单抗维持治疗,维持治疗期间肿瘤未出现增大,末次治疗后疗效评价 (PR)。目前患者二线治疗的 PFS 达到 14 个月。
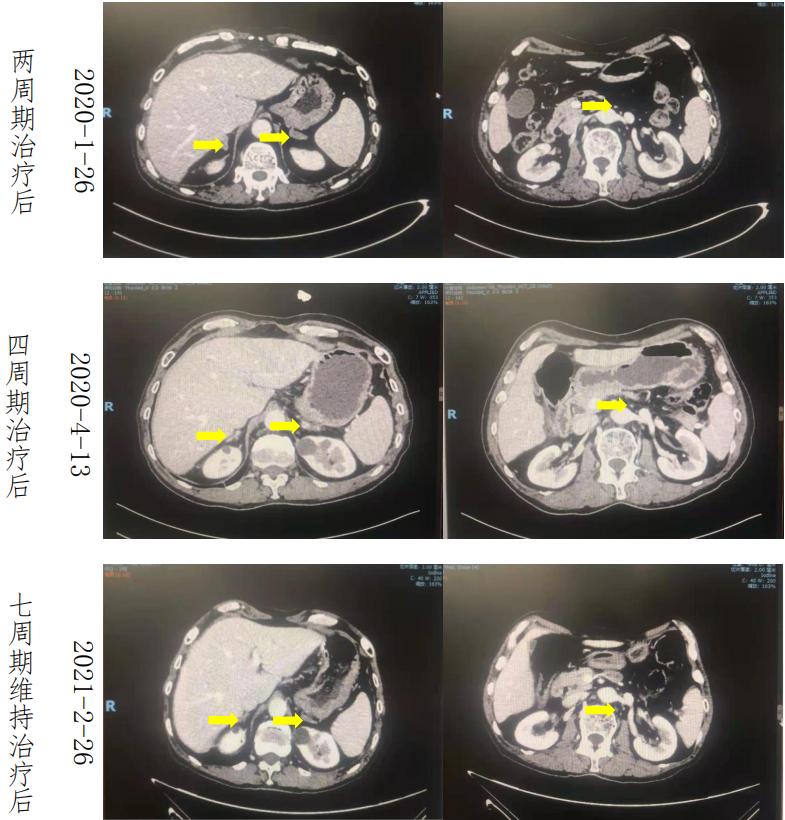
肿瘤标记物:化疗联合免疫治疗 2 周期后标记物显著下降,4 周期后标记物降至 正常范围并维持至今。
小结
小肠腺癌是一类罕见肿瘤,发 病率低,由于缺乏典型的疾病症状,临床体检筛查容易漏诊。与其他胃肠道恶性 肿瘤(包括食道癌,胃癌,结肠癌和直肠癌)在同一时期内发病率下降的趋势相 反,目前小肠癌的发病率呈上升趋势,在 2006 年至 2015 年期间以每年 1.8%的 速度增长。大多数 SAB 病例的肿瘤位于十二指肠(52%~57%),其次是空肠 (18%~29%)、回肠(10%~13%)以及小肠的不明部位(4%~14%)1。诊断为 SBA 的 患者中约有 32%患者已经出现远处转移。最常见的转移部位与其他胃肠道恶性 肿瘤一致,主要是腹膜腔和肝脏。SAB 局限期术后的 5 年生存率相对较高(85%), 但 IV 期 SBA 患者的 5 年生存率仅为 42%。此外,手术治疗的局部 SBA 仍然具有 较高的复发率 2-3。
SBA 的治疗一直未有明确的诊疗指南,全身治疗模式参照化疗,在 2018 年 法国协作组首次推出了 SBA 共识 4,在 2019 年 NCCN 推出了小肠癌的指南,本中 心的一项关于晚期小肠癌一线化疗的临床研究结果也被 SBA NCCN 指南所引用, 我们采用改良 FOLFOX 方案治疗 33 例进展期 SBA,获得了接近 50%的有效应答率, 其中包括 1 例完全缓解 5。本例患者诊断为小肠腺癌,IV 期,患者年龄超过 60 岁,三药联合方案化疗的预期耐受性较差。一线我们依照指南推荐予以 Xelox 方案化疗,并获得了较为显著的近期疗效,但疾病控制时间较短,且患者出现了 明显的奥沙利铂相关外周神经毒性,因而更换二线方案进行治疗。
早年的一些研究提示 SBA 的分子特征与结直肠癌(CRC)类似,而与胃癌(GC) 不同。但 SBA 是在基因层面上还是有别于 CRC,近年(2014 ASCO Abstract No:3647) 研究通过全面基因组测序,发现 SBAs 不同于 CRC 的主要特点包括:第一,其 MSI 的发生率较高;第二,不同于 CRC 和 GC,SBA 主要表现为 HER2 和 EGFR 点突变, 而非扩增。提示 SBA 可能从 ERBB 的小分子激酶*制剂抑**治疗中获益。另外,ZEBRA 研究是一项 SBA 接受单药免疫治疗的二期临床研究,研究观察了既往标准化疗后 进展的 SBA 患者接受单药帕博丽珠单抗(pembrolizumab)治疗的客观有效率, 值得注意的是,研究发现对于检测为 MSS 的 18 名 SBA 患者,帕博丽珠单抗的疾 病控制率高达 50%6。该患者虽然 MSI 状态为 MSS,但在肿瘤细胞有较高的 PD-L1 表达,并有相对较高的肿瘤突变负荷。在接受含有 PD-1 单抗的二线方案治疗后 患者的疾病缓解时间超过了 1 年,提示小肠肿瘤可能存在对免疫治疗良好反应的 分子特征并区别于 CRC。我们相信免疫治疗将可能成为未来小肠癌重要的治疗手段之一。
来源:南昌大学第一附属医院肿瘤科