树突状细胞(dendritic cells, DC)是由加拿大学者免疫学家拉尔夫・斯坦曼( Ralph Steinman)于1973年发现的一种抗原递呈细胞。它们群成熟时会向周围伸出许多树枝状或伪足样的突起,这就是它们名字的由来细胞质呈星状凸起、细胞核极不规则的细胞。之之后的研究发现DC细胞DC表达大量的MHCI类分子和、MHCII类分子,并具有极强的抗原递呈能力,能够有效地激活免疫效应细胞免疫系统。拉尔夫・斯坦曼也籍因此获得2011年的诺贝尔生理或医学奖。
DC疫苗介导的肿瘤免疫治疗就是在DC细胞DC上加负载载肿瘤抗原,再回输给患者,利用DC的抗原递呈能力在患者体内激活T细胞*伤杀**肿瘤。近期的研究越来越关注肿瘤抗原的个性化,即每个患者的肿瘤抗原都不相同,这就需要对每例患者的肿瘤组织进行分析。另外一个研究的热点就是如何获得足量的有功能的DC细胞DC用于制造DC肿瘤疫苗肿瘤的免疫治疗。
原代DC疫苗
DC在人体免疫细胞中所占的比例很小,只有0.1%-1%。原代DC疫苗需要从患者体内先分离出外周血单个核细胞,再从外周血单个核细胞中分离出DC前体细胞。此时的DC前体细胞尚未成熟,还不具备抗原递呈能力,需要经过体外抗原负载和用细胞因子刺激它们成熟以后,才具有抗原递呈能力。这些DC才可以用作疫苗。
Science Translational Medicine:患者全肿瘤裂解物负载DC的疫苗在卵巢癌中获得良好效果
在一项针对卵巢癌的DC疫苗临床试验中,来自宾夕法尼亚大学的研究者使用DC疫苗对抗卵巢癌的方法获得良好的效果。
研究人员从招募的25名晚期卵巢癌患者体内分离出了患者自体的DC以及自体的肿瘤组织。将肿瘤组织裂解后,负载到自体的DC上,再回输给患者。回输后的DC会激活体内的T细胞,将癌症所有的突变都告诉给T细胞,让T细胞发挥肿瘤*伤杀**作用。
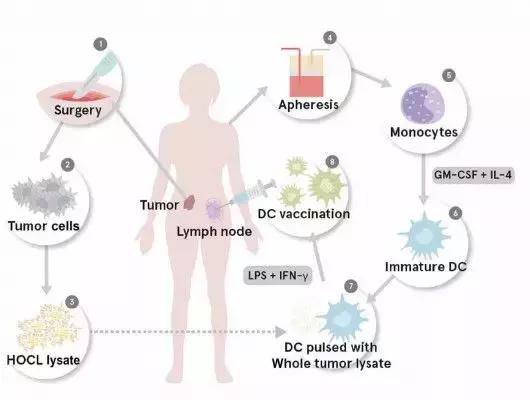
在回输DC的患者体内,能够检测到针对肿瘤细胞的特异性T细胞数量显著上升,说明DC疫苗有着良好的效果。能够响应该疗法的患者的两年生存率为100%,不能响应的患者两年生存率只有25%。在接受治疗的患者中,有一例IV期卵巢癌患者奇迹般地完全康复。此外,采用DC疫苗治疗卵巢癌,没有观察到明显的不良反应。
该项临床试验使用的原代DC疫苗,其中的DC含量只有70%多,每次回输需要5-6 x106个DC,一个疗程回输5次,需要2.5-3 x107个DC。要从患者身上分离如此多的DC非常困难,再加上DC的分离、分化、成熟等工艺复杂,使得DC疫苗的生产十分困难,这是该项临床实验面临的一大问题。
(文章来源:Janos L. Tanyi, Lana E. Kandalaft. et al. Personalized cancer vaccine effectively mobilizes antitumor T cell immunity in ovarian cancer, Science Translational Medicine, 2018-04-11, DOI: 10.1126/scitranslmed.aao5931)
J Transl Med:患者全肿瘤裂解物负载DC的疫苗在脑瘤三期患者取得良好疗效
胶质母细胞瘤(GBM)是一种恶性程度非常高的肿瘤,极具侵袭性,是由中枢神经系统(CNS)内的神经胶质母细胞或者其前体产生的肿瘤。由于中枢神经系统是免疫豁免区(免疫细胞进入不了的区域),因此免疫疗法被认为对该种肿瘤的治疗不会有作用。UCLA的研究人员用了20年的时间,证明细胞疗法对胶质母细胞瘤同样有着很好的疗效。
研究人员招募了331名患者,分离出了患者自体的DC以及肿瘤组织。将肿瘤组织裂解后,负载到自体的DC上,再回输给患者。接受该疗法的患者的中位生存期为23.1个月,比采用标准疗法(手术和化疗)的患者中位生存期要延长8个月。不仅如此,约20%到30%的患者的生存期比预期的要长得多。
疫苗生产涉及到外周血单个核细胞的采集、DC的分离、分化、激活和负载肿瘤抗原等复杂步骤,每一步都会对最后的疫苗功效造成影响。每位患者需要制备10次使用的DC量,如此大量DC的提取同样限制着其的临床使用。
(文章来源:Linda M. Liau et al. First results on survival from a large Phase 3 clinical trial of an autologous dendritic cell vaccine in newly diagnosed glioblastoma, Journal of Translational Medicine, 2018-05-29, https://doi.org/10.1186/s12967-018-1507-6)
J Clinical Investigation:更快更便捷的新生抗原筛选方法在DC肿瘤疫苗中的应用
与直接给DC负载肿瘤组织裂解物不同,新生抗原需要通过生物信息学方法找到肿瘤细胞与正常细胞之间的蛋白差异。只在肿瘤细胞表达的蛋白质即为肿瘤新生抗原。再用这些肿瘤新生抗原负载DC,最后回输给患者。
基于患者自身的肿瘤基因组变异信息,建立以肿瘤突变蛋白产生的新生抗原为基础的个体化免疫治疗模式是未来免疫治疗的重要发展方向,对肿瘤有着治愈性的潜力,尤其在实体瘤中相比其他免疫治疗模式更具优势。
在该项临床研究中,有一例胸腺瘤术后多发转移性肺结节的患者,在三线治疗失败后接受该个体化新生抗原为基础的DC疫苗联合NRT回输治疗,迄今已实现近3年完全缓解,更多的临床试验还在开展中。
该项临床试验中使用的DC疫苗,其制作也需要复杂的分离、分化、成熟等传统过程。因此,同样受到DC数量和DC成熟的效率限制。
(文章来源:Fangjun Chen, Baorui Liu et al. Neoantigen identification strategies enable personalized immunotherapy in refractory solid tumors, J Clin Invest, 2019-05-01 https://doi.org/10.1172/JCI99538)
采用原代DC制作疫苗,虽然取得了良好的效果,但是有两点限制:一是原代DC在外周血单个核细胞中所占的比例很低,分离出足量的疫苗所需的DC特别困难,尤其是肿瘤患者的外周血单个核细胞通常会比正常人的还要低。二是分离后的原代DC体外不能增殖,存活时间不长,且需要复杂的细胞因子刺激成熟后才有一定的抗原递呈功能,不便于操作。基于以上两点原因,使得大多数肿瘤患者无法使用DC疫苗治疗肿瘤。
永生化DC介导的细胞免疫治疗
为了解决DC体外不增殖、数量少、需要激素刺激才能成熟、具备抗原递呈功能的问题,从1973年DC发现到2018年共45年的时间里科学家做出了很多尝试。
直到2008年研究人员才从白血病患者身上偶然分离出一株经细胞因子刺激可以分化为DC的MUTZ-3细胞系。2010年法国的科学家从白血病患者身上分离到一株DC系p DC line,能增殖且无需细胞因子刺激并且具有DC抗原递呈功能。
但是由于每个人的DC表面的白细胞表面抗原(Human leucocyte antigen, HLA)不同,其它人的DC不能直接用于不同患者,为此需要开发一种能够扩增不同患者自体DC的技术。2018年美国马里兰大学的科学家开发出了一种DC永生化技术,可以定制每个人的DC细胞株,获得不限量的、有功能的DC。
PNAS:采用少量血液即可大量扩增DC,定制患者的自体DC细胞株
马里兰大学的Long Wu博士和Hua Cheng研究员,开发出了一种新方法来获得自体DC细胞株。该方法只需抽取供体数十毫升的外周血,分离出其中的单个核细胞后,激活其中的DC分化成熟,再转入永生化基因使DC永生化,从而获得大量的DC,同时保留了DC的抗原递呈功能。
这些DC在体外导入肿瘤抗原基因后可以强劲激活特异性的T细胞,激活的T细胞能够有效*伤杀**肿瘤细胞。在小鼠肺癌模型中,经DC激活的T细胞能够有效清除小鼠肺部的肿瘤细胞,并且不会对小鼠组织造成损伤。在小鼠的乳腺癌模型中,经DC激活的T细胞能够有效抑制肿瘤的生长。
由于该技术可定制患者的DC细胞株,因此DC表面HLA可以完全匹配患者自身的T细胞,在DC介导的肿瘤免疫治疗方面有着很大的潜力。
该技术的合作公司北京惠大生物科技有限公司已经开展了多例永生化DC 细胞株的构建,针对非小细胞肺癌的相关临床试验也正在进行中。

(文章来源:Long Wu , Hua Cheng et al. Induction of antitumor cytotoxic lymphocytes using engineered human primary blood dendritic cells, PNAS, 2018-05, DOI:10.1073/pnas.1800550115)
J Leukocyte Biology:MUTZ-3 细胞系体外分化为DC
研究人员偶然从一名急性淋巴细胞性白血病患者的外周血中获得了细胞系MUTZ-3。该细胞系有三种细胞亚型,其中一种能够在细胞因子刺激下分化为DC。但是这种DC的稳定性不好,一旦缺乏对应浓度的细胞因子就会失去DC表型,很不稳定,限制着它的临床实用。
此外由于不同人的DC表面的HLA不同,异体DC疫苗不一定能够有效激活异体的T细胞,也限制着它的临床应用。
(文章来源:Saskia J. A. M. Santegoets , Alfons J. M. van den Eertwegh et al. Human dendritic cell line models for DC differentiation and clinical DC vaccination studies, Journal of Leukocyte Biology, 2008-06-02, ODI : 10.1189/jlb.0208092)
Plos One:从白血病患者身上偶然获得一株DC系p DC line
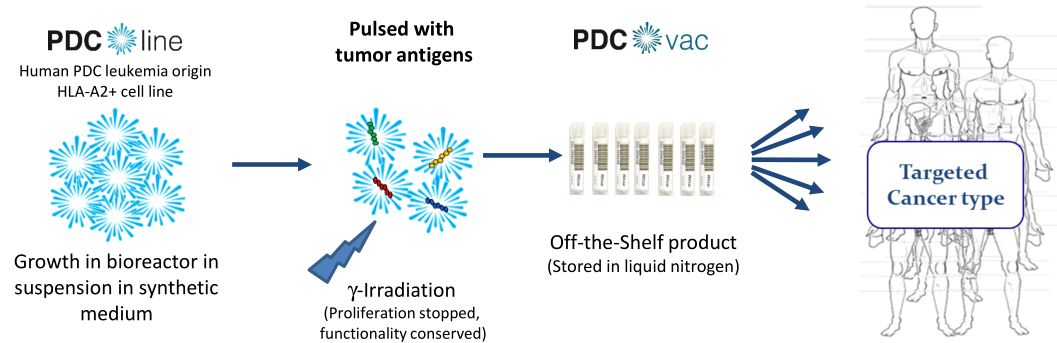
法国的科研人员偶然从白血病患者的血液中获得了一株DC系p DC line。在异体配对的体外实验中,能够有效刺激T细胞增殖。采用该DC系负载抗原肽后,能够在小鼠体内刺激活相应的T细胞增殖,抑制肿瘤进展。
虽然该株DC系突破了DC增殖的限制并具备有抗原递呈功能,但与MUTZ-3细胞株衍生的DC一样,由于不同人的细胞表面的人HLA不同,异体DC疫苗表面的HLA不能够与T细胞表面的HLA完全匹配。
尽管如此,其合作公司法国的PDC LINE PHARMA公司,已经在黑色素瘤和肺癌中完成了I期临床试验,并取得良好效果。
(文章来源:Caroline Aspord1 , Julie Charles et al. A Novel Cancer Vaccine Strategy Based on HLA-A*0201 Matched Allogeneic Plasmacytoid Dendritic Cells, Plos One, 2010-05-04, DOI: 10.1371/journal.pone.0010458)