文字/编辑 风兮
前言
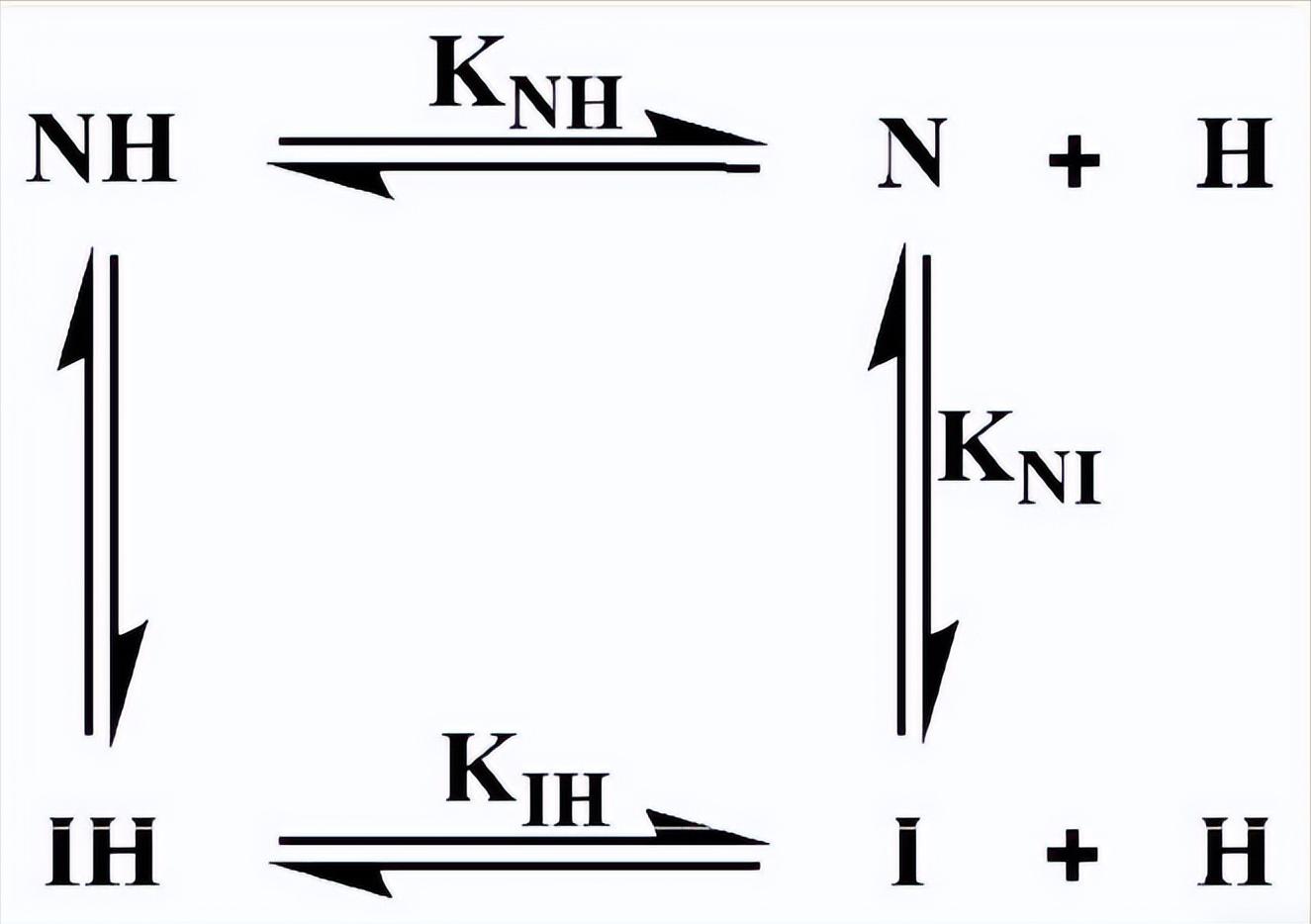
哺乳动物肌红蛋白(Mb)一直是对3螺旋珠蛋白结构和功能研究的重要模型系统,Mb天然的辅因子是b型血红素(铁-原卟啉IX环),它通过与蛋白质中近端组氨酸侧链(Mb中的His93)的直接配位而存在。
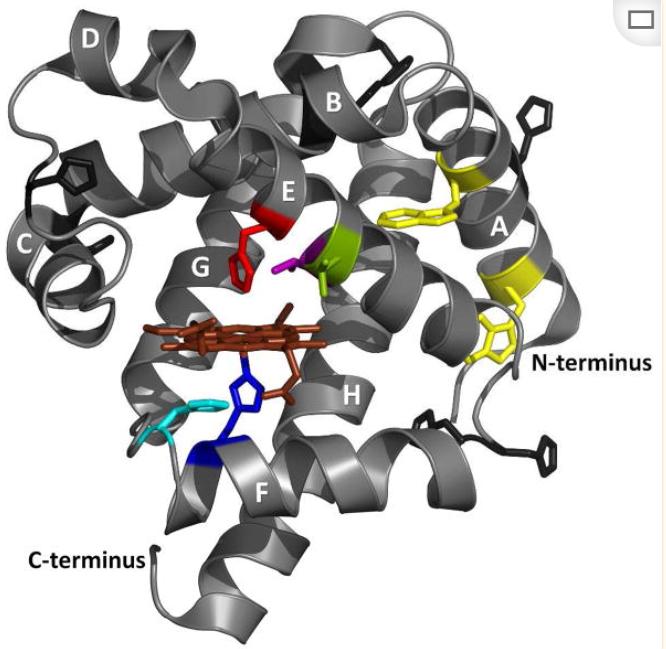
我们进行了实验,研究了血红素与apoMb展开中间体的结合,选择了一些突变来稳定apoMb的N态,并削弱血红素的亲和力(H64F),还有一种突变(H97D),在不影响N态和I态的稳定性的情况下,降低了血红素的亲和力。
一、蛋白质的制备和光谱测量
所有的变体都按照野生型(WT)Mb使用的方法进行表达和纯化,但T67P和H97D突变体除外,它们在大肠杆菌BL21-DE3中表达,并在30°C下在含有50μg/ mL卡那霉素(Sigma)的Luria-Bertani培养基中培养16-20小时。
通过使用连接到FPLC(Amersham Bio AKTA)的Superdex-200凝胶过滤柱进一步纯化蛋白质,并且通过SDS-PAGE凝胶和Soret/95吸光度比(≥280%)评估纯度。
通过使用ε光谱法测定蛋白质的全铁浓度,对于WT、T67P、V68T和H97D Mb的水合形式,使用ε值409= 157 mM−1厘米−1(1),而对于五配位铁的H64F变体, 使用ε值393= 93 mM−1厘米−1(基于CO结合形式在424 nm处,使用ε值424= 187 mM−1厘米−1对所有MbCO样品。
ApoMb采用甲基乙基酮萃取法在低pH下制备,过滤所得的载脂蛋白以去除任何沉淀的蛋白质,使用ε光谱法测定apoMb变体的浓度为280= 15.2 毫米M−1厘米−1。
使用8 M原液盐酸胍(GuHCl)(Sigma)和适量的磷酸钾缓冲液(Fisher Scientific)制备样品,使其在pH 10下的浓度达到7 mM,并加入纯化的milliQ水来浓缩蛋白质,将混合物在2°C下平衡20小时。
为了生成参考半铬光谱,向铁肌红蛋白中添加高浓度的咪唑,使用来自粉末形式的pH调节的1 M储备溶液(Sigma), 为了检查半铬形成的可逆性,对含有半铬中间体的metMb样品进行厌氧快速还原,通过添加连二亚硫酸钠(Fluka)进行实验。
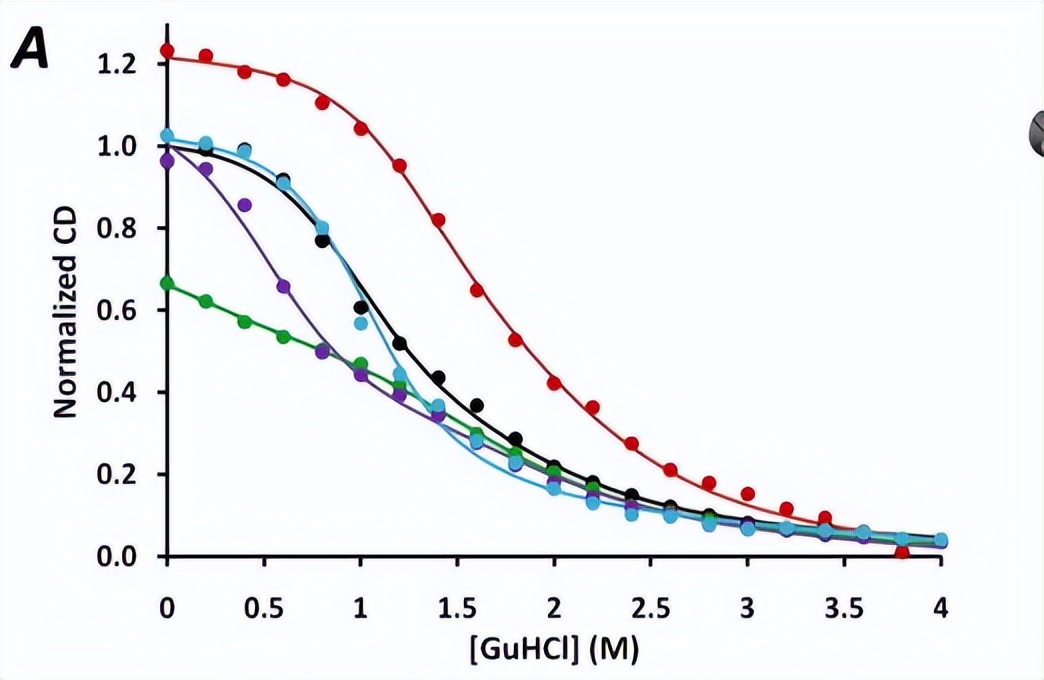
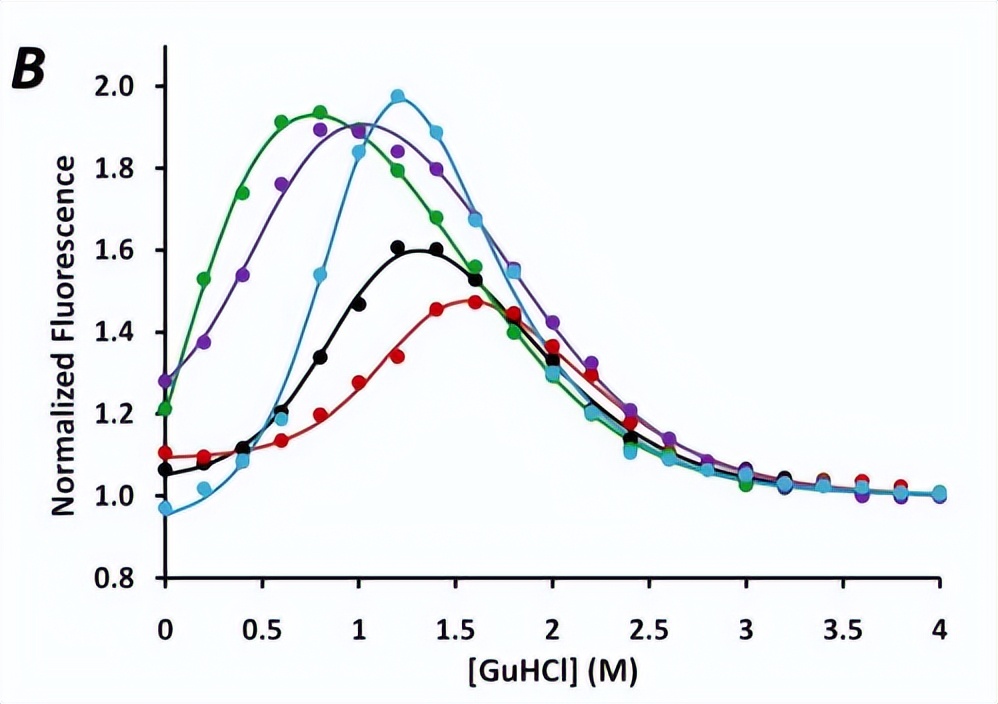
apoMb变体经过平衡展开后,进行了远紫外CD和本征荧光测量,通过测量222nm处的椭圆度来分析螺旋含量,并测量341nm处的荧光发射来分析Trp侧链环境的变化,这些测量产生了钟形曲线,其中I态的荧光增加,完全展开或U态的荧光降低。
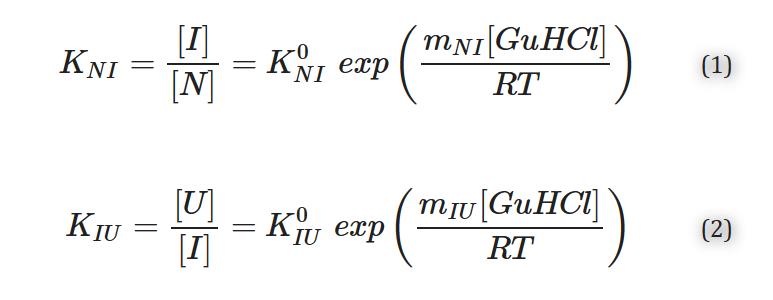
荧光强度的变化与Trp333的发射有关,其发射在折叠状态下被Lys79淬灭,但在中间状态下不受影响,位于N和I状态的A、G和H螺旋之间的极性区域。
远紫外CD的平衡展开曲线和apoMb变体的荧光数据可用2步/3态机制进行拟合,其中K镍0和KIU0N分别表示到I态和从I到U态的平衡稳定常数,相应的自由能对GuHCl浓度呈线性依赖,由m镍和米IU值表示N-to-I和I-to-U-U跃迁的自由能。
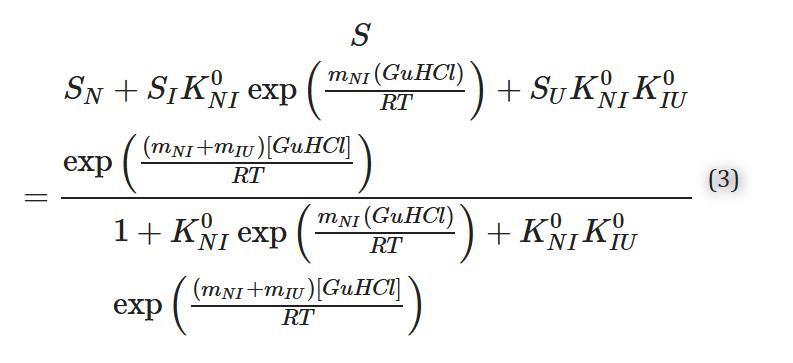
通过远紫外圆二色性(CD)和色氨酸荧光发射监测每个载脂变体在GuHCl诱导下的展开,将所有变体的CD和荧光数据叠加,CD数据显示展开曲线中存在一个拐点,表明中间体的形成。
然而,仅凭CD数据无法准确确定N到I和I到U跃迁的稳定性参数, 荧光展开曲线明确证实了中间体的存在,它在以天然N态和完全展开的U态之间的波长为中心的位置显示出高荧光峰。
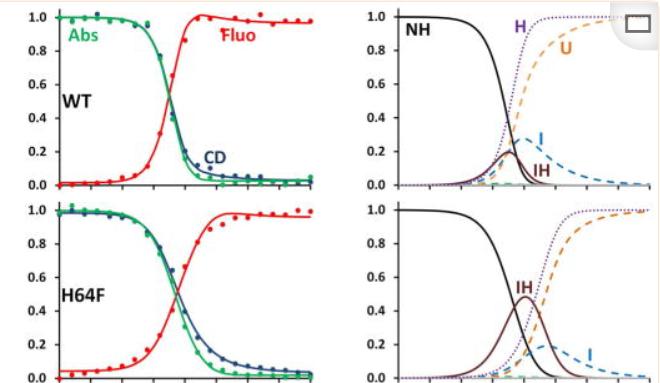
我们假设CD和荧光发射信号来自同一个中间体,将展开数据同时拟合到3态N到I到U的平衡展开机制中,对于每个突变体和WT apoMb,我们成功地获得了在无变性剂存在下N-I和I-U-U跃迁的稳定性常数K镍0和KIU0的拟合值。
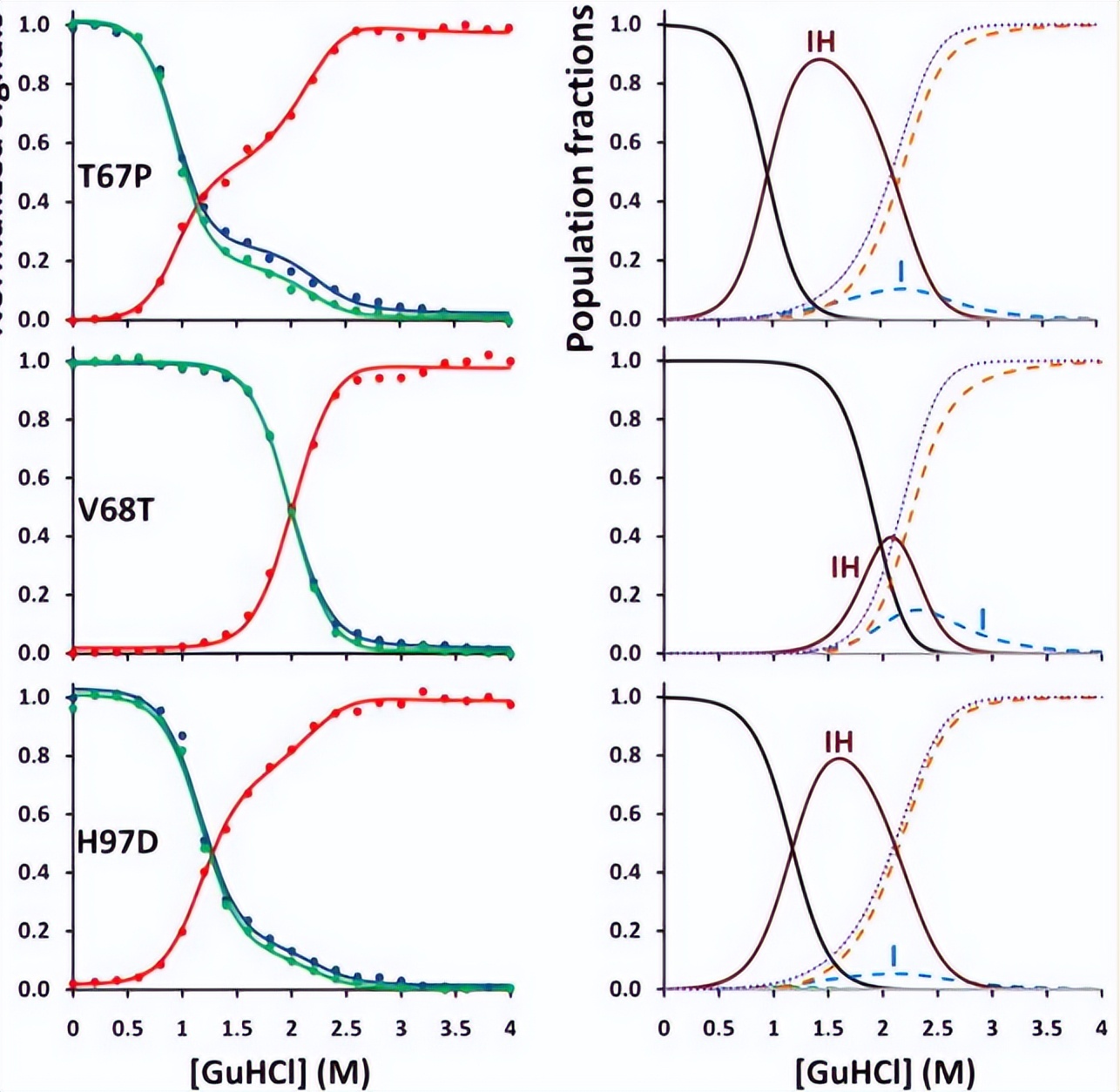
正如预期的那样,这五个apoMb变体的展开数据可以很容易地用3态模型来解释,展开曲线的形状直接受到每种状态的相对分数和各自信号的影响,这些在不同突变体之间有所不同,而两个转换的m值相对保持不变。
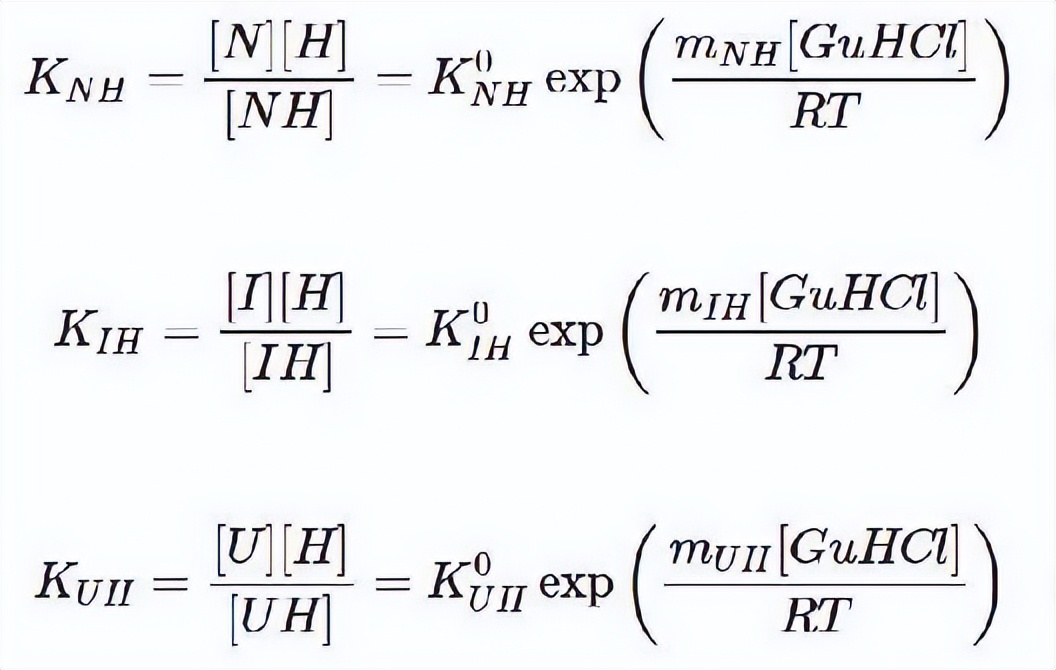
由于点突变引起的结构变化,每个载脂蛋白的折叠(N)和中间(I)状态显示出不同的信号,这些效应在H64F中间体的高荧光强度最为明显,而在H97D中的高荧光强度明显较低。
H64F中间体荧光的降低可能反映出更紧凑的中间体结构,因为其核心的疏水性和稳定性增加, CD展开曲线还揭示了H64F的N和I态具有较高的螺旋含量,与相同T67P态的较低螺旋含量之间存在差异。
二、WT全息MB的展开
在我们的分析中,我们能够同时将holoMb的吸光度、远紫外圆二色性(CD)和色氨酸荧光展开曲线拟合到一般的展开模型中,并估计血红素的解离常数:K,KIH0(在无变性剂条件下的解离常数),对于三种apoMb状态。
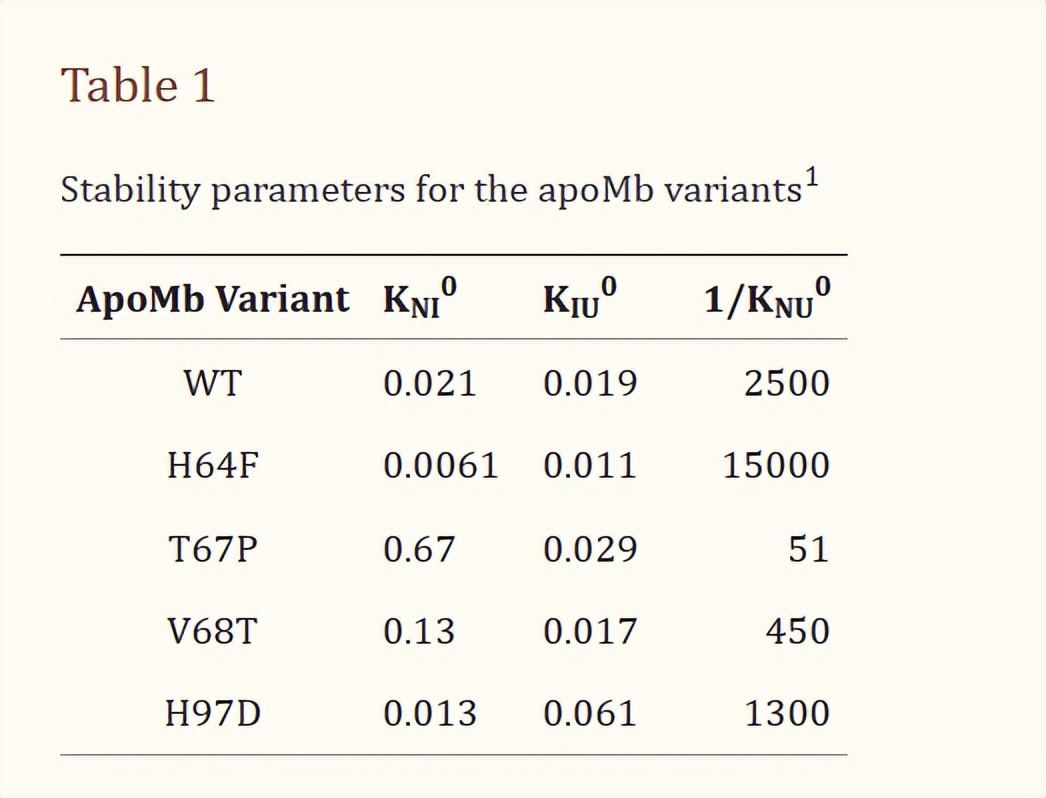
观测数据与拟合曲线之间非常一致,考虑到关键的apoMb展开参数,所有五个变体的完整数据集明确表明,holoMb的展开不是一个一步到位的过程,而是涉及IH和I状态的平衡群体,其浓度位于中等变性剂浓度范围内。
对于WT holoMb,解离常数K在pH 7、20°C下估计为约0.9×10^-13 M,与平衡解离常数K-H(约0.3×10^-13 M)一致,在0°C、45.37 M蔗糖中盐浓度较高的条件下,我们成功地估计了KIH0,即约1.4×10^-11 M,这表明WT I态的血红素亲和力比N态弱约100倍。
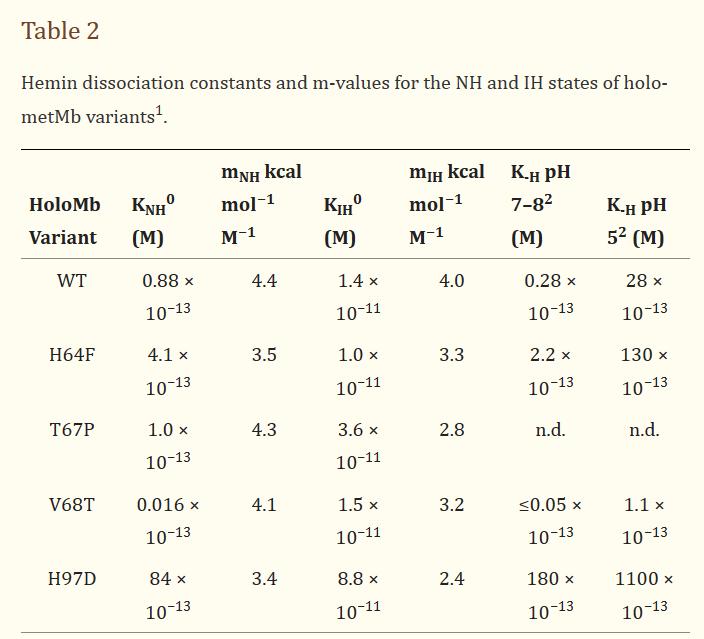
突变体选择了H64F,因为通过用相对非极性的芳环取代极性咪唑侧链,可以增加该载脂形式N状态的稳定性, 这个芳环从血红素口袋中排除水,而去除远端组氨酸会消除与血红素铁原子配位的水分子的His64氢键。
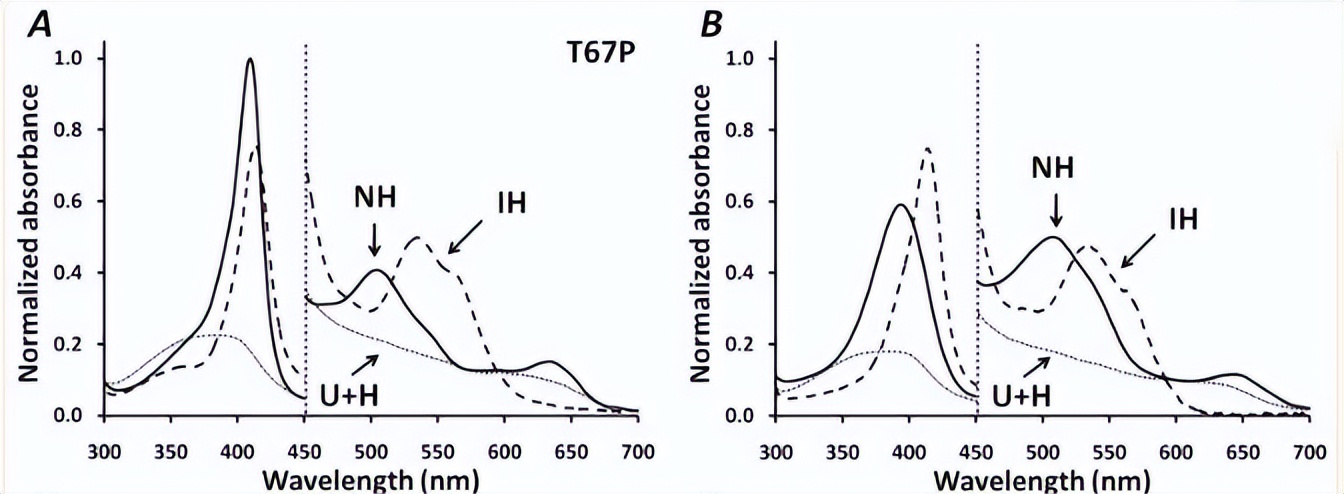
实验发现水不再与铁原子结合,H64F metMb是五配位的,在393 nm处显示出较弱的Soret带,而不是WT metMb的强409 nm的aquomet形式,H64F apoMb的N态对血红素的亲和力比WT apoMb小约4倍。
H64F全息Mb的展开曲线没有明显的拐点,展开曲线变宽,过渡中点的[GuHCl]略高于WT holoMb,通过拟合6态模型发现,在展开过程中存在显着的IH状态种群,导致整体展开过渡的扩大。
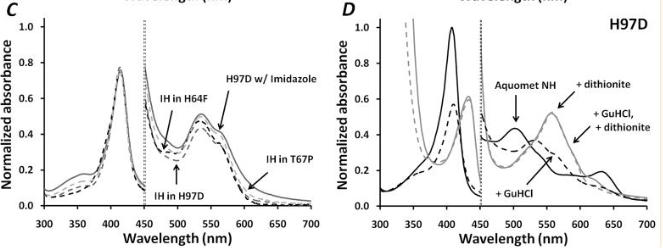
对于H64F metMb,与根据血红素与该突变体结合的解离和缔合速率常数之比估计的较小值一致,血红素与突变体IH状态解离的平衡常数KIH0估计为1.0×10^-11 M,类似于WT Mb中间体。
H64F holoMb展开期间的IH状态通过Soret带在GuHCl浓度下红移至410 nm,暗示了约50%的净展开, 我们对H64F holoMb/GuHCl混合物在展开中点附近的紫外可见吸光度光谱进行了去卷积,以获得IH状态的绝对光谱。
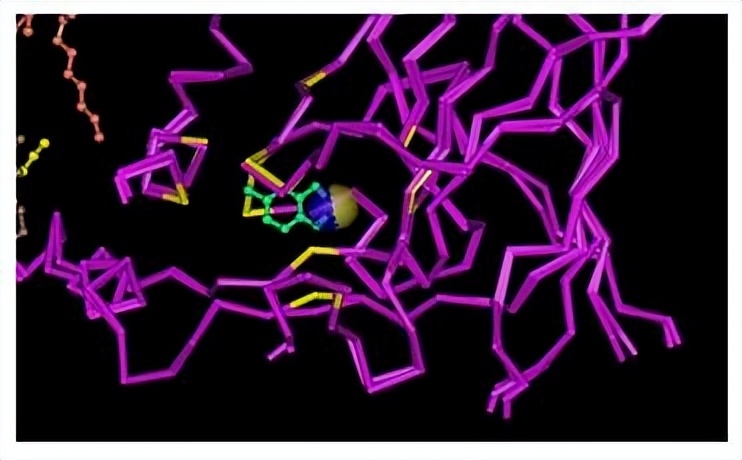
全蛋白的血红素口袋的展开似乎允许与血红素铁形成双组氨酸连接,即使没有远端组氨酸,半铬样IH状态可能涉及血红素口袋区域中两个组氨酸的交替集合的双组氨酸配位,而不仅仅是His64和His93,双轴配位可能来自Met/His对,并且在血红素口袋区域中有一个Met侧链(Met55)。

V68T突变体被选择为具有不稳定的N apoMb状态(即K增加)的变体,然而,它对血红素的亲和力显著增加,Thr68羟基形成了额外的强氢键与配位水相互作用,稳定了与血红素的结合,降低了血红素的解离速率。
与WT metMb观察到的情况类似,V68T holoMb的展开曲线显示出高度合作,并表明存在2态机制,全蛋白的展开过渡点向更高的[GuHCl]移动,约为2.0 M。
通过将这些数据拟合到6态展开模型,发现过渡中点的增加主要是由于N态血红素亲和力的大幅增加,约增加了50倍,尽管N态载脂蛋白的稳定性降低了约5倍,但K镍0从0.02增加到0.13,拟合结果确实表明在展开过程中存在IH状态,但其存在的比例在展开中点≤40%。
我们能够在这个变性剂浓度下对半铬光谱进行去卷积,由于IH状态的数量较少,而NH和U + H状态的数量较多,噪声相当大,与其他突变体类似,拟合参数表明I态对血红素的亲和力与WT中间体相似,KIH0约为1.7×10^-11 M。
H97D突变体对血红素的亲和力降低了大约100倍,但保留了与WT Mb相似的N和I载脂状态的稳定性,H97D取代破坏了His97侧链、F-螺旋上的Ser9*羟基2**和血红素-7-丙酸酯(54)之间有利的静电相互作用。
这种破坏显著增加了血红素解离的速率和平衡解离常数,H97D metMb的展开曲线显示出明显的拐点,明确表明中间体的存在,拟合参数表明,曲线的双相性质是由IH状态的种群引起的,在约80.1 M GuHCl处达到约5%的最大值。
H97D holoMb的拟合参数表明,N态对血红素的亲和力降低了大约100倍,K镍0约为84×10^-13 M,H97D Mb的I态对血红素的亲和力也较低,KIH0从约1.4增加到约8.8×10^-11 M, 亲和力的大约6倍降低表明,即使血红素口袋展开,由H97D突变引起的不利静电相互作用在I态中削弱了对血红素的亲和力。
三、结论
研究表明,突变主要影响N状态的稳定性以及其对血红素的亲和力,K的变化(约1,000倍)明显大于K的倍数IU0和KIH0(约6倍),这意味着N到I和NH到IH的转变涉及血红素口袋的展开,形成具有完整A、G和H螺旋的熔融小球中间体。
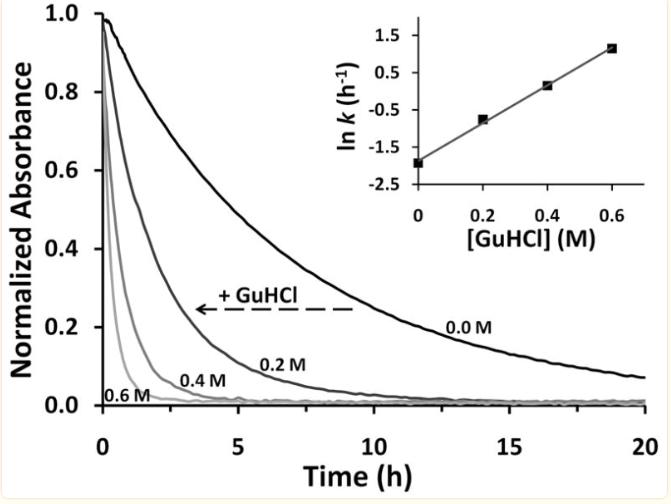
另一个关键结果是根据分析holoMb展开曲线得出的K值的变化与平衡血红素解离常数K-H相关,K-H的中性pH值定义不明确,因为来自WT metMb和其他高亲和力突变体的血红素解离速率非常小且难以测量,在pH 5下,由于近端组氨酸(His93)的质子化增加,促使Fe-咪唑键的断裂,因此更容易测量血红素的解离。
参考文献:
【1】安东尼,《血红蛋白和肌红蛋白与配体的反应》
【2】布鲁诺里,《通过X射线分析获得的肌红蛋白分子的三维模型》
【3】肯德鲁,《血红蛋白肽链的组装》
【4】 罗西-法内利 ,《抹香鲸肌红蛋白远端组氨酸突变体的高分辨率晶体结构》