随着医学的发展和药物研发的深入,人们对于类风湿关节炎(RA)的认识不断加深,各类治疗药物也不断更迭。虽然在合理用药的三原则(安全、有效、经济)中,安全性居首位,但在RA致残的巨大阴影下,临床医生有时会认为「有效性」似乎更重要。然而实际上,RA治疗药物已在追求安全性的路上完成了多轮变革。

非甾体抗炎药:从广泛应用到限制使用
20世纪前半世纪缓解RA症状主要使用水杨酸,之后以该药为原型衍生出了非甾体抗炎药( NSAIDs)。NSAIDs虽然不能改变疾病进程或阻止关节破坏进而真正控制RA,但可以较好地缓解关节疼痛等症状,因此获得了广泛应用。
然而,随着研究的推进,越来越多的证据发现长期使用NSAIDs会引发多系统的不良反应。一项研究分析了不同种类NSAIDs的不良反应发生率,结果显示患者的消化道和心血管不良事件发生率分别高达23.68%和21.92%。
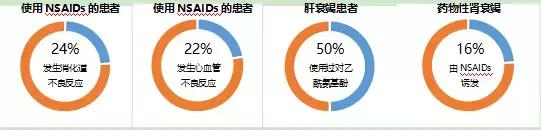
NSAIDs的不良反应不仅局限于此,还包括肝、肾功能损害等。据文献报道,约50%的肝衰竭患者都使用过对乙酰氨基酚,16%的药物性肾衰竭由NSAIDs诱发。
因此,目前临床上认为应避免长期使用NSAIDs并严格控制剂量。2018中国类风湿关节炎诊疗指南明确指出,NSAIDs的使用场景为:中/高疾病活动度的患者,根据症状和病情小剂量短疗程使用。
糖皮质激素跌落神坛
1944年美国内科医生Philip S.Hench首次用激素治疗RA,发现糖皮质激素强大的抗炎作用能迅速缓解关节肿痛和全身炎症,随即糖皮质激素在RA中的应用获得迅速传播,Philip S.Hench医生也因此获得了1950年的诺贝尔医学奖。
遗憾的是,与NSAIDs一样,很快医学界便发现了大剂量糖皮质激素的严重副作用,大家开始重新反思糖皮质激素治疗RA的利弊。
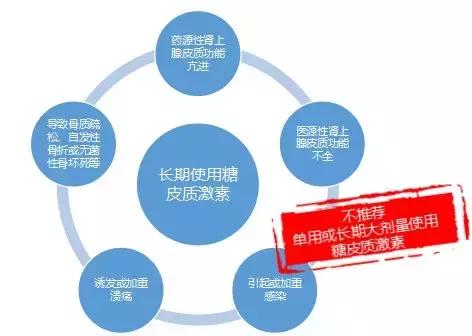
研究显示,长期使用糖皮质激素可能会引起药源性肾上腺皮质功能亢进,医源性肾上腺皮质功能不全,引起或加重感染,诱发或加重溃疡,导致骨质疏松、自发性骨折或无菌性骨坏死等,尤其是常见的激素性骨质疏松症,无疑将使RA患者雪上加霜。
到了50年代末,糖皮质激素在RA治疗中受到极大冷落,大有被“淘汰出局”之势。直到现在,对于RA患者,指南仍明确不推荐单用或长期大剂量使用糖皮质激素4,可谓是受了安全性问题的重创。
但是我们也无需因噎废食,目前的研究也证实,对于中/高疾病活动度的RA患者,在改善病情的抗风湿药(DMARDs)治疗的基础上加用小剂量糖皮质激素可快速控制RA的症状和体征,同时安全性尚可,可以作为DMARDs起效前的桥梁药物。
DMARDs:安全性各有不同
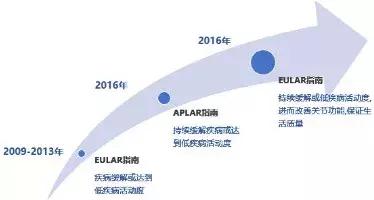
20世纪80年代,RA治疗进入了标准化治疗时代,其基本的治疗方案是甲氨蝶呤(MTX)±DMARDs。在欧洲抗风湿病联盟(EULAR)的2016 RA管理指南更新中,RA的治疗目标已从「缓解」提升到了「持续缓解」,这无疑进一步提高了对DMARDs药物安全性的要求,因为治疗药物的远期安全性是影响RA患者持续缓解的重要因素。由于DMARDs的安全性特点不近相同,应基于患者特点和用药方案合理选择药物。
MTX 是目前RA的首选治疗药物,也是基石。因此,在选择与MTX联用的DMARDs时,必须考虑MTX原本的不良反应,避免产生不良反应的叠加,增加安全性问题。
目前常见的的MTX不良反应主要为恶心、呕吐、腹痛、厌食等消化道症状,以及脱发、口腔溃疡、白细胞计数降低、肝功能损害和肺炎等。以肝功能损害为例,来氟米特 ( LEF)在治疗过程中也易发生肝脏不良反应,因此,不宜与MTX联合使用。
2002年欧洲药物评价组织发现296例使用LEF后发生的肝脏不良反应,且129例均为严重不良反应,15例肝衰竭,9例死亡。
目前,包括EMEA、加拿大卫生部和美国食品药品监督管理局(FDA)在内的多个官方机构都对MTX+LEF联合用法提出了明确的反对意见。而我国1.1类新药艾拉莫德在安全性方面表现优异,是非常适合与MTX长期联合的DMARDs。
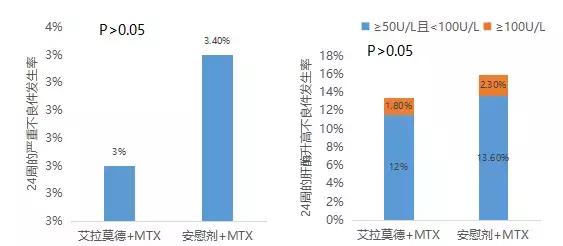
研究显示,与安慰剂相比,艾拉莫德与MTX联用24周,不增加常见不良反应和严重不良反应。且艾拉莫德IV期研究提示艾拉莫德的安全性与年龄无关,即便是老年患者也可安全使用。
至于生物DMARDs,虽然目前认为其不良反应的发生率较低,但研究发现有些特殊不良反应的后果却非常严重,甚至可能致命,因此还是应该受到关注。常用的生物制剂几乎均有药物相关性间质性肺病(ILD)的报道。而ILD是RA死亡的重要因素,RA-ILD中位生存时间仅为2.6-3.0年。
英国一项前瞻性研究(BSRBR)纳入9,294例使用TNF-α拮抗剂和2,454例使用合成DMARDs治疗的RA患者,分析其ILD的发生率,结果显示TNF-α拮抗剂引起的新发ILD事件显著高于合成DMARDs(2.9% vs. 1.8%, P=0.02)。
此外,其他报道较多的严重不良反应包括:感染、充血性心力衰竭、系统性红斑狼疮样综合征等。
RA长病程管理时代:谁是未来的安全性之王?
RA是一种慢性疾病,长病程管理是关键。如何优选用药呢?基于上安全性问题,NSAIDs和糖皮质激素已明确注定只能是短期使用的药物,无法成为RA的常驻常客,DMARDs中安全性的佼佼者才可能获得长期应用。
以羟氯喹的视网膜病变风险为例,随着使用时间和剂量的增加,其视网膜病变风险快速提升。像这样的药物,在长期使用时必须权衡获益与风险。
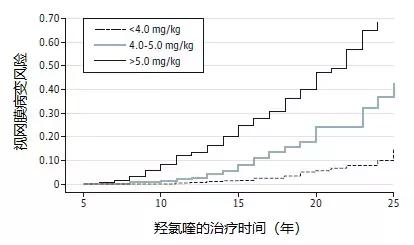
值得一提的是新型DMARD艾拉莫德,其短期(24周)用药的安全性已在国内外的大量临床试验中获得了明确证实,与此同时,艾拉莫德的长期疗效更可为人称道。日本一项研究纳入294例RA患者,进行了为期52周的临床研究,其中部分患者甚至持续使用艾拉莫德达100周。
结果显示,谷丙转氨酶和谷草转氨酶升高的累积发生率分别为19.4%和18.3%,但不良反应均主要发生在第4-8周的时间内;即便不停药,不良反应大多也可自发消退,在第16-100周时,不良反应未较前增加,提示艾拉莫德具有出色的长期安全性。
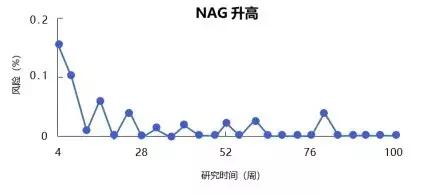
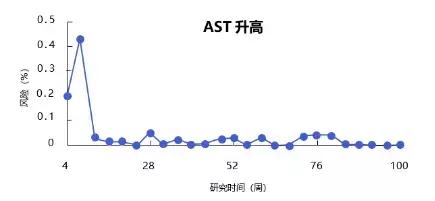
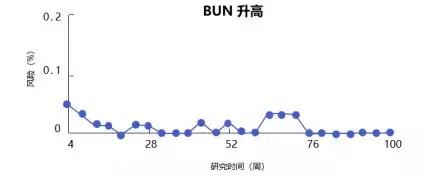
非甾体抗炎药和糖皮质激素已退出核心地位,而DMARDs,特别是艾拉莫德这样长期安全性好的新型DMARDs,必将成为RA联合治疗的优选药物。期待未来有更多的安全优效的药物为RA治疗带来新的变革。
参考文献:
[1] Day RO, Graham GG. Non-steroidal anti-inflammatory drugs (NSAIDs)[J]. BMJ. 2013 Jun 11;346:f3195.
[2] 张建环,朱群娣,钟建明.我院非甾体抗炎药在治疗膝骨关节炎中的临床应用分析[J].广东药学院学报,2014,30(04):486-488.
[3] 曹向光,杨华.非甾体消炎药的不良反应研究进展[J].中国医药,2017,(4):631-633.
[4] 中华医学会风湿病学分会.2018中国类风湿关节炎诊疗指南[J].中华内科杂志,2018,(4):242-251.
[5] Nassar K,Janani S,Roux C,et al.Long-term systemic glucocorticoid therapy:patients' representations,prescribers' perceptions,and treatment adherence[J]. Joint Bone Spine,2014,81(1):64-68.
[6] Da Silva JA,Jacobs JW,Kirwan JR,et al.Safety of low dose glucocorticoid treatment in rheumatoid arthritis:published evidence and prospective trial data[J]. Ann Rheum Dis,2006,65(3):285-293.
[7] Kirwan JR,Bijlsma JW,Boers M,et a1.Efiects of glucocorticoids on radiological progression in rheumatoid arthritis[J].Cochrane Database Syst Rev,2007,1(1):CD006356.
[8] Gorter SL, Bijlsma JW, Cutolo M, et al. Current evidence for the management of rheumatoid arthritis with glucocorticoids: a systematic literature review informing the EULAR recommendations for the management of rheumatoid arthritis [J]Ann Rheum Dis,2010,69(6):1010-1014.
[9] 刘升云,杨璐,张磊,等.甲氨蝶呤联合小剂量泼尼松治疗类风湿关节炎的短期疗效与安全性[J].中华内科杂志,2013,52(12):1018. 1022.
[10] Smolen JS, Landewé R, Bijlsma J, et al. EULAR recommendations for the management of rheumatoid arthritis with synthetic and biological disease-modifying antirheumatic drugs: 2016 update[J]. Ann Rheum Dis, 2017, 76(6):960-977.
[11] 高素辉. 甲氨蝶呤治疗类风湿关节炎的不良反应分析[J]. 临床合理用药,2012,5( 24) : 20-21.
[12] Hara M, Ishiguro N, Katayama K, et al. Safety and efficacy of combination therapy of iguratimod with methotrexate for patients with active rheumatoid arthritis with an inadequate response to methotrexate: an open-label extension of a randomized, double-blind, placebo-controlled trial[J]. Mod Rheumatol. 2014 ,24(3):410-8.
[13] Symmons DP, Silman AJ. Antitumor necrosis factor alpha therapy and the risk of lymphoma in rheumatoid arthritis: no clear answer[J]. Arthritis Rheum, 2004,50:1703–6.
[14] Chen J, Chi S, Li F, et a. Biologics-induced interstitial lung diseases in rheumatic patients: facts and controversies[J]. Expert Opin Biol Ther, 2017, 17(3):265-283.
[15] Suda T. Up-to-date information on rheumatoid arthritis-associated interstitial lung disease[J]. Clin Med Insights Circ Respir Pulm Med,2015,9(Suppl 1):155-162.
[16] Nakashita T,Ando K,Kaneko N,el a1.Potential risk of TNF inhibitors on the progression of interstitial lung disease in patients with rheumatoid arthritis[J].BMJ Open, 2014, 4(8):e005615.
[17] Melles RB, Marmor MF. The risk of toxic retinopathy in patients on long-term hydroxychloroquine therapy[J]. JAMA Ophthalmol. 2014, 132(12):1453-60.
[18] Hara M, Abe T, Sugawara S, et al. Efficacy and safety of iguratimod compared with placebo and salazosulfapyridine in active rheumatoid arthritis: a controlled, multicenter, double-blind, parallel-group study[J]. Mod Rheumatol. 2007;17(1):1-9.
[19] Lü LJ, Teng JL, Bao CD, et al. Safety and efficacy of T-614 in the treatment of patients with active rheumatoid arthritis: a double blind, randomized, placebo-controlled and multicenter trial[J]. Chin Med J (Engl) 2008;121:615-9.
[20] Hara M, Abe T, Sugawara S, et al. Longterm safety study of iguratimod in patients with rheumatoid arthritis[J]. Mod Rheumatol 2007;17:10-6.
中国首部《CSCO原发性肝癌诊疗指南》(以下简称《指南》)在2018中国临床肿瘤学会肝胆胰肿瘤大会上正式发布。据了解,本《指南》在参考ASCO、NCCN、ESMO、AASLD、EASL指南,以及我国2017版国家规范、TACE共识、射频共识、放疗共识、抗病毒指南等一系列专科规范的基础上,结合CSCO规范撰写而成。
关注公众号“MED24”,回复“原发性肝癌诊疗指南”查看更多内容
MED24医学传媒面向广大医生及医学生,致力于打造中国最具影响力的医学视频资讯平台。敬请关注