系统性红斑狼疮(SLE),是很多女性的噩梦,面部出现红斑、对光过敏、口腔溃疡……全身各处组织器官的损伤,都可能是“狼”烙下的印记。也正因为临床表现复杂多样,SLE被公认为许多风湿和自身免疫性疾病的“原型”[1]。
随着诊疗水平的进步,我国SLE患者的5年生存率已稳定在90%以上[2],但生存≠生活,通过有效地治疗最大程度延缓疾病进展和减少复发,是无数SLE患者的期待。
如今,这份期待或将很快随着一种“中国力量”的成功,真正化为现实。
SLE治疗的“全新时代”,仍在前方
生物制剂,是21世纪医学对抗各种风湿和自身免疫性疾病的“利器”。但相比在类风湿关节炎、银屑病等疾病的广泛应用,生物制剂在治疗SLE方面可谓“姗姗来迟”,2011年贝利尤单抗(Belimumab)的获批,才使得生物制剂进入SLE治疗领域。
在前不久更新的《2020中国系统性红斑狼疮诊疗指南》(简称《指南》)中,首次推荐贝利尤单抗和利妥昔单抗(未获批SLE适应症)这两种生物制剂用于常规治疗效果不佳、不耐受或复发的患者,但推荐级别仅为2B级[3]。
可以看到,《指南》对目前现有生物制剂的推荐力度明显有限,同时也指出其有效性和安全性仍有待进一步验证。从临床研究来看,两种生物制剂也可能存在应答率有限(不足60%)、对肾脏等SLE受累器官的保护稍差、部分患者有安全性风险等问题[4-5]。
面对SLE复杂的病情,看来现有的生物制剂还不能“彻底搞定”。想要让SLE治疗真正大踏步走向“全新时代”,生物制剂就必须在作用机制、有效性和安全性上全面进步。
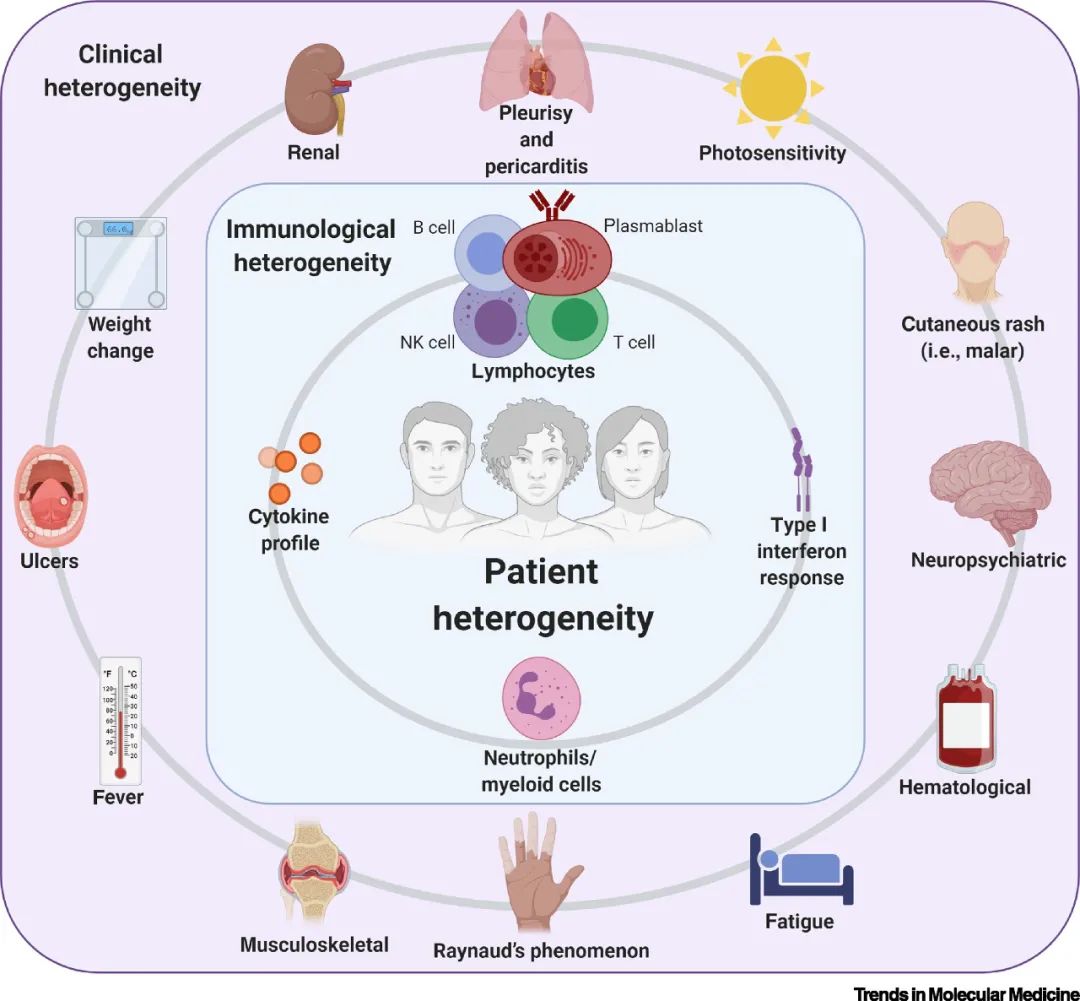
SLE的诊疗还有很多问题要解决
(图片来源:Trends in Molecular Medicine)
*管双**齐下,全方位抑制异常B细胞的“一生”
众所周知,SLE的发病主要与患者体内的B细胞出现异常,产生大量的致病性自身抗体有关,但导致B细胞异常的机制也很复杂,各种亚群的T细胞、巨噬细胞以及其它内外因素都参与其中,因此到现在SLE的发病机制仍未完全阐明。
虽说矛盾多多,但还是得先抓主次。归根到底,SLE发病最主要的矛盾就是B细胞异常,而目前“收拾”这些异常B细胞的思路有两种:一种是传统的靶向特定位点、对其进行直接攻击,比如靶向CD20的利妥昔单抗.
另一种思路,则是对异常B细胞成熟和增殖过程中,多种起到关键作用的细胞因子进行抑制,从而减少异常B细胞产生的致病性自身抗体。已被发现与SLE有关的重要细胞因子包括B淋巴细胞刺激因子(BLyS,又名B细胞活化因子/BAFF)、增殖诱导配体(APRIL)等。
BLyS和APRIL会与体内异常B细胞结合,导致原本应该被清除的异常B细胞得以存活,但两种细胞因子在SLE发病机制中的功能也不尽相同,BLyS主要参与B细胞的发育成熟,而APRIL与B细胞活化和分泌抗体有关。因此抑制BLyS或APRIL,在理论上可以减少导致SLE的异常B细胞,降低患者的疾病活动度。
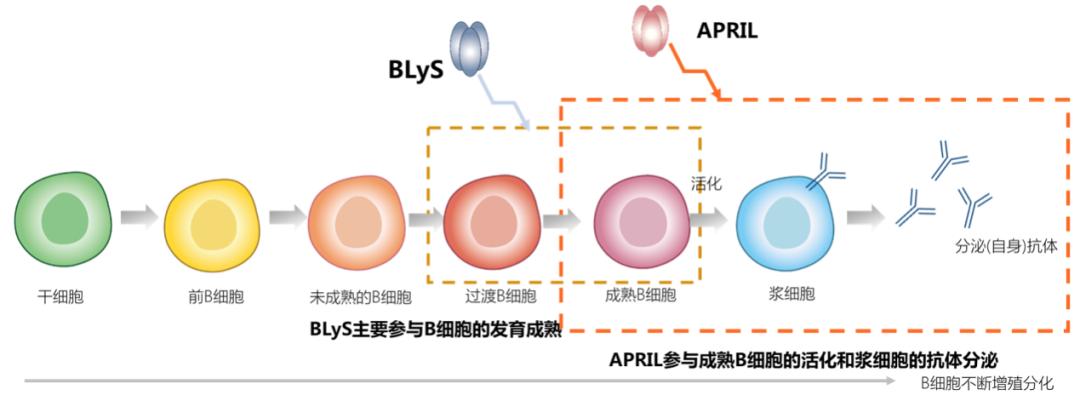
这张图信息量更大更详尽
在靶向这两个位点的药物设计上,科学家们也采用了两种并行的思路。
一种是单独靶向BLyS,例如已经获批治疗SLE的贝利尤单抗,以及折戟临床III期研究的Tabalumab[6]。
另一种就是“双靶点生物制剂”,能同时靶向BLyS和APRIL,是因为二者存在TACI、BCMA等三种共用受体,在理论上能被一种药物共同抑制。
首个靶向BLyS/APRIL双靶点的生物制剂是Atacicept,它与贝利尤单抗几乎同步进入临床研究,但在一项预防中重度SLE患者狼疮再发的临床III期试验中,75毫克Atacicept组未体现明显疗效优势,而150毫克组则因两例患者安全性问题,入组提前终止[7]。
虽然Atacicept在临床试验中遗憾失利,但同时靶向BLyS/APRIL的治疗价值仍值得继续探索,对药物的安全性进行改进,优选更需要、更适合双靶向生物制剂的患者,就能把这条路继续走下去。
疗效安全性双优,有望改写中国SLE患者治疗历史
由我国自主研发的生物制剂新锐泰它西普(Telitacicept),就在“前浪”的基础上更进一步:它的临床II期试验结果于2019年底的美国风湿病学会(ACR)年会被口头报告,并被列为“压轴级别”的延迟公布摘要(Late-Breaking Abstract,LBA)之一。
能成为国际级学术会议的LB*级A**研究,泰它西普靠的是试验中体现的出色疗效和安全性,它的成功源自药物设计上的进步,也标志着“中国智造”的力量。
泰它西普并不是单抗类药物,而是TACI-Fc融合蛋白型生物制剂,它的开发通过重组DNA技术,将能够抑制BLyS/APRIL双靶点的TACI蛋白基因片段,和人体IgG蛋白的Fc基因片段融合在一起,表达出来的蛋白就同时具备两种蛋白的特点。
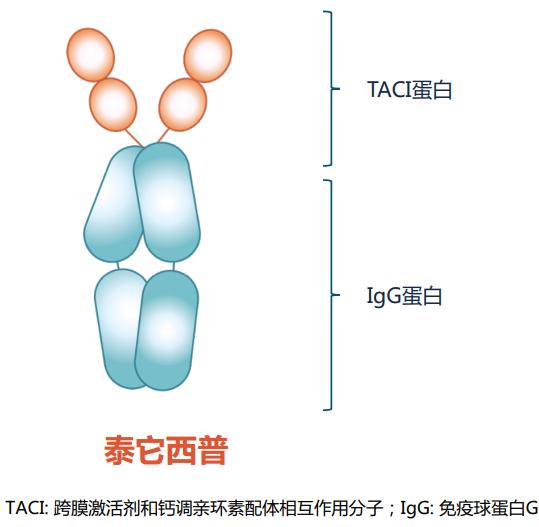
“融合蛋白型”生物制剂长这样
虽然思路相似,但泰它西普在设计上较Atacicept更优化,这也反映在临床前的研究数据中:泰它西普结合并抑制BLyS/APRIL的能力,与Atacicept相比提升了一倍[8]。药理学特性的提升,也为泰它西普的临床试验成功奠定了基础。
说回去年在ACR年会上公布的临床II期试验,这是一项多中心、随机、双盲、安慰剂对照的研究,共入组249例SLE患者,患者被分为四组,每周一次分别接受80、160、240毫克泰它西普治疗或使用安慰剂。
试验结果显示,160/240毫克泰它西普组的SRI4应答率分别为68.3%和75.8%,都显著优于安慰剂组的33.9%,而且泰它西普起效迅速,治疗4周时应答率即明显高于安慰剂组,患者异常IgG、IgM和IgA抗体的水平也相对更低[9]。
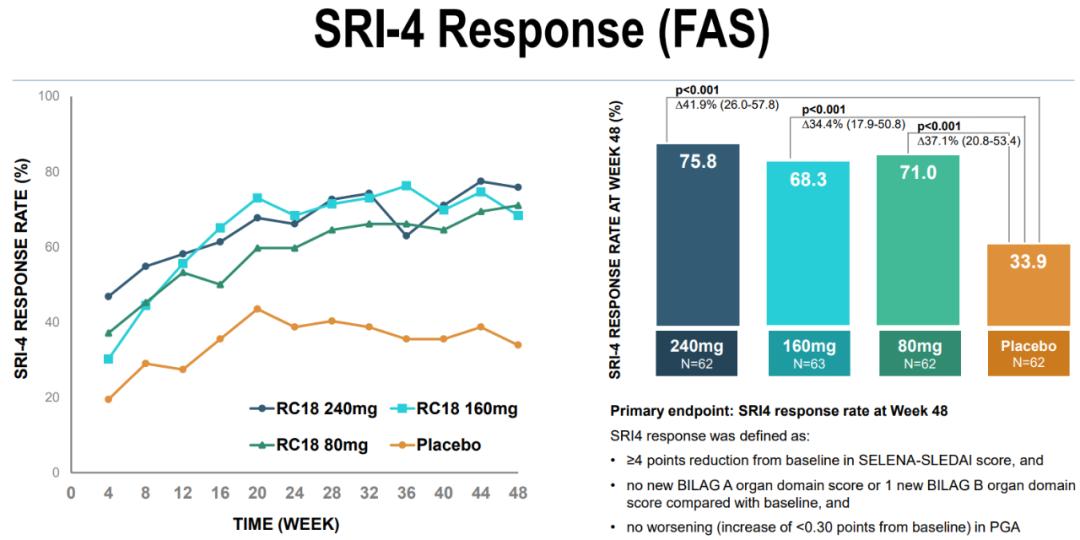
不同剂量泰它西普与安慰剂的疗效对比,都达到了显著性差异
疗效上应答率高、迅速起效,而泰它西普在安全性方面的表现也同样出色:治疗组呼吸道感染、注射部位反应等不良事件的发生率和严重程度,以及不良事件导致的剂量调整或停药发生率,也基本与安慰剂组相当,患者对治疗的耐受性好。
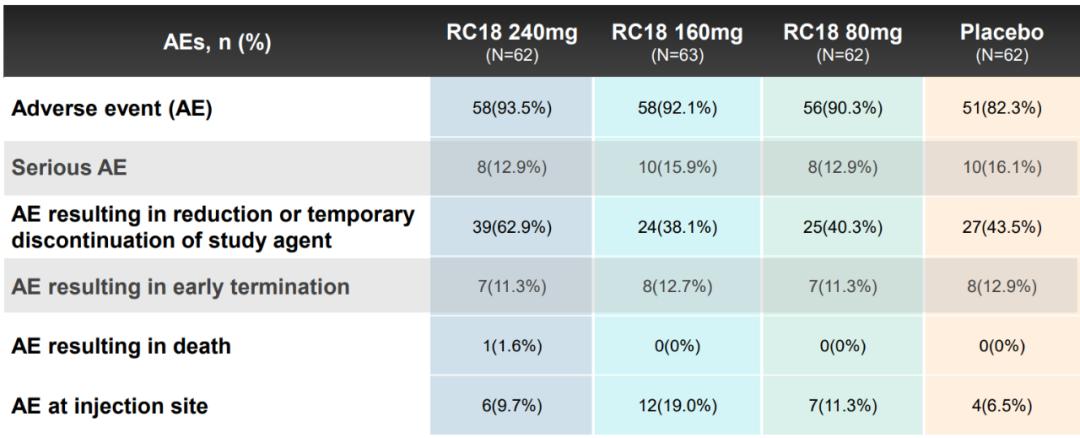
评价生物制剂治疗,安全性很关键
正是基于优秀的疗效和安全性,泰它西普已向国家药品监督管理局(NMPA)提交上市申请,并获优先审评,有望获批后为中国SLE患者提供新的治疗选择,相信也会带动国内诊疗指南和临床实践的变革。
而美国FDA也授予泰它西普快速审批通道(Fast Track)的资格,为进一步验证临床II期试验的发现,泰它西普治疗SLE的临床III期试验已在国内启动,并将在美国同步启动类似试验,争取尽快走上国际舞台。
进入生物制剂时代,战胜SLE这只“狼”仍然不易,但奇点糕一直相信,随着创新药物源源不断地涌现,再强的狼也会被打垮。如果能引领“战狼”的是国产创新药物,那绝对会是历史性的一刻。
参考资料:
1.Ballestar E, Esteller M, Richardson B C. The epigenetic face of systemic lupus erythematosus[J]. The Journal of Immunology, 2006, 176(12): 7143-7147.
2.Wang Z, Wang Y, Zhu R, et al. Long-term survival and death causes of systemic lupus erythematosus in China: a systemic review of observational studies[J]. Medicine, 2015, 94(17).
3.中华医学会风湿病学分会. 2020中国系统性红斑狼疮诊疗指南[J].中华内科杂志, 2020, 59(3): 172-185.
4.Dooley M A, Houssiau F, Aranow C, et al. Effect of belimumab treatment on renal outcomes: results from the phase 3 belimumab clinical trials in patients with SLE[J]. Lupus, 2013, 22(1): 63-72.
5.Wallace D J, Navarra S, Petri M A, et al. Safety profile of belimumab: pooled data from placebo-controlled phase 2 and 3 studies in patients with systemic lupus erythematosus[J]. Lupus, 2013, 22(2): 144-154.
6.Isenberg D A, Petri M, Kalunian K, et al. Efficacy and safety of subcutaneous tabalumab in patients with systemic lupus erythematosus: results from ILLUMINATE-1, a 52-week, phase III, multicentre, randomised, double-blind, placebo-controlled study[J]. Annals of The Rheumatic Diseases, 2016, 75(2): 323-331.
7.Isenberg D, Gordon C, Licu D, et al. Efficacy and safety of atacicept for prevention of flares in patients with moderate-to-severe systemic lupus erythematosus (SLE): 52-week data (APRIL-SLE randomised trial)[J]. Annals of The Rheumatic Diseases, 2015, 74(11): 2006-2015.
8.Chen X, Hou Y, Jiang J, et al. Pharmacokinetics, pharmacodynamics, and tolerability of single ascending doses of RCT-18 in Chinese patients with rheumatoid arthritis[J]. Clinical Pharmacokinetics, 2014, 53(11): 1033-1044.
9.Wu D, Li J, Xu D, et al. A Human Recombinant Fusion Protein Targeting B Lymphocyte Stimulator (BlyS) and a Proliferation-Inducing Ligand (APRIL), Telitacicept (RC18), in Systemic Lupus Erythematosus (SLE): Results of a Phase 2b Study[C]//ARTHRITIS & RHEUMATOLOGY. 111 RIVER ST, HOBOKEN 07030-5774, NJ USA: WILEY, 2019, 71.
头图来源:Pixabay

本文作者 | 谭硕