N6-甲基腺苷 (N6-methyladenosine,m6A) 修饰是真核生物 mRNA 转录后 修饰中最常见、最丰富的化学修饰之一,由“Writer”甲基转移酶复合体 (包括 METTL3、METTL14 及辅助因子 WTAP 等) ,“Reader” RNA 阅读蛋白 (包括 YTH 域家族 YTHDF1-3、YTHDC1-2 和 IGF2 RNA 结合蛋白家族 IGF2BP1-3 等) ,以及“Eraser”去甲基化酶 (FTO 和 ALKBH5) 共同调控 【1】 。m6A 修饰在 多种细胞生物学过程中发挥重要作用,包括调控 RNA 的加工、剪接、转运、降 解和翻译等 【2,3】 。异常的 m6A 修饰与多种恶性肿瘤的发生和进展密切相关。
YTHDF2 作为最早被鉴定的 m6A 修饰阅读蛋白之一,主要分布于细胞质中, 介导 m6A 修饰的 mRNA 代谢,包括调控靶 mRNA 的翻译与稳定性等 【4】 。YTHDF2 由一个负责结合 m6A 的 C 端 YTH 结构域和一个富含 P/Q/N 的 N 端结 构域组成,其表达或功能异常与多种肿瘤的发生与转移密切相关,是潜在的肿瘤 治疗靶点之一 【5】 。目前已报道的 YTHDF2 蛋白翻译后修饰包括 SUMO 化修 饰、磷酸化修饰、乳酸化修饰等,受肿瘤微环境、胞外信号刺激和细胞营养状况 等调控。 YTHDF2 是否存在其他翻译后修饰?是否影响 YTHDF2 蛋白的生物学 功能,并通过调控下游靶基因的 m6A 修饰,在 HBV 相关肝癌的发生发展过程 中发挥重要作用?目前国内外未见相关报道。
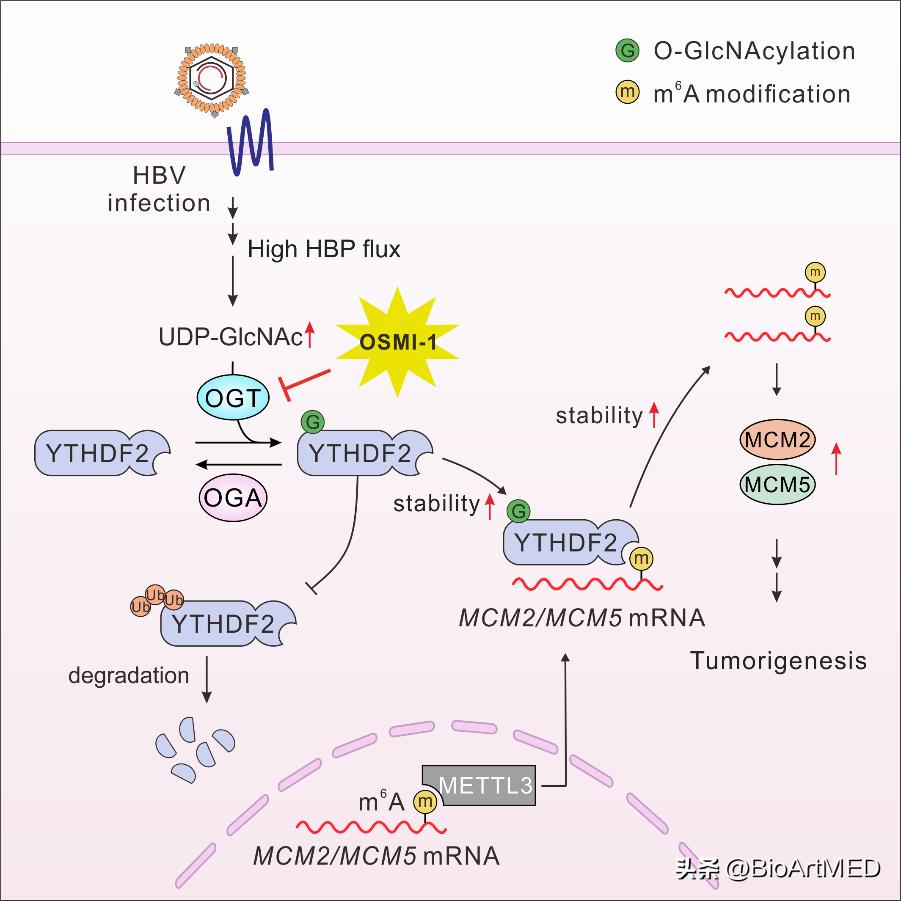
2023年2月10日,重庆医科大学感染性疾病分子生物学教育部重点实验室 黄爱龙/唐霓 课题组在 Signal Transduction and Targeted Therapy 在线发表 了题为 O-GlcNAcylation of YTHDF2 promotes HBV-related hepatocellular carcinoma progression in an N6-methyladenosine-dependent manner 的 研究论文。该研究首次发现乙型肝炎病毒 (HBV) 感染导致 YTHDF2 蛋白 O- GlcNAc 糖基化修饰增强,质谱和免疫沉淀等实验表明第 263 位丝氨酸 (Ser263) 是YTHDF2发生O-GlcNAc修饰的关键位点;采用m6A-seq、RIP-seq和RNA- seq 联合筛选并鉴定到微小染色体维持蛋白 2 (minichromosome maintenance protein 2, MCM2) 和 MCM5 是其下游靶标;而 OGT *制剂抑** OSMI-1 可减弱 YTHDF2 的 O-GlcNAc 修饰,进而抑制 HBV 相关肝癌进展。 该研究首次报道了 YTHDF2 的一种新的蛋白质翻译后修饰——O-GlcNAc 修饰,揭示了病毒感染、 蛋白质翻译后修饰与 RNA m6A 表观修饰之间的动态调控网络,为寻找 HBV 相 关肝癌新的预后标志物和分子靶点提供新思路。

氧连接 N-乙酰葡萄糖胺 (O-linked N-acetylglucosamine,O-GlcNAc) 修饰 是一种广泛的、动态的蛋白质翻译后修饰方式,参与基因转录、信号转导、细胞 周期和代谢等多种细胞生命活动 【6,7】 。己糖胺生物合成途径 (Hexosamine- biosynthesis pathway, HBP) 来源的尿苷二磷酸 N-乙酰氨基葡萄糖 (UDP- GlcNAc) 是 O-GlcNAc 修饰的供体底物 【8】 。研究团队在既往研究中发现 HBV 相关肝癌中,HBP 途径关键代谢物 UDP-GlcNAc 浓度升高,O-GlcNAc 修饰水 平显著上调 【9】 。本研究通过免疫沉淀联合质谱 (IP-MS) 筛选到 YTHDF2 可能 被 O-GlcNAc 修饰,点突变及 IP 实验证实 Ser263 是 YTHDF2 发生 O-GlcNAc 修饰的关键位点;O-GlcNAc修饰减弱YTHDF2的泛素化降解、增强其蛋白稳定 性,从而促进 HBV 相关肝癌进展。
为了进一步寻找 YTHDF2 调控的下游靶标,研究人员通过 m6A-seq、RIP- seq 和 RNA-seq 等多种技术联合筛选并鉴定到 MCM2 和 MCM5 是受其调控的 m6A 修饰分子。RIP、RNA 稳定性及荧光素酶活性等实验进一步证实 YTHDF2 的 O-GlcNAc 修饰通过稳定 MCM2 、 MCM5 ,促进 HBV 相关肝癌细胞周期进展 和增殖。最后,该研究采用 HBV (r)cccDNA 感染的 Alb-cre 小鼠和 HBV 转基因 小鼠构建乙肝相关肝癌模型,验证了 YTHDF2 蛋白的 O-GlcNAc 修饰与 MCM2/MCM5 表达和肝癌增殖密切相关。
上述研究结果揭示了 HBV 感染通过促进己糖胺代谢,导致 YTHDF2 的 O- GlcNAc 修饰增强,以 m6A 依赖的方式调控下游靶基因并促进 HBV 相关肝癌进
展的分子机制。同时,该研究也发现 OGT *制剂抑** OSMI-1 可以通过靶向 YTHDF2 O-GlcNAc 修饰,抑制 HBV 相关肝癌进展,提供了一种新的潜在抗癌治疗策略。
重庆医科大学杨泱博士、严宇硕士、印家鑫硕士、唐霓教授和汪凯副研究 员为该文的并列第一作者;黄爱龙教授为该文的通讯作者。
原文链接:
https://www.nature.com/articles/s41392-023-01316-8
制版人:十一
参考文献
1. Huang, H., Weng, H. & Chen, J. m6A Modification in Coding and Non-coding RNAs: Roles and Therapeutic Implications in Cancer. Cancer Cell 37, 270– 288 (2020).
2. Frye, M., Harada, B. T., Behm, M. & He, C. RNA modifications modulate gene expression during development. Science 361, 1346–1349 (2018).
3. Wang, X. et al. N6-methyladenosine-dependent regulation of messenger RNA stability. Nature 505, 117–120 (2014).
4. Chen, X., Zhou, X. & Wang, X. m6A binding protein YTHDF2 in cancer. Exp Hematol Oncol 11, 21 (2022).
5. Liao, J. et al. Insight into the structure, physiological function, and role in cancer of m6A readers—YTH domain-containing proteins. Cell Death Discov. 8, 137 (2022).
6. Parker, M. P., Peterson, K. R. & Slawson, C. O-GlcNAcylation and O-GlcNAc Cycling Regulate Gene Transcription: Emerging Roles in Cancer. Cancers 13, 1666 (2021).
7. Makwana, V., Ryan, P., Patel, B., Dukie, S.-A. & Rudrawar, S. Essential role of O-GlcNAcylation in stabilization of oncogenic factors. Biochimica et Biophysica Acta (BBA) - General Subjects 1863, 1302–1317 (2019).
8. Akella, N. M., Ciraku, L. & Reginato, M. J. Fueling the fire: emerging role of the hexosamine biosynthetic pathway in cancer. BMC Biol 17, 52 (2019).
9. Hu, J. et al. Hexosamine biosynthetic pathway promotes the antiviral activity of SAMHD1 by enhancing O-GlcNAc transferase-mediated protein O- GlcNAcylation. Theranostics 11, 805–823 (2021).