继发性甲状旁腺功能亢进(SHPT)是慢性肾脏病患者常伴有的并发症,其在很大程度上影响着患者的生活质量及存活时间。多种因素参与了 SHPT 的发生及发展。
目前已知的包括高磷血症、低钙血症、钙敏感受体(CaSR)及维生素D受体(VDR)的异常,成纤维细胞生长因子23(FGF-23)与该疾病的形成存在着密切的相关性。

人们越来越认识到控制SHPT的重要性,控制高磷血症被认为是控制SHPT的基础,维生素D受体激活剂(VDRAs)广泛用于治疗SHPT,在使用 VDRAs 和拟钙剂仍不能控制PTH的情况下,应考虑使用甲状旁腺切除术。
随着肾小球滤过率(GFR)的降低,系统矿物质代谢和骨成分开始改变。随着 GFR 的丢失加剧,矿物质代谢紊乱打乱了骨的微观结构和重塑情况,称之为慢性肾脏病-矿物质骨疾病(CKD-MBD)。
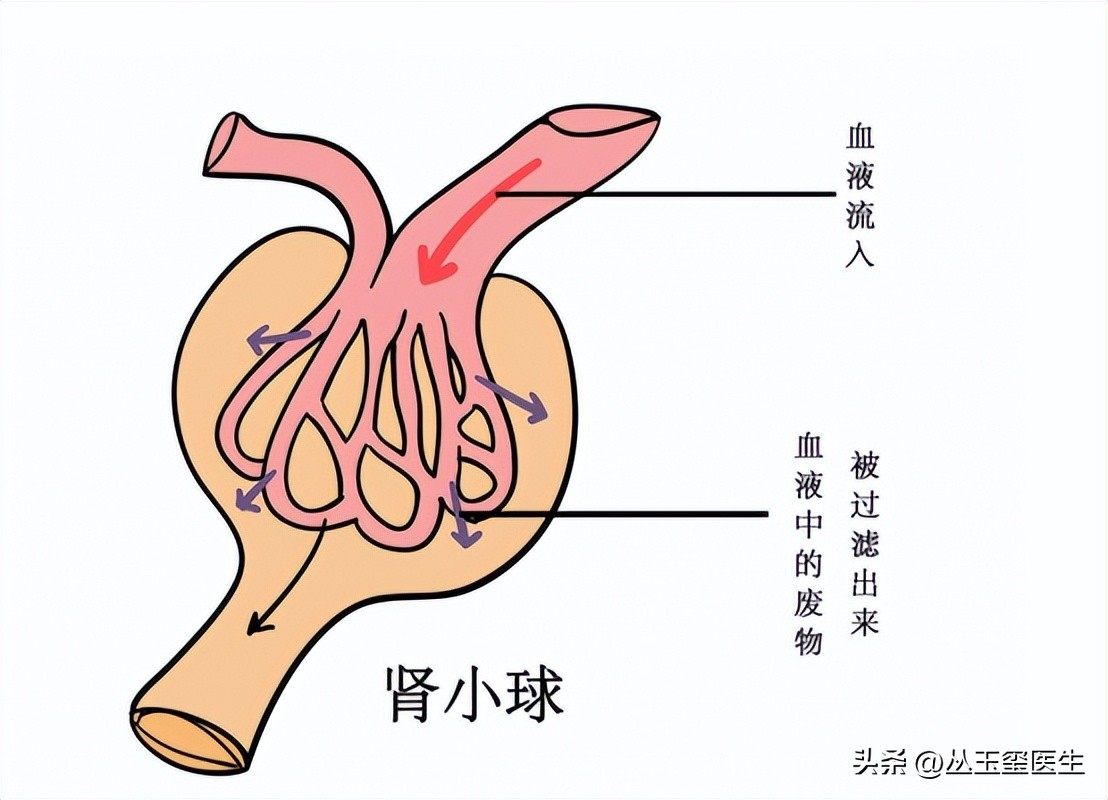
KDIGO 将 CKD-MBD 定义为CKD 导致的更广泛的全身性矿物质和骨代谢紊乱。CKD-MBD 具有普遍性、全身性、致残性、间接致死性的特点,已成为当前全球肾脏病界关注及研究的热点。CKD-MBD中最有代表性的表现之一就是SHPT。
一、定义
SHPT是慢性肾衰竭患者尤其是维持性血液透析不充分的患者一种比较常见的并发症,从形成机制上看,甲状旁腺长期受到低血钙等的影响,释放出更多的甲状旁腺激素,这种激素会对人体产生一系列负向影响。

随着透析龄的增加,SHPT的发病率不断升高。SPTH 的特点是促进 PTH 分泌和甲状旁腺细胞增生,SHPT最初表现为多克隆甲状旁腺细胞增殖。
随着病情的进展,甲状旁腺会发展为腺瘤样组织的进行性扩张,并由于维生素 D 和钙敏感受体的表达减少而对药物治疗产生抵抗。SHPT 可引起多种并发症,其可使钙磷代谢紊乱加重、纤维性骨炎、血管及软组织钙化,增加心血管事件和全因死亡风险。
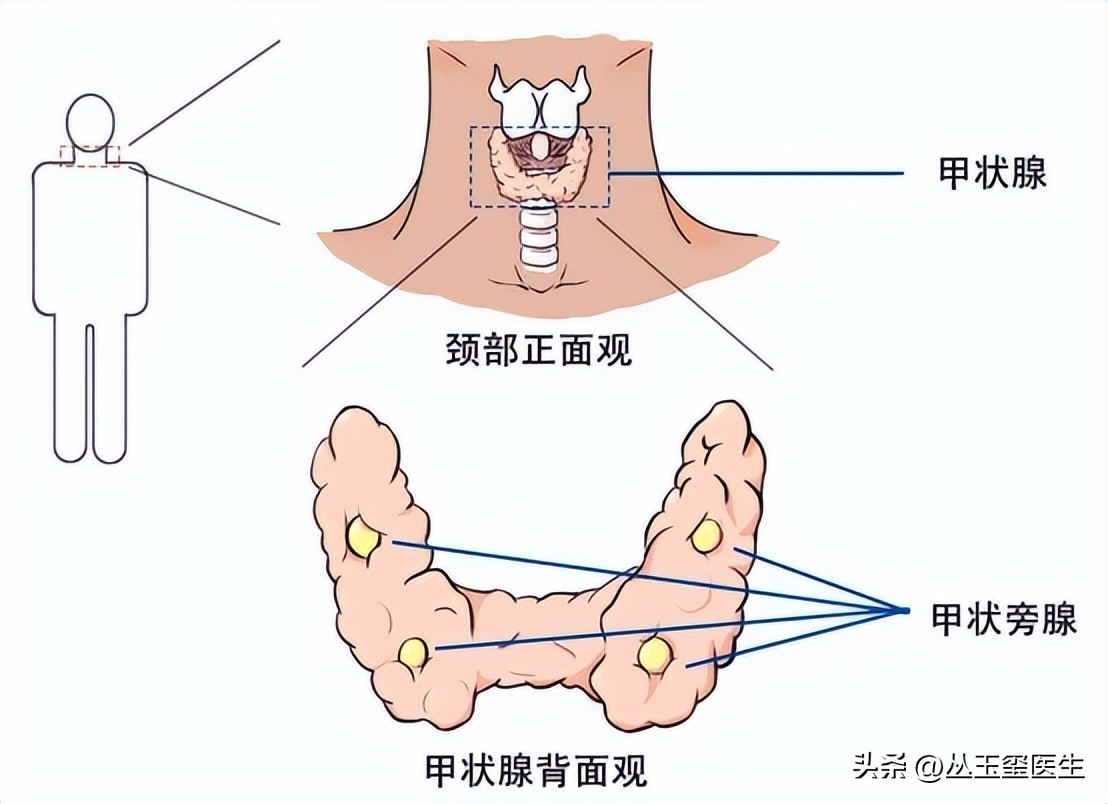
二、发病机制
SHPT 的发病机制源于 Bricker 倡导的一种基于甲状旁腺激素分泌亢进的权衡假说,这种 PTH 的过度分泌是对于纠正肾功能衰竭所致的钙磷代谢紊乱的生理反应。
在肾功能衰竭患者中,由于PTH通过肾脏控制的生理矿物质平衡失败,导致甲状旁腺功能亢进。具体有以下几点原因:①肾衰竭时,肾脏1α-羟化酶的活性减弱,导致活性维生素D3合成减少,降低的活性维生素D3引起低钙血症,刺激PTH持续产生。
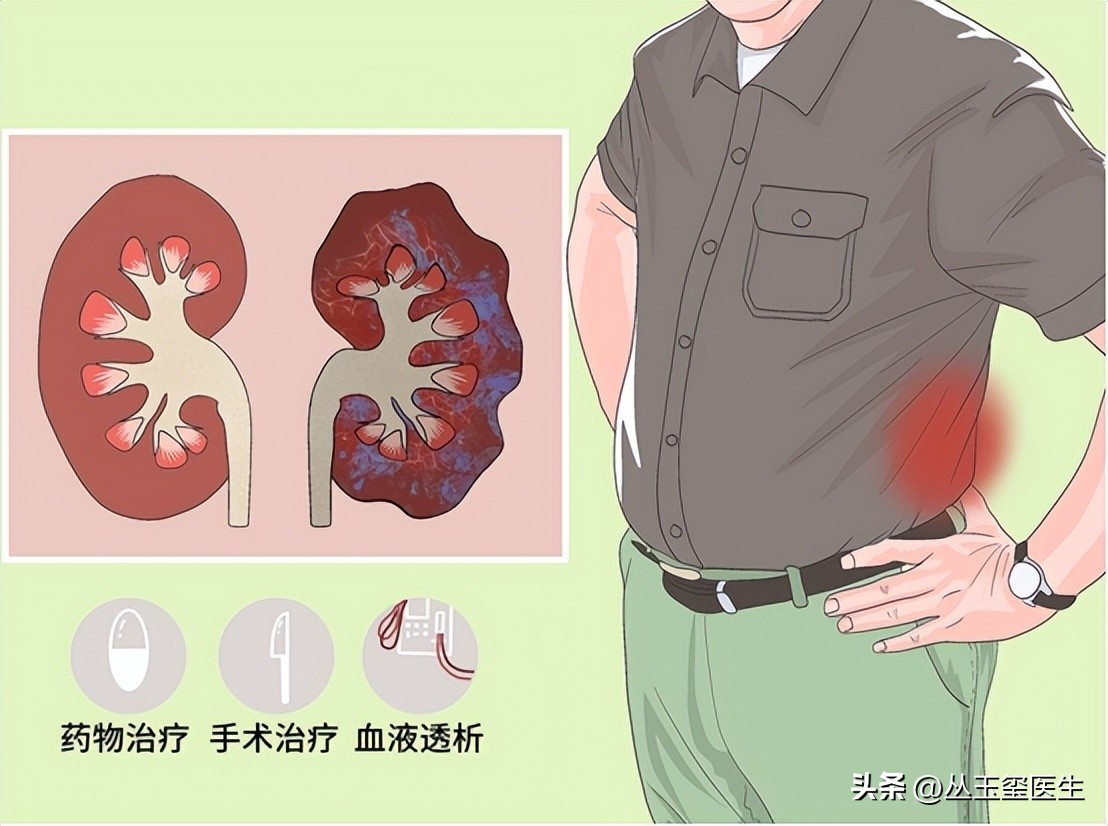
②高血磷直接刺激甲状旁腺细胞增殖和 PTH 的分泌,但由于甲状旁腺细胞培养困难,甲状旁腺中的磷感应系统仍然不为人所知。③细胞外 Ca 浓度是调节 PTH 分泌的主要因素,SHPT 中甲状旁腺对钙的敏感性改变。
④有学者经过大量的研究后指出,成纤维细胞生长因子 23(FGF23)对于 SHPT 形成起着重要的作用,FGF23 是近年来明确的磷调节激素。FGF23 在体内各部位分布,在 Koltho 共结合受体作用下与 FGFR 结合发挥生理作用。
三、临床表现
SHPT在CKD早期仅表现为血生化检查异常等,而这些症状不易被察觉,因此患者就诊时通常已发展为重症。而大量的实践经验显示,当其发展到一定程度后,ESRD 患者几乎全部发生肾性骨营养不良。
临床表现有:1.骨痛和骨折 2.肌病:以近端肢体肌无力最常见 3.关节炎和关节周炎 4.自发性肌腱破裂 5.骨骼畸形和生长迟缓 6.皮肤瘙痒:高PTH引起皮肤瘙痒的机制还不清楚,可能与细胞外液中钙浓度异常升高有关。7.转移性和骨外钙化。
四、检测与检查结果
PTH是一种由84个氨基酸组成的肽类激素,由甲状旁腺细胞分泌,与靶器官的甲状旁腺激素受体结合,激活细胞内信号以控制血钙和血磷的浓度,是评估SHPT的重要依据。
血液循环中的 PTH 分子包括全段 PTH 1-84(i-PTH)和 PTH降解后的片段-氨基端片段(N-PTH)、羧基端片段(C-PTH)等。全段 PTH1-84释放入血后极不稳定,半衰期仅有2-5min。
五、SHPT的综合治疗
1、控制高磷血症
(1)饮食控磷
几乎所有的食物都含有磷酸盐,但更多的磷酸盐存在于乳制品和各种肉类中,显著的饮食磷酸盐限制也会导致蛋白质的限制,严格的饮食限制可能并不可取。
我们注意到,肉类、蔬菜和谷物中的磷酸盐含量有较明显的差异,以谷物为基础的饮食具有较低的磷酸盐与蛋白质比率,而加工食品中有很多含有磷酸盐的添加剂,这些磷酸盐添加剂的生物利用度高于天然来源的磷酸盐,是一类容易被人们忽视的磷酸盐来源。

(2)充分透析
充分透析是促进磷排泄的重要措施。人体血液循环中的磷只占人体总体磷量的1%,剩下99%的磷存在于组织细胞内、骨骼和牙齿中,磷是高度水合物。
由于三个主要因素,无机磷有着类似于中间分子的特征:1.作为亲水性分子,无机磷被水性覆盖物包围,从而扩大其分子量。2.磷主要存在于细胞内,转移速率较慢。3.磷在细胞膜上的扩散不是一个自由的过程。
这些特征使得磷的透析动力学与尿素明显不同,更类似于中分子的透析动力学。血液透析治疗前2小时,磷进入透析液速率高,而随着透析的持续进行,透析除磷受制于磷从组织进入血清的速度,所以常规透析后,血磷水平在透析结束后的短时间内会出现显著反跳。
透析期间,透析处方的各种因素,如血液和透析液流量、透析器膜面积和超滤量都会影响透析期间的磷酸盐清除。现在可通过各种方式如血液透析滤过、高通量血液透析、增加透析频率和延长治疗时间来增加体内磷酸盐的清除。
有研究报道,长时间透析、每日透析或夜间透析可以提高磷的清除率,但这些方法受到的限制较多,比如透析资源的受限、人力资源不足、频繁夜班降低医务人员的工作效率等,无法得到广泛推广。
(3)磷结合剂
通过饮食控制和充分透析血磷仍不达标的患者建议使用磷结合剂,磷结合剂是治疗高磷血症的主要药物,这些药物的基本机制是通过活性阳离子如钙、镧、镁、铝、铁等与阴离子磷酸盐和七聚体交换,形成一种不被人体吸收的化合物。
随后通过粪便排出,有效减少胃肠道对膳食磷酸盐的吸收。磷结合剂的类型多年来不断发展,最早的含铝结合剂虽有明确的效果,但由于其存在铝中毒的风险,在当前的临床实践中基本不用于长期治疗。
含钙的磷结合剂随即被广泛使用,具体机制是其在体内与磷酸盐结合成难以被人体吸收利用的磷酸钙,从而达到降低血磷浓度的目的,然而需要注意的是,这种含钙的磷结合剂会导致明显的正钙负荷,而正钙负荷与加速血管钙化有关。
2、介入治疗及手术选择性
经皮乙醇注射疗法在此治疗领域很早就被引入,且积累了丰富的经验。这种方法治疗过程中,主要是超声下将乙醇注入增生的甲状旁腺腺体使其破坏,其余的腺体则继续药物治疗。
一般用于对药物治疗抵抗,血清学、影像学指标或骨活检诊断为高转运型骨病的患者,但这种治疗复发率高,增加再次手术的难度。在注射时也可选择活性维生素D,这样可以在短期内降低PTH,不过也容易导致复发问题。
腺体较大情况下疗效相对差,对结节性增生腺体效果差。当难治性 SHPT 用药物治疗没有明显的改善后,尤其在存在伴随性疾病如持续性高钙血症或高磷血症、组织或血管钙化或骨营养不良恶化时,就应考虑手术治疗。
1964 年第一例甲状旁腺大部切除术顺利完成,并取得良好的效果,在国外,该治疗方式得到逐步推广,且疗效显著。维持性透析超过 10 年的患者大约有 15%需要进行甲状旁腺切除术(PTx),透析超过 30 年的患者有 38%的比例需要手术治疗SHPT。
甲状旁腺切除术适用于 SHPT 患者对药物治疗效果不明显的患者。当透析患者的 PTH 水平达到 600-800pg/ml,再加上存在持续的高钙血症或高磷血症、骨质疏松的症状存在或难以纠正的贫血时,可以考虑行甲状旁腺切除术。
严重的继发性甲状旁腺功能亢进会表现为骨质疏松、关节疼痛、肌肉无力及顽固性瘙痒,导致患者的生活质量下降。在手术时可选择的术式主要包括次全切除术、全切除+自体移植术、全切除术等几种,其各有一定适用范围。
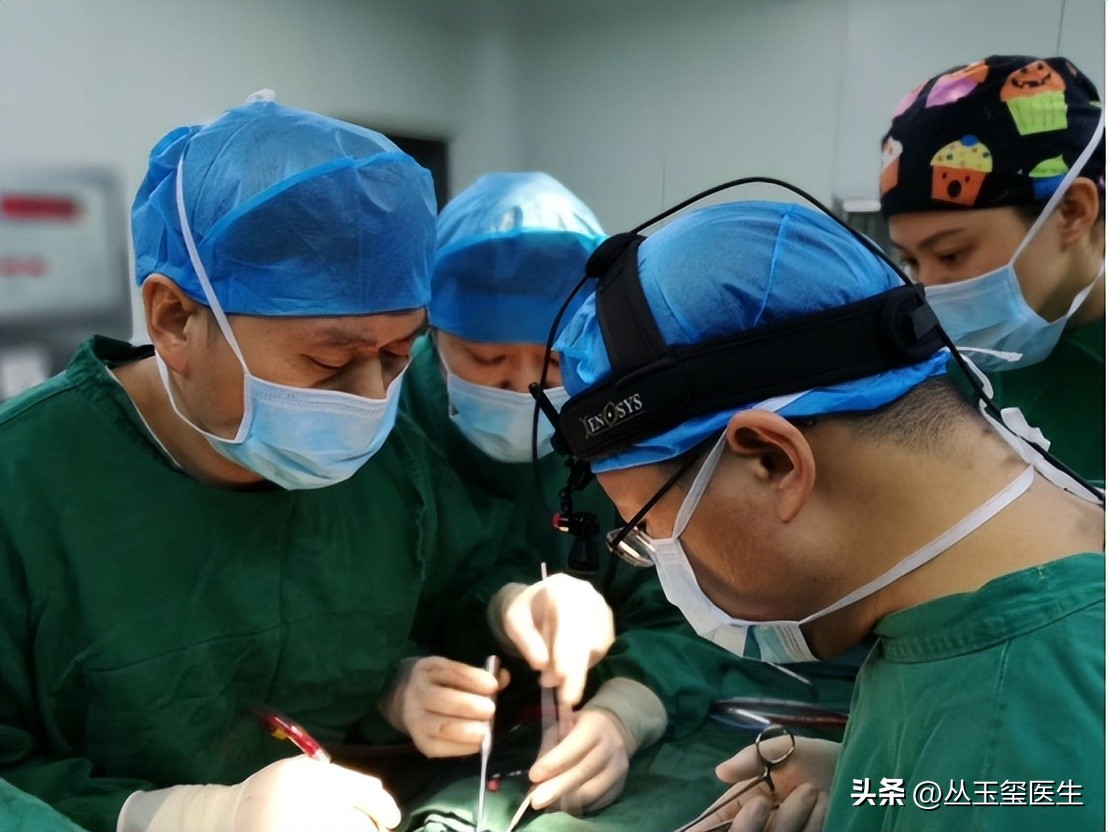
一些学者认为在没有移植情况下,可能会产生持续性低钙血症、骨伤难愈合相关的问题。而移植后也无法杜绝复发问题,因而存在一定的困扰。
一些则这对此进行深入研究,而提出折中的术式,近乎全切术,也就是在探查后结合切片结果,将很少一部分正常的腺体保留,其余的全部切除。此种方式手术效果及复发率比较还在进一步探讨中。
六、总结
PTX 术后也容易引发各种并发症,近期的可划分为外科与内科两方面,其中外科的如感染、血肿、神经损伤;内科的则如低钙血症等;远期并发症包括长期顽固的低钙血症、持续性 SHPT 及 SHPT 复发和低转运骨病等。
一些年老体弱难以耐受开放手术的患者,国内开展的超声引导下甲状旁腺微波热消融技术以其损伤小、效果好逐渐得到青睐,是一种安全、有效的治疗手段,但若不处理好所有的甲状旁腺,术后的复发率很高。