在阅读此文前,诚邀您点击一下 “关注” ,既方便您进行讨论与分享,又给您分享更多的专业健康知识,为您的健康保驾护航,感谢您的支持。
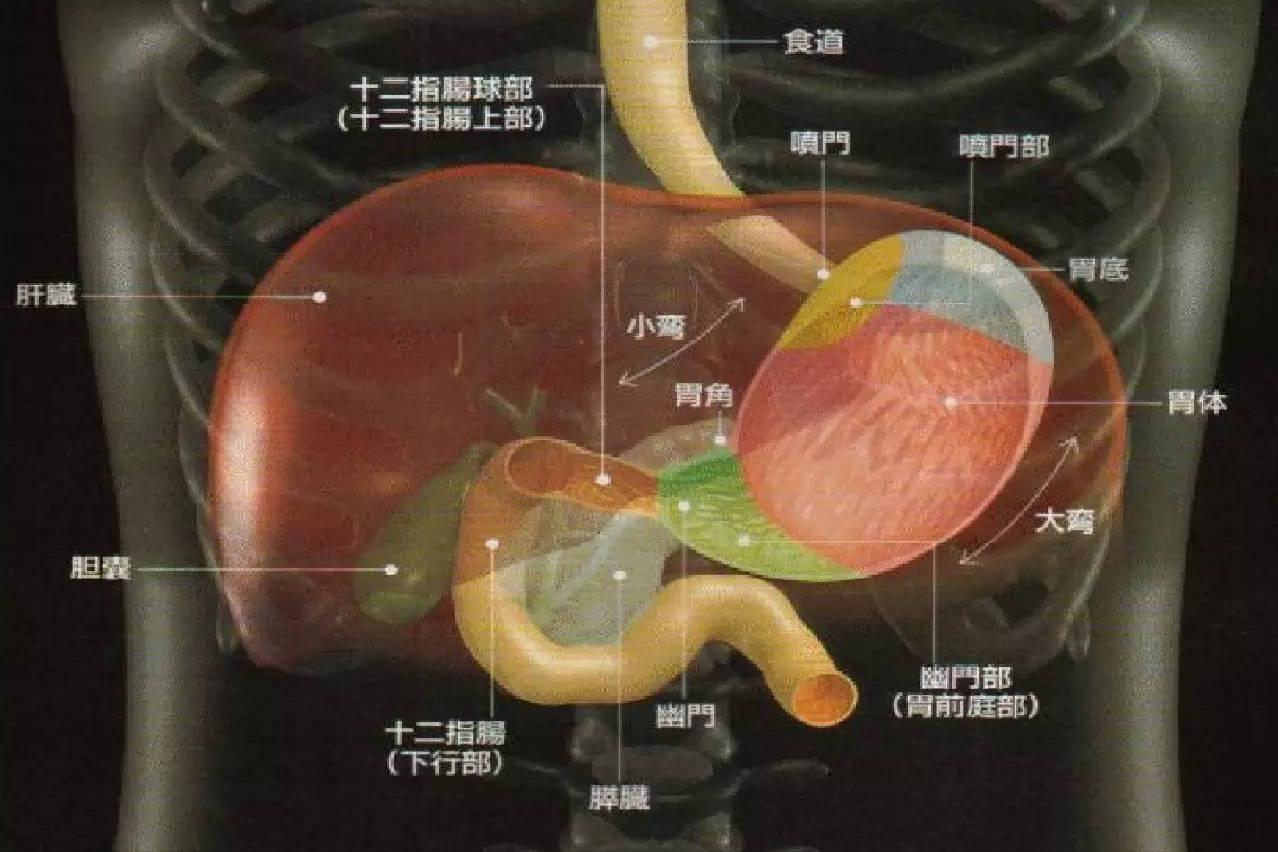
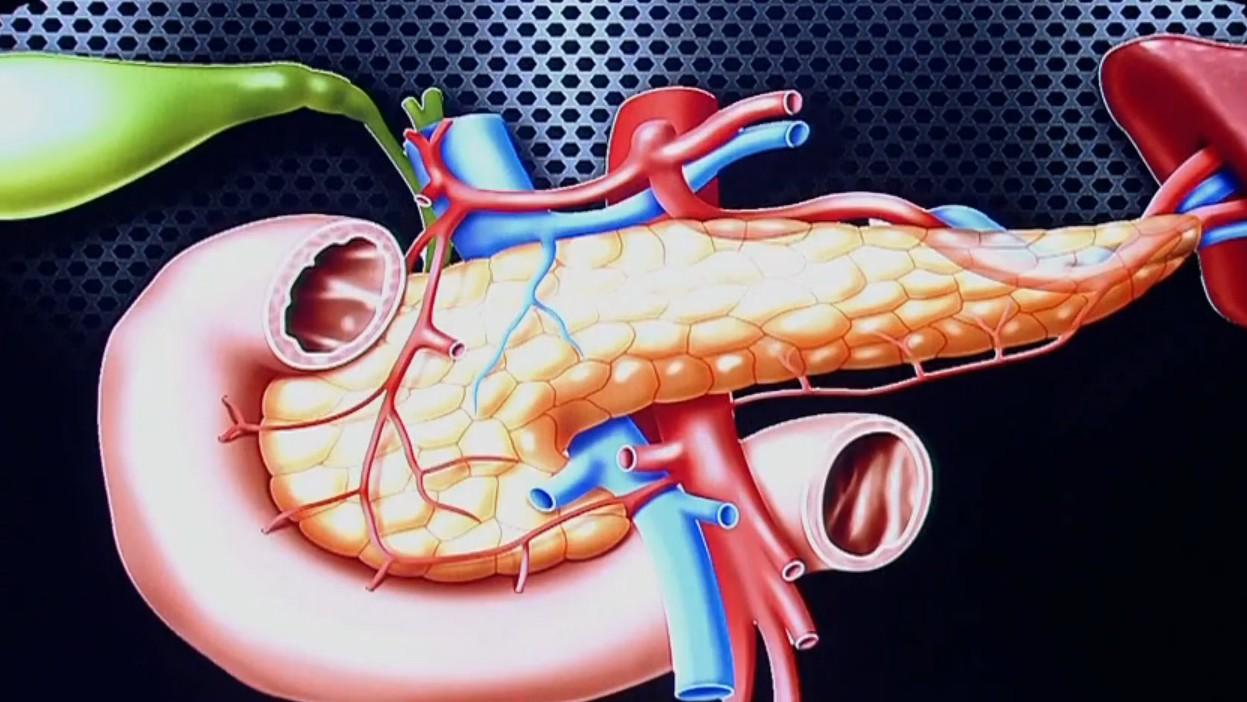
腹腔镜胰十二指肠切除术(laparoscopicpan-creaticoduodenectomy,LPD)在普外专业里是除了肝移植之外的第二大手术,是治疗壶腹周围肿瘤的经典术式,对术者及其团队在手术技术上有极高的要求。
胰十二指肠切除术(Pancreaticoduodenectomy,PD)从开腹发展至腔镜,历经了60余年,在1935年完成了首例PD手术。 1944年成功完成了不同于消化道重建的PD,首先进行胰肠吻合,后行胆肠吻合及胃肠吻合,此消化道重建术是目前临床广泛应用的Child法。
2003年成功完成了我国首例LPD,此手术采用经典的Child消化道重建方式,正式宣告我国进入全新的LPD时代。20年来,我国越来越多的胰腺中心积极尝试并成功完成了大量的LPD,获得了令人瞩目的成就。
LPD开展前期,举步维艰,遇到了各种挫折,术后出现各种严重并发症,住院周期长、住院费用高,其临床疗效备受质疑。

但近十年来,随着医疗水平的快速提高,3D腹腔镜、达芬奇机器人、超声刀在术中得到了广泛应用, 其中3D腹腔镜以其超清的视野,身临其镜的代入感,缝合操作的便捷性极大提高了腔镜手术的可操作性和安全性,LPD得到飞速发展。
近年来, 一线临床科研人员通过大量的临床数据已然证实了LPD的临床疗效等同于开腹手术,且腹腔镜对患者机体的应激反应及创伤更少,具有出血少、创伤小等显著优势。
但是, LPD术后并发症发生率与其他普外手术相比仍较高,例如:胰瘘、胆漏、出血、胃瘫等,与传统开腹手术相比并没有减少。
其中,胰瘘(PancreaticFistula,PF)是胰腺外科大夫最担忧的并发症之一,其发生率约3%-45%。胰瘘本身不严重, 其危险之处在于腹腔内淤积的胰液如果引流不畅,可造成周围组织坏死,易继发腹腔感染,胰瘘与腹腔感染在手术后相互影响。

胰液侵蚀血管可使血管破溃,引起出血,最严重可造成病人死亡。另外胰瘘会造成病人更长的住院周期,增加费用,会给患者家庭经济增加压力。
针对当前居高不下的PF发生率,胰腺外科大夫采用多种方案去降低PF的发生,PF的防治方案包括一方面及时发现胰瘘并对症处理,包括对腹水淀粉酶进行动态检测、全身营养支持、进行充分的引流及手术干预等;
另一方面则是术前或术中对术后胰瘘(PostoperativePancreaticFistula,POPF)发生的概率进行预测,提前采取:术前准备充分、术中操作精细、术后加强管理等积极的围术期预防策略。
各国胰腺外科中心在术后胰瘘相关危险因素的基础上,积极研究与探索,成功建立了多种POPF评分系统。

本文主要研究在2019年提出的改良版胰瘘风险评分(AlternativeFistulaRiskScore,a-FRS)系统, 其是一个能够预测POPF的系统,并成功验证了2005年和2016年的胰瘘双重诊断标准。
a-FRS系统对早期预测POPF有实际意义与临床价值。因此,研究LPD胰瘘的原因,有效规避其危险因素和提前预测术后胰瘘概率, 从而采取针对性防治胰瘘的策略,进一步降低患者术后死亡率。

十二指肠切除术的发展
1989年,全世界第一例胰头切除术在意大利开展,医生对此患者实施了胰头以及部分十二指肠切除术。 随后在1909年考施医生成功手术切除胰头肿物并完成了第一例胰肠吻合。
美国医生在1935年报道了因壶腹周围肿瘤而实施PD的病例,完成了全世界实际意义上的第一例PD手术, 此时将胰腺残端旷置封闭,并没有进行胰腺空肠吻合,随后在1942年首次一期完成了脏器切除联合消化道重建(先行胆肠吻合,后行胰肠吻合)。

这一手术方案大大促进了胰腺外科的发展,医学界将PD术命名为Whipple手术。1944年,Child成功地完成了与Whipple消化道重建不同的PD术, 先进行胰肠吻合,后行胆肠吻合及胃肠吻合,此消化道重建术是目前临床广泛应用的Child法。
1953年,新中国建立初期,我国普外科教授完成了国内首例PD术。1994年成功完成了全世界首例LPD,术后患者恢复情况良好。

2003年成功完成LPD,此手术采用经典的Child消化道重建方式,为我国首例LPD术,正式宣告我国进入全新的LPD时代。
20年来,我国越来越多的胰腺中心积极尝试并完成了大量的LPD术,并获得了令人瞩目的成就。现如今,LPD术已成为治疗壶腹周围肿瘤的经典手术,LPD在不同国家、不同地区被广泛应用。

胰瘘的定义和分级
胰瘘的定义为:各种因素导致胰腺导管上皮与其他上皮表面形成的异常通道,其通道内有源自胰腺分泌的消化酶液体。
2004年在一篇文献中报道了关于胰瘘的26种诊断标准,存在较大的差异,这种情况严重影响了各胰腺中心的交流,无法进行高效的学术沟通及数据共享,阻碍了临床的进展。为改变以上状况,国际胰瘘研究组在2005年系统且规范的对术后胰瘘进行了诊断和分级。

但随着临床实践和科学研究的发展,也暴露出局限和不足,如微创手术、介入治疗和康复医学的革新,原来的分级并不能满足现状。
经过十余年的临床实践、广泛的文献的核实,2016年国际胰腺外科研究组对胰瘘的诊断标准和分级进行了重新的修改,新的诊断标准为“术后≥3d,任意量的腹腔引流液淀粉酶值超过正常血清淀粉酶值上限的三倍,并且干预了临床治疗措施和进展”。

此定义突出了胰瘘的临床相关性,原来的*级A**胰瘘定义为生化漏。新的分级严格区分了B、C级胰瘘:B级胰瘘影响了临床治疗进展、干预了治疗措施,
包括因胰瘘导致腹腔引流管留置超过3周、使用内镜或介入治疗或引起腹腔感染;C级胰瘘是指在B级胰瘘的前提上,因胰瘘实施二次外科手术、导致单一或多个器官功能衰竭、造成病人死亡。

根据新的标准,两个等级均存在明显差异。2016年国际胰腺外科研究组重新制定的胰瘘定义和分级标准更为清晰、简明,该标准对生化漏定义明确,可对术后胰瘘进行更客观的评价。
此外,患者病情千变万化,更加细化的胰瘘分级仍十分必要,未来仍需要在临床实践中不断修改、补充和完善。

胰瘘的危险因素
有关LPD术后PF的危险因素,国内外已有大量研究报道 。目前认为引起术后胰瘘因素可能包括多方面: (1)患者自身相关因素:年龄、BMI、性别、术前白蛋白、术前血红蛋白、术前总胆红素、是否伴有其它合并症等; (2)胰腺情况:胰腺质地、胰管直径、病理类型等;

( 3)手术相关因素:胰肠吻合方式、是否放置胰管支撑管、手术时间、术中出血量等; (4)其他因素:是否使用生长抑素、围手术期管理、腹腔引流管拔除时间等。
胰瘘的风险预测发展及现状
近年来,随着外科学的不断发展,外科大夫在PD围手术期管理的相关经验越来越丰富,尝试通过各种方法去减少POPF的发生,但目前尚未找到行之有效的治疗方案。
因此,针对当前居高不下术后胰瘘发生率,治疗胰瘘的临床方案一方面是及时发现并治疗胰瘘, 另一方面是术前或术中及时地预测术后胰瘘风险、 识别POPF高危病人,在围术期采取积极的预防措施 。
各国胰腺外科中心在术后胰瘘危险因素的基础上,积极研究与探索,成功建立了多种POPF预测模型。

在2010年,法国学者发表一项关于胰瘘的预测模型,此研究结论提示, 胰瘘的相关独立危险因素为:1.体重指数≥25kg/m2;2.胰腺脂肪浸润;
3.胰腺纤维化程度,然后根据患者存在上述三种危险因素的不同数量去分为4个层级,随着层级升高,评估术后胰瘘风险概率也增高。 其中根据酒精性慢性胰腺炎胰腺纤维化的病理分级,确定胰腺脂肪浸润及胰腺纤维化的诊断标准。

但不理想的是, 胰腺纤维化及脂肪浸润程度需要一周左右时间等待术后病理结果,这对早期诊断和预防胰瘘有一定的影响。
2011年根据279例PD术后胰瘘(B级和/或C级)的情况,总结提出了日本国立癌症中心医院胰瘘评分系统(NCCH评分系统), NCCH评分系统一共包含5项相关指标,分别是主胰管指数、性别、是否是胰腺癌、门静脉是否受侵、腹腔内脂肪厚度。
其中主胰管指数指的是主胰管管径与胰腺体部最短直径之比; 门静脉侵犯定义为:手术之前,经影像学检查发现有肿瘤侵犯门静脉和(或)肠系膜上血管;
腹腔内脂肪厚度定义为:脐水平和腹直肌(腹白线)交点, 在此部位从腹腔内侧面(腹膜处)至腹主动脉后壁之间的距离。 上述指标和数据的获得,均是需要依靠术前CT和MRI的相关检查。

根据上述指标进行评分,每项因素被赋于一定分值,随后量化以上五项指标,并进行累计评分, 其中手术后发生胰瘘的危险程度最低为0分,手术后发生胰瘘的危险程度最高为7分 。 其中>4分为术后胰瘘高风险组,更应做好围手术期相关管理,≤4分定义为术后胰瘘低风险组。
NCCH评分预测系统注重术前对胰瘘的预测,指导临床医师在术前进行精确的胰瘘发生风险的评估, 对于高危人群在术中更应注意缝合打结、胰肠吻合质量,以及采用术后全身营养支持、腹腔充分引流等措施来最大程度预防术后胰瘘的发生。

2013年建立的一套胰瘘风险评分(FRS)系统,能够及时有效预测术后胰瘘,尤其是术后临床相关胰瘘(CR-POFF)的发生。 FRS系统是当前广泛应用的术后胰瘘风险预测模型。
2017年中华医学会的外科专家共识推荐了FRS评分系统, 本评分系统主要研究胰腺质地、术后肿物病理结果、主胰管直径、以及术中出血量四项相关因素, 该模型总分为10分,每个危险因子都有特定的分数,根据以上四种危险因子进行分类,最终将患者划分为四级:

可忽视风险等级(0)、低危等级(1-2分)和中危等级(3-6分)、高危等级为7-10分。高风险等级的患者几乎有100%的可能性发生CR-POPF。
该模型采用了术中及术后评估的方法,对CR-POPF的预测相比较于之前的胰瘘评分系统,其准确性较高。FRS系统中观察的指标囊括了术前、术中、及术后相关因素。 并且FRS系统简单易操作,临床医生对胰瘘的发生进行及时有效的预测,从而提前采取相应的治疗方案:

手术操作精细、放置双套管引流以及放置胰管支撑管等以减少胰瘘的发生。 在2019年提出的改良版胰瘘风险评分系统(a-FRS),其是一个能够预测CR-POPF的系统,并成功验证了2005年和2016年的胰瘘双重诊断标准,评分基于3个变量:胰管直径、胰腺质地和BMI。
a-FRS中的三个变量与胰瘘发生的相关性是临床研究公认的,a-FRS系统对早期预测CR-POPF更有实际意义与临床价值。a-FRS系统是基于大量临床数据建立起来。
与FRS系统中的四个变量相比,a-FRS不需要以术中出血量或术后病理为变量,首先失血量与手术质量及术者本人有关, 其次病理诊断需要一周时间等待术后病理出来,影响了对术后胰瘘的及时预测。 以上这些情况极大的降低了FRS系统的效率。
目前,a-FRS预测效果在2016版胰瘘诊断标准中等同于FRS。微创胰十二指肠切除术在近年来被各胰腺外科中心广泛应用, 其与开腹胰十二指肠切除术相比较,手术创伤小,对患者内环境影响小,具有术后恢复快的优势而越来越受欢迎。
在2019年建立了升级版改良胰瘘风险评分(ua-FRS)系统,它包含4个变量,其对微创胰十二指肠切除术后胰瘘的预测更加精细与准确。
ua-FRS系统相比较于a-FRS系统,性别变量被纳入。但是目前对于ua-FRS的合理性和可使用性,研究量本量较少,仍需要更多的胰腺外科中心使用大量数据去研究和验证。

当前,人们对POPF的病理生理水平的认识还不够透彻,以后仍需要深入研究胰瘘的发生机制,去建立更高效、更精准的胰瘘预测模型。
