
瘙痒是主人带犬去看兽医最常见的原因之一。有时瘙痒的原因很明显(例如,犬身上长满了跳蚤),有时则不是那么简单。继发性感染或(新的)过敏性皮肤病的发展可能使患者的原发病加重。如果有必要,兽医必须准备好“剥开”诊断层以找到潜在的原因——或多个原因。这篇文章提供了一个合乎逻辑的方法来检查瘙痒的犬。
引起瘙痒的主要疾病类别
虽然肯定有例外,但大多数引起犬瘙痒的情况分为三大类:感染、寄生虫和过敏(表1-3)。通常,同时存在1种以上的病症(例如,特应性皮炎患者也可能患有跳蚤和继发性酵母感染)。此外,瘙痒感可以被认为是一种附加现象,其中每种情况都建立在其他情况产生的不适之上。


图1.酵母足皮炎犬爪上的褐色变色。



图2.患有蠕形螨病的犬腹部(A)和前臂(B)的色素沉着、苔藓化和粉刺。这只犬接受了几个月的奥拉替尼治疗,同时服用了越来越多的糖皮质激素治疗过敏性皮炎。


图3.用显微镜聚光器向下(A)和向上(B)拍摄的犬蠕形螨。请注意当显微镜聚光镜降低时,清晰度和对比度显著增加

图4.深层皮肤刮擦显示成年蠕形螨(橙色箭头)、螨碎片(蓝色箭头)、若虫(黑色箭头)和卵(黄色箭头)。


图5.患有慢性跳蚤过敏性皮炎的犬的尾部脱发、色素沉着和疤痕。
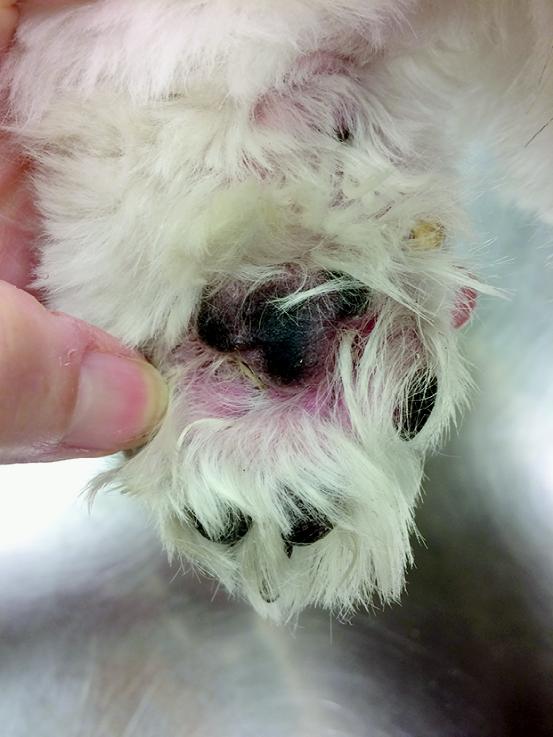

图6.食物过敏犬的腹部趾间(A)和腋窝(B)红斑和脱毛。

图7.食物过敏和特应性皮炎犬的耳廓红斑和化脓性创伤性皮炎。
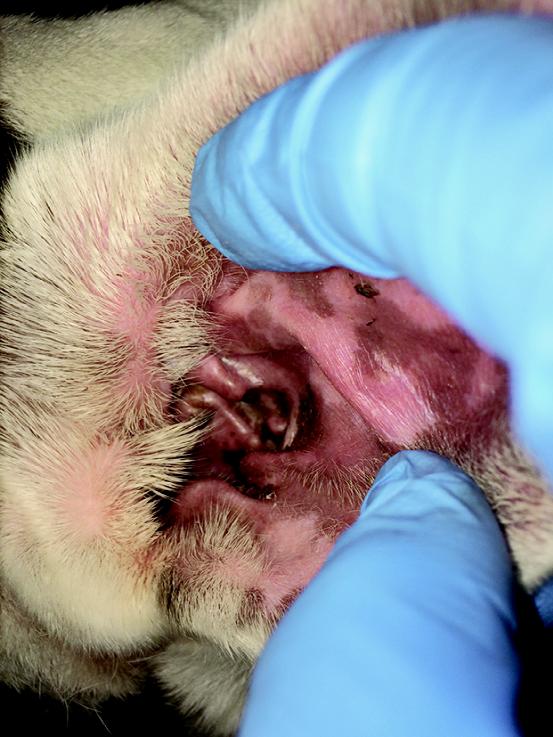
图8.过敏性中耳炎。即使没有明显的感染迹象,也要注意明显的红斑。
感染
与犬瘙痒相关的最常见的感染疾病是葡萄球菌性脓皮病和酵母菌皮炎(典型的是马拉色菌属,虽然念珠菌属也可见到,尽管很少)。皮肤癣菌病也可能与瘙痒有关,尽管不如细菌和酵母疾病常见。除了皮肤癣菌病,感染通常是瘙痒的次要原因。然而,任何微生物的过度生长或入侵都可能通过激活和募集炎性细胞而触发皮肤中非特异性炎症反应的产生,这些炎性细胞随后释放炎性和致瘙痒物质。这些事件一起诱发或增强了瘙痒感。表1描述了瘙痒最常见的感染原因及其分布。
寄生虫
通常与犬瘙痒的发展或持续有关的寄生虫可分为寄生在皮肤表面、皮肤表层(如角质层和表皮)或皮肤深层(尤其是毛囊)的寄生虫。
l生活在地表的寄生虫包括跳蚤、虱子、耳螨和姬螯螨,以及恙螨。
l浅表寄生虫包括疥螨。
l深层寄生的寄生虫包括犬蠕形螨和隐在蠕形螨。
其他昆虫和螨虫也可能通过直接寄生以外的方式导致瘙痒,包括蚊子、稳定的苍蝇(口蝇)和黑苍蝇(蚋)。表2描述了与寄生虫相关的皮炎的典型临床表现和分布以及相关的诊断技术。
过敏
与犬瘙痒相关的3种最常见的过敏是跳蚤过敏、食物过敏(有时称为食物不良反应)和特应性(或特应性皮炎)(表3)。犬可能会受到一种或多种这些情况的影响,甚至同时受到三种影响。犬也可能经历接触过敏,虽然不像其他3种过敏情况那样常见。除跳蚤过敏外,其他过敏性疾病的检查比感染性和寄生虫性疾病的检查更复杂。由于这个原因,对过敏的深入检查常常被推迟,直到瘙痒的非过敏性原因被识别和控制或消除。
诊断工具
初次就诊
细胞学:瘙痒犬的初步检查至少应包括皮肤和/或耳朵细胞学检查。
皮肤刮片:瘙痒犬的初始检查还应包括受影响区域的皮肤刮片。浅表皮肤刮片可能显示许多表面和浅表螨虫;深层皮肤刮屑可能显示蠕形螨。
跳蚤梳梳理和/或表面胶带采样:检查通过跳蚤梳理或表面胶带采样获得的碎片可能有助于证明表面栖息的螨虫、跳蚤、“跳蚤污垢”和虱子。
跳蚤控制:积极的跳蚤控制是检查和管理瘙痒犬的重要部分。作者认为,即使在跳蚤被认为不常见的地区,建立跳蚤控制试验计划也是值得的。考虑到气候变化和节能住宅的潜在影响,这一点尤其正确,因为节能住宅可以最大限度地减少温度、湿度等季节性变化的影响。,创造可能更有利于跳蚤生存的微环境。
即使跳蚤过敏被认为不是一种可能的诊断,也应将跳蚤控制纳入瘙痒犬的检查中,因为跳蚤及其叮咬即使在非过敏患者中也会产生刺激。提供可用代理的详细讨论超出了本文的范围,但也提供了其他资源。作者特别喜欢异恶唑啉类药物;然而,在某些情况下(例如,已有神经系统疾病或癫痫发作史的患者),这些药物应谨慎使用。对于这些患者,其他药物(例如,每月一次的呋虫胺或茚虫威或每周一次的吡虫啉)可能就足够了。
为了确保正确使用跳蚤控制产品,仔细询问顾客他们目前的跳蚤控制措施。具体询问可能与患者接触的其他动物的存在和治疗情况。还要询问犬是否暴露在跳蚤可能传播的环境中(例如,犬公园、小犬日托)。在跳蚤控制试验期间,自由活动的动物应该被限制在一个受控的空间内。应采取措施确保犬和接触的动物无法进入开放的棚舍、爬行空间等。野生动物可能会在这些地区传播跳蚤。在严重感染的情况下(或者如果临床症状特别提示跳蚤过敏),可能需要对环境进行处理。事实上,许多从业者认为环境跳蚤控制在易受严重跳蚤侵扰的地理区域(例如,美国东南部)是至关重要的。环境跳蚤控制措施可以包括经常用真空吸尘器清扫犬接近的区域,以及用昆虫生长调节剂(例如,吡丙醚)喷洒家庭。
可能有用的其他诊断
伍德氏灯检查、皮肤癣菌培养、皮肤癣菌聚合酶链反应试验或仔细检查拔毛(毛发图):如果怀疑有皮肤癣菌病,这些方法都可能有帮助。
培养和药敏试验:对于有反复抗生素用药史、深部脓皮病或经验性抗生素治疗无效的患者,考虑细菌培养和药敏试验。
活检:对于经过适当的抗微生物和抗寄生虫治疗后仍无改善的患者,可以考虑进行皮肤活检。皮肤活检不能代替评估患者的传染性、外寄生虫性和(其后)过敏性疾病。虽然组织学可以证明一些感染情况(如皮肤真菌病、蠕形螨病),但这通常不是最有效的方法。组织学本身无法区分本文中描述的许多情况。尽管如此,考虑到这些限制,活检可以提供更多的信息,并有助于排除瘙痒的更深奥的原因,如皮肤淋巴瘤。作者通常为对适当治疗无反应的患者或具有非典型表现的患者(例如,持续性弥漫性红斑或鳞屑、溃疡、涉及粘膜皮肤连接)保留活检。
诊断方法
1.全面了解病史
为了评估一只瘙痒的犬,一份完整的病史是非常宝贵的。良好的病史可以帮助兽医指出可能的诊断,同样重要的是,远离不可能的诊断。表4显示了询问皮肤病史时要问的问题,一些后续问题,以及从回答中获得的信息的简要概述。

2.进行身体和皮肤检查
每一只瘙痒的犬都应该接受彻底的身体和皮肤检查。涵盖所有可能的相关发现超出了本文的范围;但是,有些领域的评估尤为重要。这些区域是背侧和腹侧趾间皮肤、爪和爪床周围的皮肤、肛周和会阴皮肤、肘部褶皱和腹侧唇褶皱。此外,直肠检查适用于任何患有尾部瘙痒症的患者,因为一些肛门囊嵌塞的患者会舔或咀嚼尾部,而不是瘙痒。评估出现红斑、脓疱、青铜色(特别是在爪子上)或潮湿或油腻皮炎的区域可能特别有用。表1-3列出了一些更常见的鉴别诊断、这些情况的典型分布以及相关的诊断技术。
3.首先确定并消除感染性和外寄生性病因
尽管确实有很大比例的瘙痒犬患有1种或多种类型的过敏性皮肤病,但最好还是先对患者进行评估,看是否有感染性或寄生虫引起的瘙痒。除了跳蚤过敏(积极控制跳蚤的机构总是被指示),食物过敏或特应性皮炎的检查在第一次检查时可能被指示,也可能不被指示。如果发现明显的跳蚤、细菌或酵母菌感染,排除这些情况可能会对患者的真实情况提供更好的基线评估。
首先识别和排除感染性和外寄生虫疾病的另一个原因是因为它们通常更容易识别和治疗,而过敏性皮肤病的彻底检查可能相当昂贵和漫长。此外,由于瘙痒可能是所有因素共同作用的结果,未能消除非过敏性疾病可能会干扰对患者病情的准确评估,从而可能扭曲过敏检查的结果。尽管传染性和寄生虫性疾病共同代表了大量的潜在鉴别诊断,但大多数此类疾病可以通过使用相对较少的诊断和治疗技术快速、经济地鉴别出来(表1、2)。如果在消除感染或寄生虫后瘙痒持续存在,则需要进行过敏性皮肤病检查。
在第一次就诊时,通常需要进行某种形式的抗炎治疗。瘙痒行为造成皮肤微创伤,导致炎症介质的释放,有利于感染的发展和持续。尽管抗炎药物可能会在短期内干扰对患者状况的评估,但炎症的减轻不仅为患者提供了缓解,而且使受创伤的皮肤得以愈合,并有助于消除继发感染。
4.治疗和重新评估
重新评估是检查瘙痒犬的一个重要部分。太多时候,兽医在最初的诊断和治疗进行并开出处方后几个月去看患者,却被告知治疗“不起作用”。有时,患者在初始治疗后确实有所改善,但在最初开出的药物用完后又开始恶化。如果患者此时不采取行动,病情很可能会继续恶化,当患者再次寻求兽医护理时,瘙痒的短暂缓解可能会被遗忘很久。作者建议主人在初次就诊后2-3周内通过电话或网络进行复查或登记。如有必要,兽医或兽医护士可以主动联系。在药物治疗结束之前,还应该对患者进行复查,以确认感染/侵袭的消退。如果患者有所改善,那么就有可能开始过敏性皮肤病的检查。如果患者没有充分改善,可能需要延迟检查,并进一步评估(或重新评估)患者是否存在或复发感染或寄生虫。
5.对过敏性瘙痒性皮肤病进行检查
跳蚤过敏
如上所述,无论跳蚤过敏是否被认为是一种诊断,良好的跳蚤控制在任何瘙痒犬的检查中是重要的。幸运的是,现代跳蚤控制剂已经使消灭跳蚤成为可能,除了最具挑战性的情况。无论选择何种药剂,对患者和所有接触动物的治疗必须维持至少12周,以确保跳蚤已经被消灭。
食物过敏
许多市售的“诊断工具”用于食物过敏的诊断,包括血清IgE、粪便IgE或唾液食物特异性IgE的测量。不幸的是,这些方法既不能可靠地诊断食物过敏,也不能识别有问题或可耐受的食物。斑贴试验和淋巴细胞刺激试验可能有一定的用途,但通常仅限于研究机构或学术机构。迄今为止,诊断食物过敏和识别致病食物的唯一实用方法是饮食排除试验。
排除试验可以通过使用水解饮食(加工以最小化肽大小)或新型蛋白质饮食(商业或家庭烹饪)来进行。这两种方法都有效,但都不能保证成功。如果水解蛋白饮食用于诊断目的,超水解饮食(1-2千道尔顿片段)被认为优于半水解饮食(约10千道尔顿片段)。超水解饮食中的小肽片段使得临床反应不太可能(但仍有可能),即使该饮食来源的蛋白质是患者以前喂养过的蛋白质。如果需要,可以从不同的蛋白质来源中选择超水解饮食(例如,对于以前喂过鸡肉的患者,可以选择基于鲑鱼的饮食)。然而,即使这种方法也有其局限性,因为最近的研究表明,在令人惊讶的完全不同的来源,如鱼和鸡之间,可能存在过敏交叉反应。
如果选择了新的蛋白质饮食,应回顾患者的饮食史,以确定患者接触过的饮食项目。适当的饮食应该包括与患者以前饮食中的成分在系统发育上有很大差异的成分。例如,对于以前喂过鸡的犬来说,以袋鼠或鳄鱼为基础的饮食可能是一个很好的经验性选择。同样,交叉反应仍然是这些饮食的潜在限制。
选择饮食只是饮食排除试验的一部分。主人还必须确保犬不会从其他来源获得食物或基于食物的物品,包括家中其他动物吃的食物、餐桌残羹剩饭、掉落的食物、基于食物的咀嚼玩具(生皮、蹄子)和零食。通常被忽视的食物来源是咀嚼药物(包括心丝虫和跳蚤预防剂)、动物粪便、舔其他动物的食物碗和水槽中的脏盘子。
对于饮食试验所需的时间长度没有达成共识。最近的一篇综述文章建议至少用8周时间来确定95%的食物过敏患者;在少数犬中,直到第13周才发现食物过敏。至少在试验的前几周,提供抗炎/止痒支持(如泼尼松龙)可能是谨慎的。这样做不仅是为了患者的福利,也是因为一些证据表明,皮肤炎症的早期抑制可能会缩短饮食试验的必要时间。理想情况下,所有消除饮食后,应使用犬以前的饮食再次刺激,即使犬没有变得无症状。刺激后临床疾病的恶化既证实了无症状犬中食物过敏的诊断,也表明犬中的食物过敏成分在试验期间仅表现出部分改善。恢复消除饮食后临床症状的缓解进一步巩固了诊断。
特应性皮炎
特应性皮炎最好被认为是一种综合征,而不是一种特殊的诊断。这种疾病通常与对环境过敏原过敏有关。此外,瘙痒的附加性质意味着其他刺激或过敏因素(如感染、跳蚤、食物过敏)的存在可引发特应性皮炎的临床发作。这种超敏反应可能是IgE介导的,尽管对于一些受到相同影响的患者,血清学或皮内试验无法证明过敏原特异性IgE。这些患者被称为患有“特应性样皮炎”
最近,已经制定了两套标准来帮助兽医诊断特应性皮炎(框 1)。就其本身而言,这些标准不能证明患者患有或不患有特应性皮炎,也不能代替适当的检查来确定和消除特应性皮肤炎的其他潜在原因。然而,他们确实提供了关于哪些临床症状(以及症状的组合)最能支持特应性皮炎诊断的有用信息。可以使用任意一组标准。第一组相对敏感,具有中到高的特异性;第二组不敏感,但具有高度到非常高的特异性。

由于许多潜在的致病因素,谨慎的做法是在诊断特应性皮炎之前,确保排除所有合理的诊断,或(在同时患有过敏性皮肤病的情况下)对其进行控制。由于这个原因,特应性皮炎被认为是一种临床诊断的排斥。尽管过敏试验(血清学或皮内试验)经常用于“诊断”特应性皮炎,但这些诊断不能可靠地区分健康犬和特应性犬,只能支持特应性的临床诊断。
虽然过敏试验本身不能诊断特应性,但它有助于识别潜在的过敏原触发点,以便尝试脱敏。首选的诊断试验通常是皮内试验,因为它模拟了过敏原与患者之间的相互作用。然而,皮内试验并不总是可行或实用的,在这种情况下,良好的血清学试验可以提供有用的信息。由于实验室方法的差异会显著影响血清学检测结果,建议在选择实验室前咨询兽医皮肤科医生。
结论
犬类瘙痒的鉴别诊断数量似乎多得令人应接不暇。然而,遵循一些简单的准则可以极大地方便检查。
- 获得良好的病史记录——提问而不是假设主人已经告诉了你所有相关的事情。
- 在进行过敏性皮肤病检查之前,首先筛查患者瘙痒的感染性或寄生虫性原因。
- 治疗和重新评估——评估对初始治疗的反应,以帮助避免根据患者记忆(失误)做出决定,并更好地了解患者的真实基线。
- 把特应性皮炎留到最后。除非患者表现出纯粹的季节性瘙痒,首先要调查感染、外寄生和食物过敏。即使是单纯季节性瘙痒的患者,也应评估是否存在季节性寄生虫,如跳蚤和恙螨。
参考文献
1. Hensel P, Santoro D, Favrot C, et al. Canine atopic dermatitis: detailed guidelines for diagnosis and allergen identification. BMC Vet Res. 2015;11:1–13.
2. Miller WH Jr, Griffin CE, Campbell KL. Diagnostic methods. In: Miller WH Jr, Griffin CE, Campbell KL, eds. Muller and Kirk’s Small Animal Dermatology. St. Louis, MO; Elsevier Mosby; 2013:57–107.
3. Bond R, Morris DO, Guillot J, et al. Biology, diagnosis and treatment of Malassezia dermatitis in dogs and cats; clinical consensus guidelines for the World Association for Veterinary Dermatology. Vet Dermatol. 2020;31(1):73–77.
4. Moriello K. Feline dermatophytosis: aspects pertinent to disease management in single and multiple cat situations. J Feline Med Surg. 2014;16(5):419–431.
5. Moriello KA, Coyner K, Paterson S, Mignon B. Diagnosis and treatment of dermatophytosis in dogs and cats. Vet Dermatol. 2017;28(3):266–e68.
6. Miller WH Jr, Griffin CE, Campbell KL. Parasitic skin disease. In: Miller WH Jr, Griffin CE, Campbell KL, eds. Muller and Kirk’s Small Animal Dermatology. St. Louis, MO: Elsevier Mosby; 2013:284–342.
7. Olivry T, Mueller RS. Critically appraised topic on adverse food reactions of companion animals (7): signalment and cutaneous manifestations of dogs and cats with adverse food reactions. BMC Vet Res. 2019;15(1):140.
8. Favrot C, Steffan J, Seewald W, Picco F. A prospective study on the clinical features of chronic canine atopic dermatitis and its diagnosis. Vet Dermatol. 2010;21(1):23–31.
9. Hill PB, Lo A, Eden CAN, et al. Survey of the prevalence, diagnosis and treatment of dermatological conditions in small animals in general practice. Vet Rec. 2006;158(16):533–539.
10. Scott DW, Paradis M. A survey of canine and feline skin disorders seen in a university practice: Small Animal Clinic, University of Montréal, Saint-Hyacinthe, Québec (1987-1988). Can Vet J. 1990;31(12):830–835.
11. Chiu IM. Infection, pain, and itch. Neurosci Bull. 2018;34(1):109–119.
12. Crkvencic N, Šlapeta J. Climate change models predict southerly shift of the cat flea (Ctenocephalides felis) distribution in Australia. Parasit Vectors. 2019;12(1):137.
13. Pucheu-Haston C. The flea-infested pet: overview of current products. Todays Vet Pract. 2017;7(3):90-95.
14. Rust MW, Dryden MW. The biology, ecology and management of the cat flea. Annu Rev Entomol. 1997;42:451–473.
15. Gross TL, Ihrke PJ, Walder EJ, Affolter VK. Perivascular diseases of the dermis. In: Gross TL, Ihrke PJ, Walder EJ, Affolter VK, eds. Skin Diseases of the Dog and Cat: Clinical and Histopathologic Diagnosis. Oxford, UK: Blackwell Science; 2005:200–237.
16. Rybnicek J, Lau-Gillard PJ, Harvey R, Hill PB. Further validation of a pruritus severity scale for use in dogs. Vet Dermatol. 2009;20(2):115–122.
17. Griffin CE, DeBoer DJ. The ACVD task force on canine atopic dermatitis (XIV): clinical manifestations of canine atopic dermatitis. Vet Immunol Immunopathol. 2001;81(3-4):255–269.
18. Mueller RS, Olivry T. Critically appraised topic on adverse food reactions of companion animals (6): prevalence of noncutaneous manifestations of adverse food reactions in dogs and cats. BMC Vet Rec. 2018;14(1):341.
19. James DJ, Griffin CE, Polissar NL, Neradilek MB. Comparison of anal sac cytological findings and behaviour in clinically normal dogs and those affected with anal sac disease. Vet Dermatol. 2011;22(1):80–87.
20. Mueller RS, Olivry T. Critically appraised topic on adverse food reactions of companion animals (4): can we diagnose adverse food reactions in dogs and cats with in vivo or in vitro tests? BMC Vet Res. 2017;13(1):275.
21. BethlehemS,BexleyJ,MuellerRS.Patchtestingandallergen-specific serum IgE and IgG antibodies in the diagnosis of canine adverse food reactions. Vet Immunol Immunopathol. 2012;145(3-4):582–589.
22. Fujimura M, Masuda K, Hayashiya M, Okayama T. Flow cytometric analysis of lymphocyte proliferative responses to food allergens in dogs with food allergy. J Vet Med Sci. 2011;73(10):1309–1317.
23. Olivry T, Bexley J, Mougeot I. Extensive protein hydrolyzation is indispensable to prevent IgE-mediated poultry allergen recognition in dogs and cats. BMC Vet Res. 2017;13(1):251.
24. Bexley J, Kingswell N, Olivry T. Serum IgE cross-reactivity between fish and chicken meats in dogs. Vet Dermatol. 2019;30(1):25–e8.
25. Olivry T, Mueller RS, Prelaud P. Critically appraised topic on adverse food reactions of companion animals (1): duration of elimination diets. BMC Vet Res. 2015;11:225.
26. Favrot C, Bizikova P, Fischer N, et al. The usefulness of short-course prednisolone during the initial phase of an elimination diet trial in dogs with food-induced atopic dermatitis. Vet Dermatol. 2019;30(6):498–e149.
27. Olivry T, DeBoer DJ, Favrot C, et al. Treatment of canine atopic dermatitis: 2015 updated guidelines from the International Committee on Allergic Diseases of Animals (ICADA). BMC Vet Res. 2015;11:210.
28. Halliwell REW. Revised nomenclature for veterinary allergy. Vet Immunol Immunopathol. 2006;114(3-4):207–208.
29. Lauber B, Molitor V, Meury S, et al. Total IgE and allergen-specific IgE and IgG antibody levels in sera of atopic dermatitis affected and non- affected Labrador- and Golden retrievers. Vet Immunol Immunopathol. 2012;149(1-2):112–118.
30. Plant JD, Neradelik MB, Polissae NL, et al. Agreement between allergen-specific IgE assays and ensuing immunotherapy recommendations from four commercial laboratories in the USA. Vet Dermatol. 2014;25(1):15–e6.
