编者按
目前,免疫检查点*制剂抑**(ICIs)已成为肿瘤治疗领域的突破性进展之一。但随着ICIs的广泛应用,这类药物的不良反应也引起了临床的重视。在12月3日举行的第九届华夏上海肝病论坛-上海国际肝病高峰论坛暨肝衰竭及其并发症诊治进展论坛上,首都医科大学附属北京地坛医院肝病中心谢雯教授进行了“肝癌靶向免疫治疗的肝损伤和治疗”的专题汇报,就临床最关心的肝癌免疫治疗的难点和困惑点一一解答。国际肝病特将报告内容整理如下,以飨读者。
目前,肝癌的治疗以多学科参与、多种治疗方法共存为特点,治疗方案包括肿瘤切除、肝移植、消融治疗、肝动脉插管化疗栓塞(TACE)、放疗和系统抗肿瘤治疗等。对于不同分期的肝癌患者,需采取不同的治疗手段,以最大程度地使患者受益。
在肿瘤发展的早期,由于肿瘤细胞尚未扩散至肝外区域,手术、肝移植等局部治疗方法可取得较好效果。一旦发展到晚期,肿瘤出现转移,系统治疗则成为优选方案。用于系统治疗的药物主要包括化疗药物、靶向治疗药物、免疫治疗药物等。其中免疫治疗近年在肿瘤治疗中风头正盛,在肝癌治疗中同样也势头强劲,已逐渐成为目前临床研究的热点。

图1. 中国肝癌临床分期与治疗路线图[1]
免疫检查点*制剂抑**的作用机制
肝癌的发生发展及远处转移机制十分复杂,免疫功能紊乱是一个重要因素。而ICIs的治疗可通过阻滞某些特定的通路来抵抗疾病(如肿瘤),已经成为肝癌领域的重要治疗手段。因程序性细胞死亡蛋白及其配体(PD-1/PD-L1)和细胞毒性T淋巴细胞相关抗原(CTLA-4)在肿瘤微环境中经常表达增高,这两者常作为ICIs的主要的靶点 。
表1. 美国FDA批准上市的免疫检查点*制剂抑**
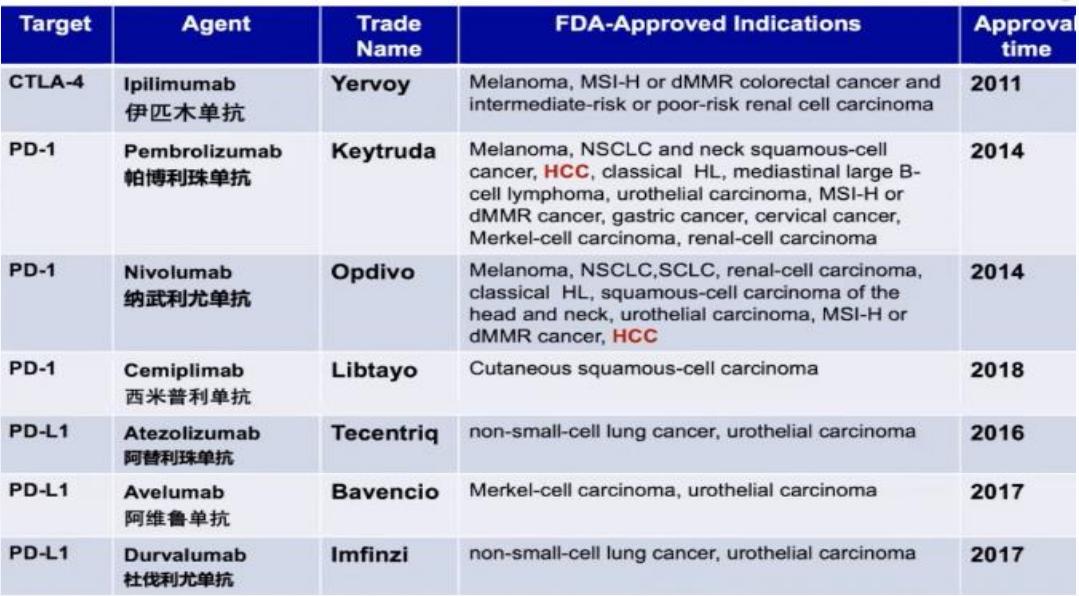
(引自讲者幻灯)
表2. 已上市的国产免疫检查点*制剂抑**
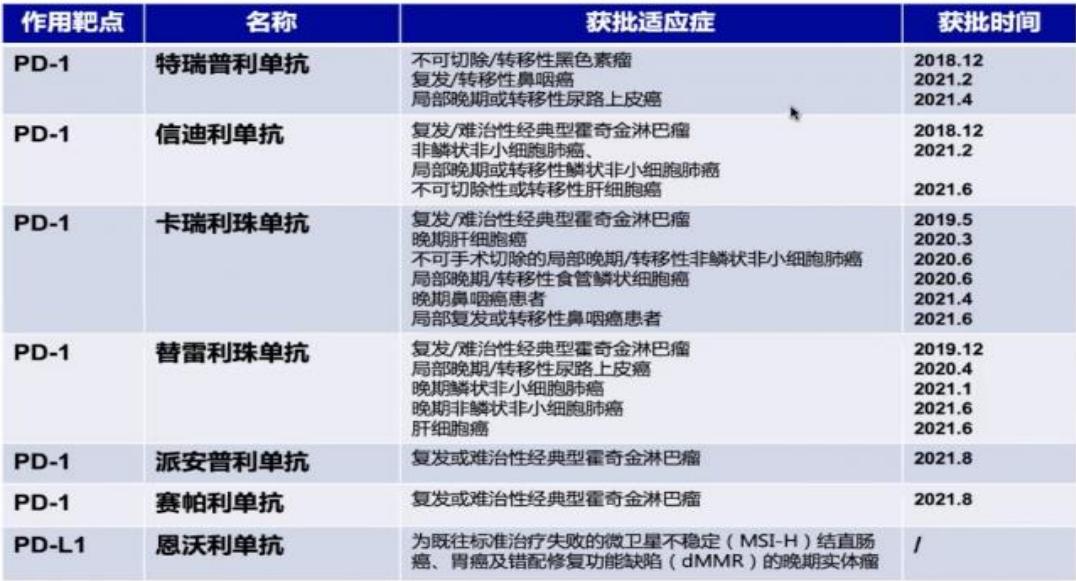
(引自讲者幻灯)
表3. 批准用于HCC治疗药物
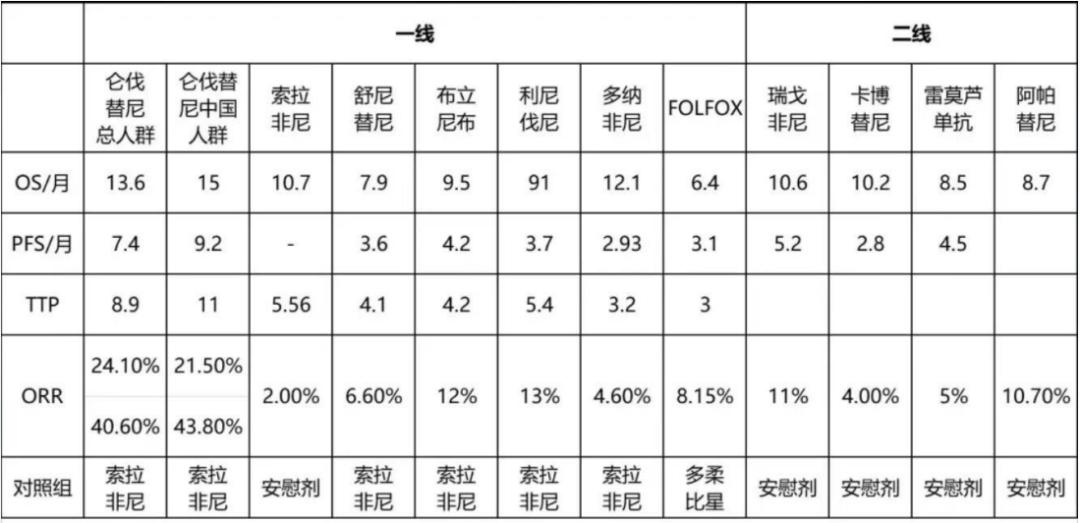
(讲者引自谢青教授报告幻灯)
CTLA-4*制剂抑**的抗癌机制
应用CTLA-4单抗时,自身反应性T淋巴细胞可不断增殖及活化,从而发挥抗肿瘤作用。CTLA-4*制剂抑**的抗癌机制一方面是阻断组成性表达CTLA-4的FoxP3+调节性T淋巴细胞活化,使辅助性T淋巴细胞(Th)或细胞毒性T淋巴细胞重新识别肿瘤新生抗原;另一方面是阻断表达于自身免疫性T淋巴细胞表面的CTLA-4,可以促进其活化,增强对肿瘤细胞的*伤杀**功效。
CTLA-4单抗的双重作用不仅增强了初期及效应阶段对表达肿瘤相关抗原肿瘤细胞的免疫应答反应,而且也增强了对于表达自身抗原的一系列正常细胞的免疫应答反应。
PD-1/PD-L1*制剂抑**的抗癌机制
PD-1广泛存在于细胞毒性T淋巴细胞和Th细胞上,肿瘤细胞表面的PD-L1和PD-L2配体会抑制细胞毒性T淋巴细胞,并上调调节性T淋巴细胞的活性从而使肿瘤细胞发生免疫逃逸。
PD-1/PD-L1途径不是调节幼稚T淋巴细胞启动,而是减少成熟T淋巴细胞的活化,进而抑制下游的TCR信号转导。淋巴细胞表面PD-1持续表达上调,通过促进一种“耗竭”状态导致广泛抗原暴露后T淋巴细胞免疫功能减弱,进而抑制组织破坏过程。PD-1与PD-L1的抗肿瘤机制在于重启淋巴细胞增殖以及细胞因子的产生,激活对肿瘤细胞的免疫再识别及*伤杀**。
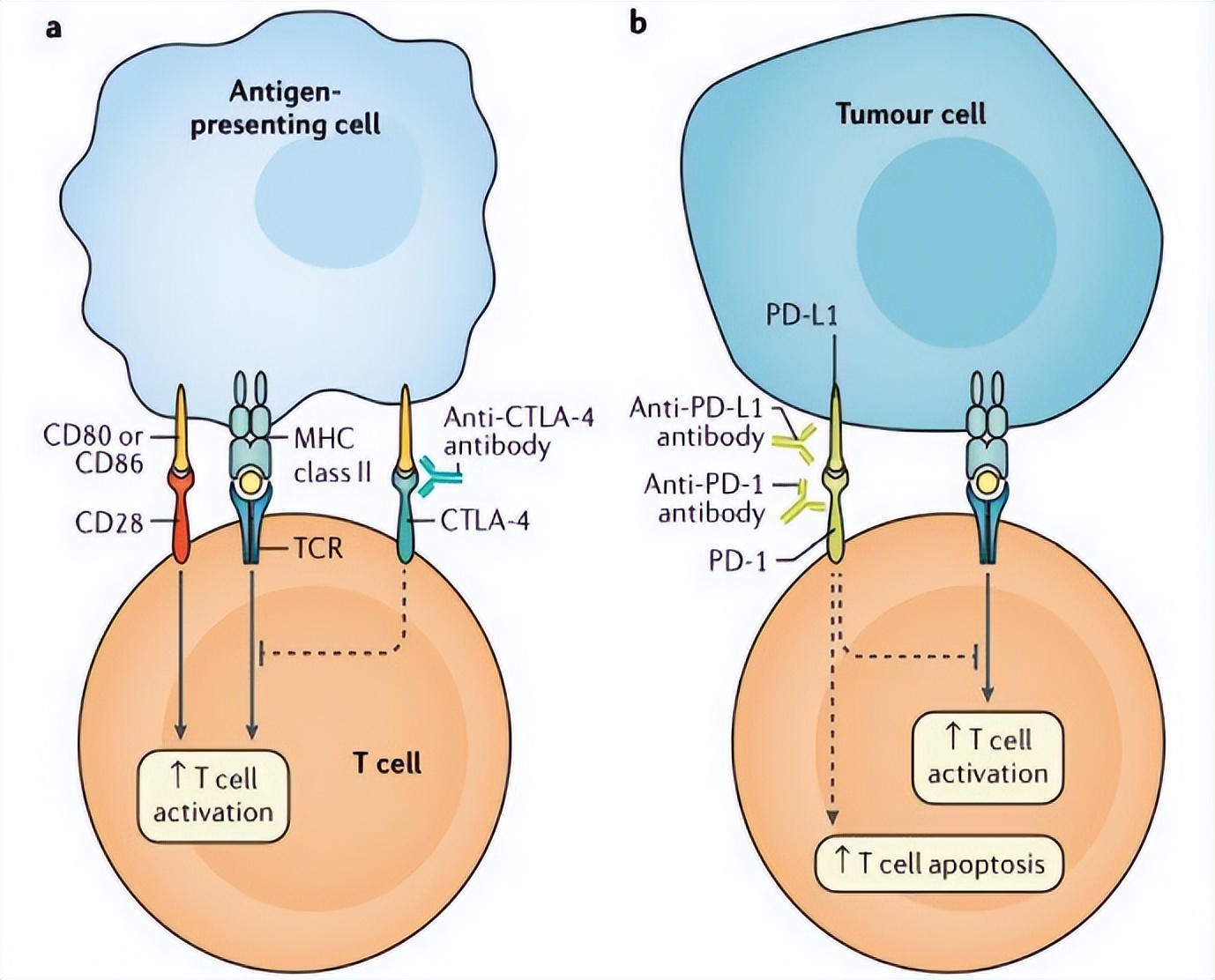
图2. CTLA-4、PD-1信号途径在T淋巴细胞活化中的作用[2]
免疫相关的不良反应
ICIs治疗虽为肝癌患者带来了希望,但也会破坏机体免疫耐受平衡,从而出现免疫相关的不良反应(irAE)[3],可以涉及全身多个脏器及内分泌系统,发生在肝脏的irAE 被称为免疫介导性肝损伤(ILICI),是药物性肝损伤的一种特殊类型。
irAEs是由于ICIs导致过度的免疫激活,对正常组织细胞产生破坏而带来相应的症状、体征、实验室检查异常结果。正常组织中免疫细胞活化,失去对自身抗原的免疫耐受,可出现类似自身免疫性疾病的症状。药物剂量、联合用药方案、自身免疫性疾病病史、肝转移瘤、年龄以及遗传易感性是ICIs相关肝损伤的危险因素。且研究显示[4],相比于单药治疗,联合治疗导致irAE风险更高,发病更早,临床应提高警惕。
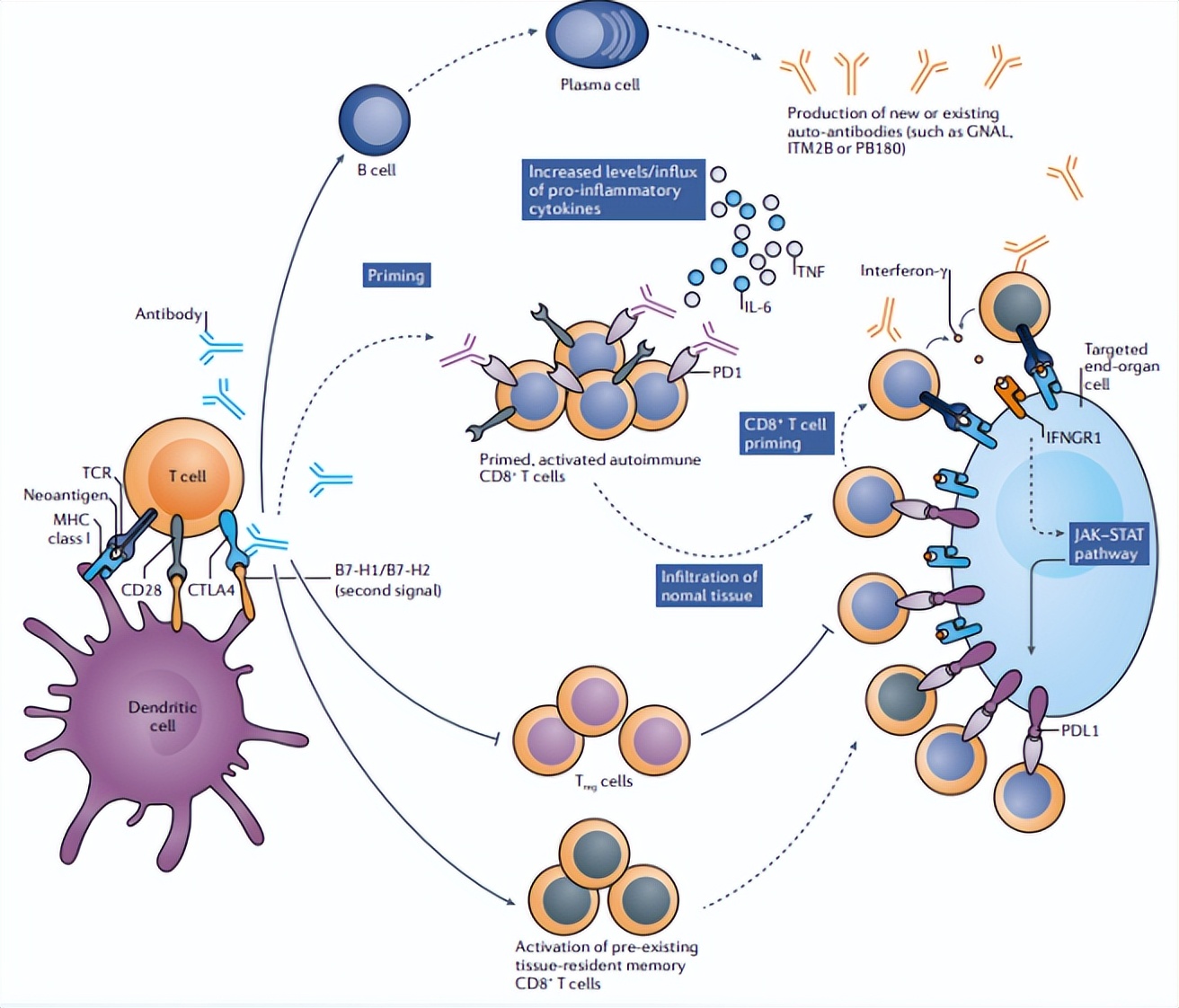
图3. 免疫相关的不良反应的不同发生机制[3]
ICIs肝损伤特点
ICIs可能会引起胆汁淤积*药性**物性肝损伤,通常发生在起始治疗后的4-12周,可能导致肝衰竭,且肝癌患者发生率略高于其他瘤种患者人群。此外,有研究表明,罹患自身免疫病的患者发生irAE风险增加。一项系统回顾纳入123例罹患自身免疫病并接受ICI治疗患者,结果显示50%患者自身免疫病加重,34%出现新的irAE,只有16%患者没有自身免疫病症状。但研究也发现,20例出现irAE的患者只有5例停止ICI治疗,罹患自身免疫病患者与没有自身免疫病患者的总生存期相同。
在大多数自身免疫病患者中,irAE可以通过糖皮质激素控制(只有16%的患者需要其他免疫抑制疗法)。文献系统回顾发现,仅有11%~17%的患者需要停止ICI治疗。
表4. 免疫检查点*制剂抑**肝损伤严重程度分级(CTCAE 5.0版)

(引自讲者幻灯)
ICIs对乙肝病毒再激活的影响
HBV再激活指HBsAg阳性/抗-HBc阳性,或HBsAg阴性/抗-HBc阳性患者接受免疫抑制治疗或化学治疗时,HBV DNA较基线升高≥2lg IU/ml,或基线HBV DNA阴性者转为阳性,或HBsAg由阴性转为阳性。HBV再激活伴有肝炎复燃,可能引起从无症状的自限性肝炎到致命的肝衰竭,延误肿瘤的正常治疗。
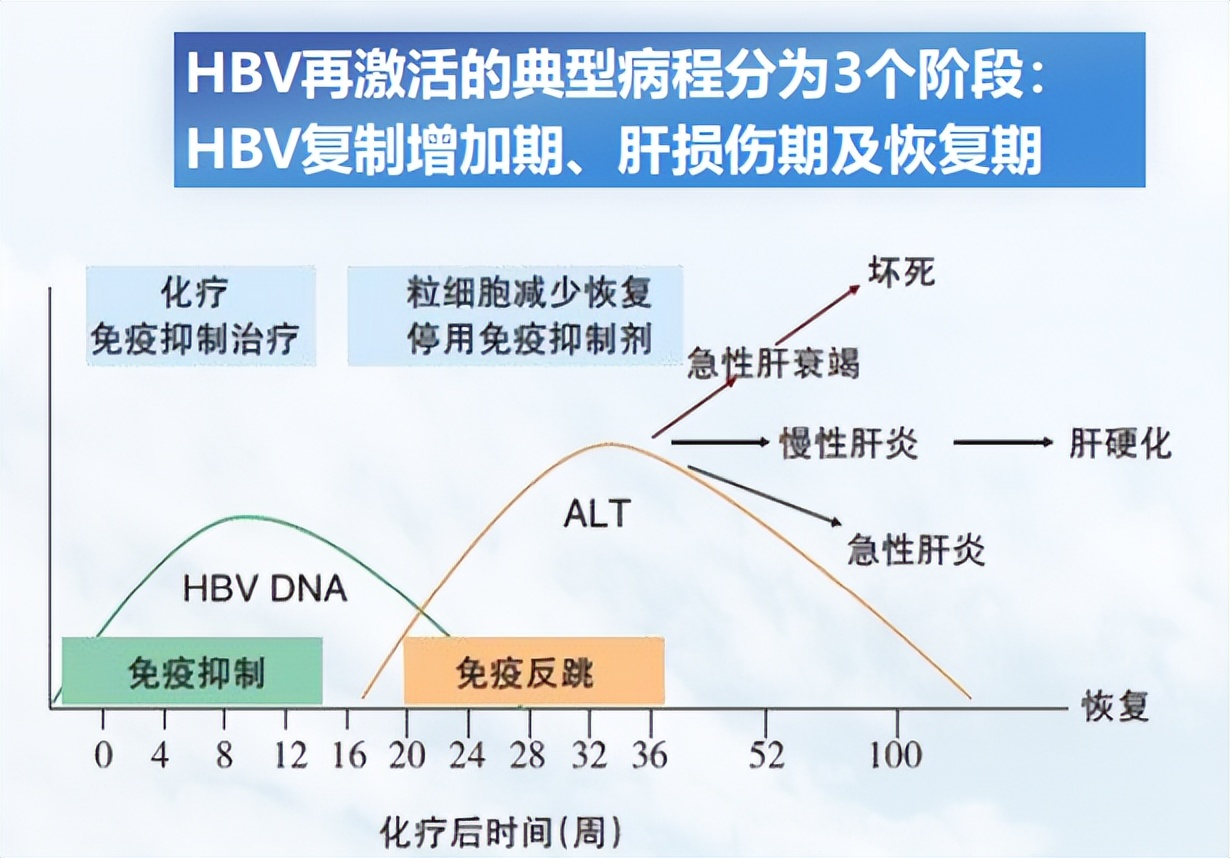
图4. HBV再激活的典型病程
ICIs肝损伤的治疗
近年来,为规范管理免疫治疗,降低药物毒性,国际国内ICIs相关毒性防治指南纷纷出台。有专家指出[5],HCC患者相关ICIs肝毒性管理的注意点,是肝癌患者肝炎的诊断可能会被潜在的肝脏疾病所混淆,应避免转氨酶升高后立即使用激素。
参考药物性肝损伤的治疗原则,ICIs肝毒性的治疗应根据肝损伤的严重程度给予患者个体化的治疗,及时停用可疑肝损伤药物;参考美国FDA停药标准,充分权衡停药引起原发病进展和继续用药导致肝损伤加重的风险。
表5. ICIs相关肝损伤的药物治疗

表6. ICIs相关肝损伤的药物治疗

(引自讲者幻灯)
大多数irAE在ICI停止后4~8周可缓解,严重病例在使用糖皮质激素后缓解。但注意,所有患者必须严密监测,以发现irAE复发或免疫抑制诱发并发症。尽管ICI似乎不会直接增加感染风险,但使用免疫抑制疗法和生物制剂治疗irAE可能会增加感染风险。
此外,irAEs恢复后考虑再次进行ICIs治疗是一种常见的临床问题,但再治疗的安全性和益处尚不清楚。ASCO和ESMO指南建议,所有4级irAE患者永久停用ICIs;ASCO指南建议对有3级心肌炎、肺炎、肾炎、肝炎和严重神经系统毒性患者永久停用ICIs;在其余情况下,肿瘤科医生需要明确一旦irAE缓解,患者是否能从重启ICI治疗中受益。需要根据患者的临床背景和具体临床需求,小心谨慎地作出重启ICIs的决定。
irAE与ICI疗效是否存在关联?
大型回顾性研究和荟萃分析均表明,转移性肺癌、膀胱癌和肾细胞癌患者接受 ICI单药治疗或与靶向药物或化疗联合治疗,出现任何级别irAE患者客观缓解率(ORR)和无进展生存期(PFS)均优于未出现irAE患者。但近期发表的一项对1500多例接受帕博利珠单抗治疗的转移性黑色素瘤患者的研究表明,irAE与PFS或OS没有关系。与转移性黑色素瘤结果相反,在另外一项帕博利珠单抗辅助治疗高危黑色素瘤的大型III期随机试验中,出现任何级别irAE患者无复发生存期(RFS)比没有irAE的患者要长。然而,在另一项纳武利尤单抗+伊匹木单抗辅助治疗的III期试验中,任何级别或3~4级irAE与患者RFS没有明显相关性。因此,irAE与ICI疗效是否相关,目前尚无统一答案。
irAE发生的潜在标志物有哪些?
根据既往临床经验,有一些可以预测irAE发生的潜在标志物,可供实践参考,但尚待大型临床研究证实。
- 治疗前:体内存在抗mAChR抗体阳性患者容易出现肌炎,抗甲状腺抗体阳性者出现甲状腺炎,抗BP180抗体阳性患者出现皮肤炎,抗核抗体患者阳性出现结肠炎,抗GNAL抗体或抗ITM2B抗体阳性患者出现垂体炎,抗CD74抗体阳性患者出现肺炎。
- 治疗后:在免疫检查点*制剂抑**开始治疗3周后检测B细胞变化(B细胞总数减少,CD21lowB细胞和浆细胞的百分比增加,CD21low B细胞克隆增加),也可能有助于识别 irAE风险增加患者。
- 血清细胞因子水平:可能预测irAE易感性,例如发生3级结肠炎患者平均IL-17血清水平高于出现0~2级结肠炎患者。
小 结
近年来,随着ICIs药物的不断发展以及药物可及性的不断提高,irAEs也逐渐被人们发现和关注。但临床实践中对ICIs所致的irAEs的管理有待进一步加强。肝癌靶向免疫治疗所致肝损伤把握治疗时机最关键,同时也需关注患者乙肝患者HBV再激活情况。只有对不良反应及时有效地控制管理,才能更加安全地进行肿瘤免疫治疗。
参考文献
1. 国家卫生健康委员会《原发性肝癌诊疗指南(2022年版)》.
2. NATURE REVIEWS DiSEASE PRiMERS. 2020(6):1-21.
3. Nature Reviews Drug Discovery. 21:495–508.
4. Martins F,et al.Nat Rev Clin Oncol.2019;16:563-580.
5. Sangro B et al. Journal of Hepatology, 2020, 72(2):320-341.