一、背景
自中国2017年加入国际人用药品注册技术协调会 (ICH)后,NMPA出台了一系列监管政策以促进中国的药监体系与国际标准一致。为了适应不断增长的药物需求并跟上中国制药领域的快速发展,鼓励创新和满足临床急需,2020年1月22日《药品注册管理法》(国家市场监督管理总局令第27号)发布,与旧的《药品注册管理办法》(国家食品药品监督管理局令第28号)相比,明确增加了“药品加快上市注册”一章,分为“突破性治疗药物程序”、“附条件批准程序”、“优先审评审批程序”、“特别审批程序”,并明确了四种程序的纳入范围、支持政策等要求,我国这四种“程序”的开辟,相当于对创新药研发开辟了“绿色通道”,为医药产业发展和公众用药安全有效提供极具价值的支持。
二、政策汇总表
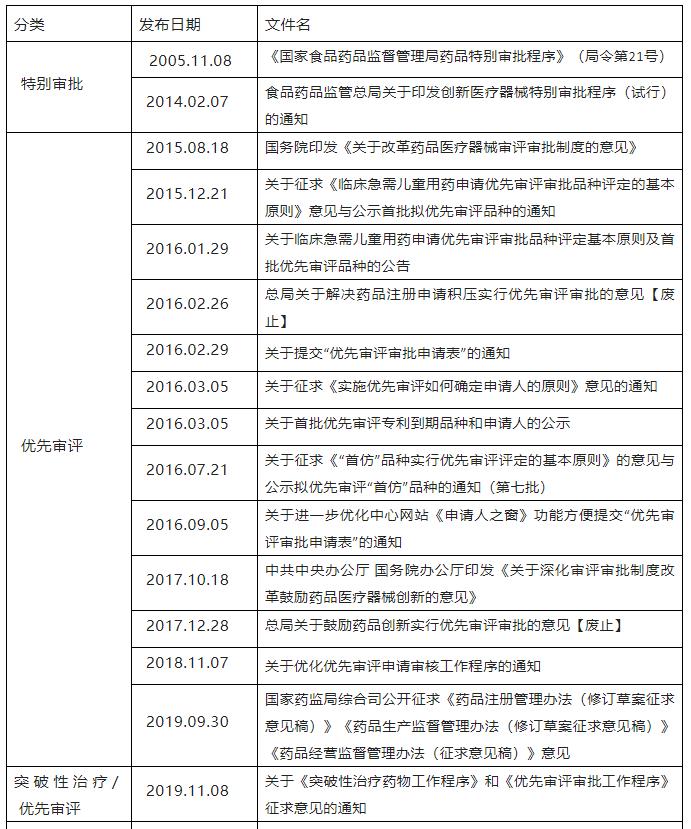

2、适用范围及申请阶段
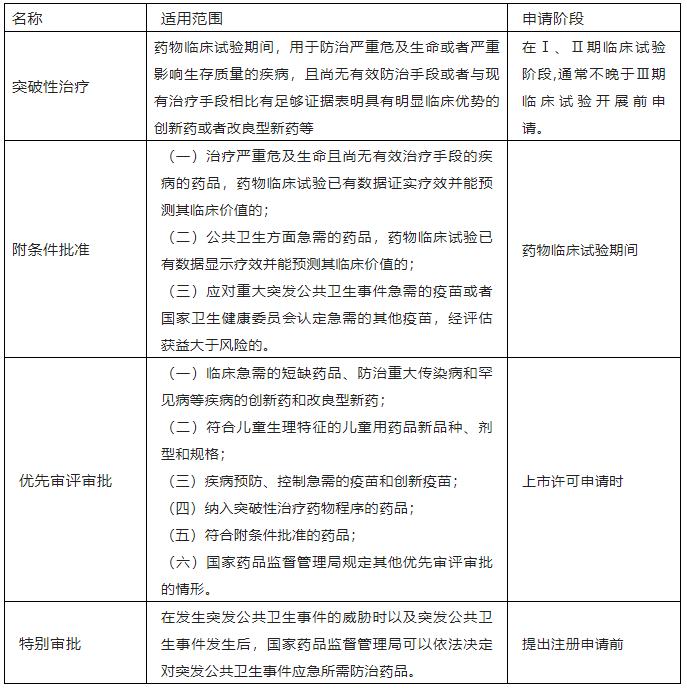
3、工作程序
3.1突破性治疗
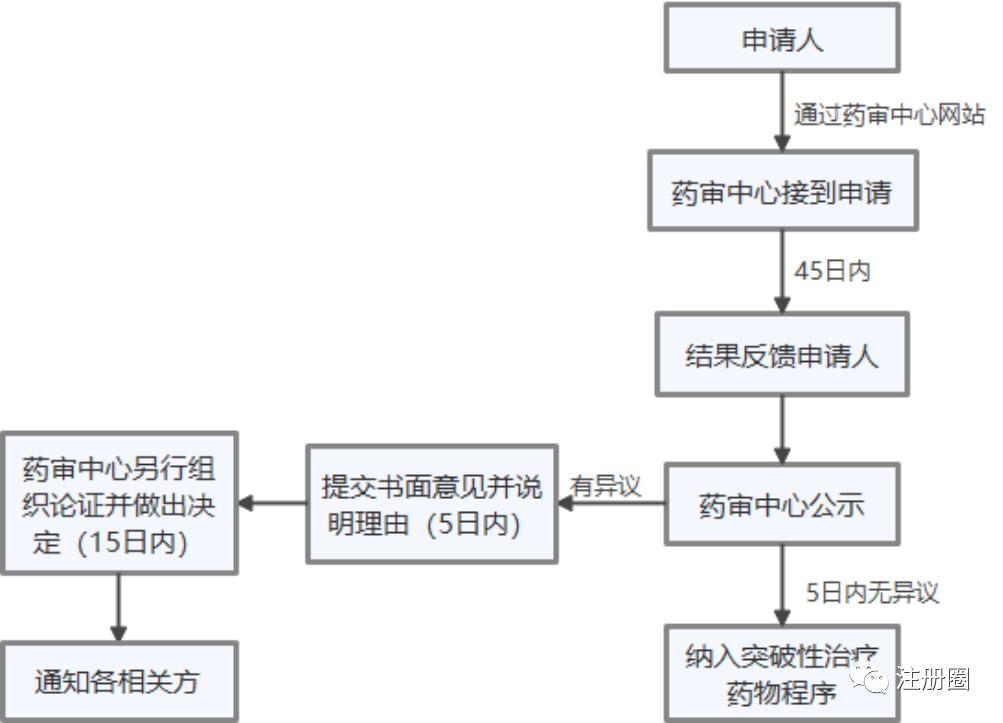
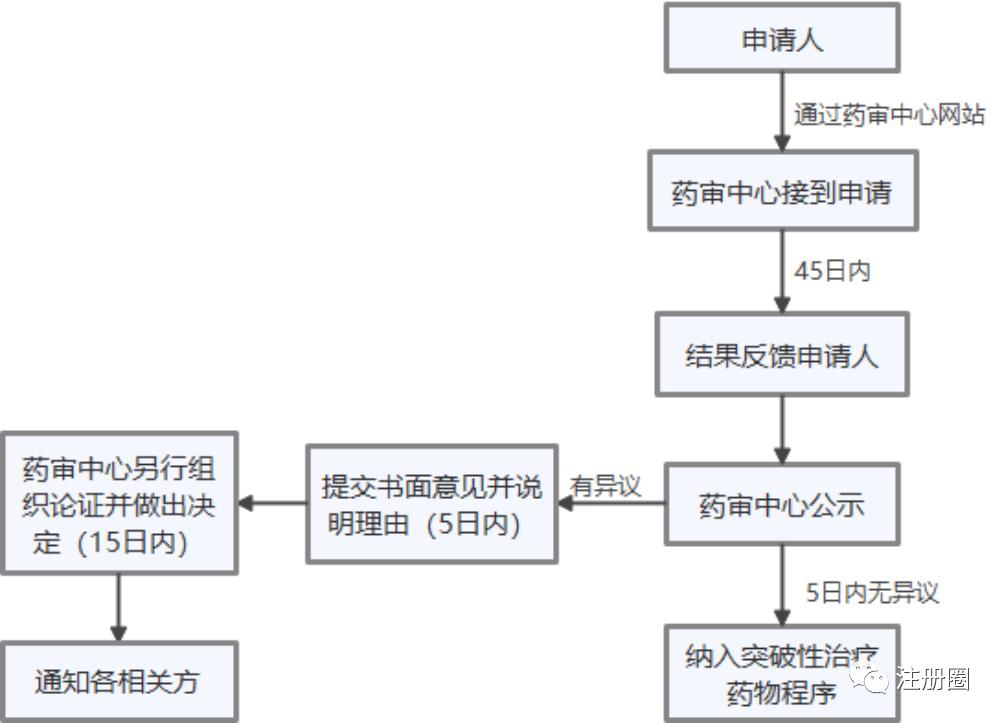
3.2优先审评
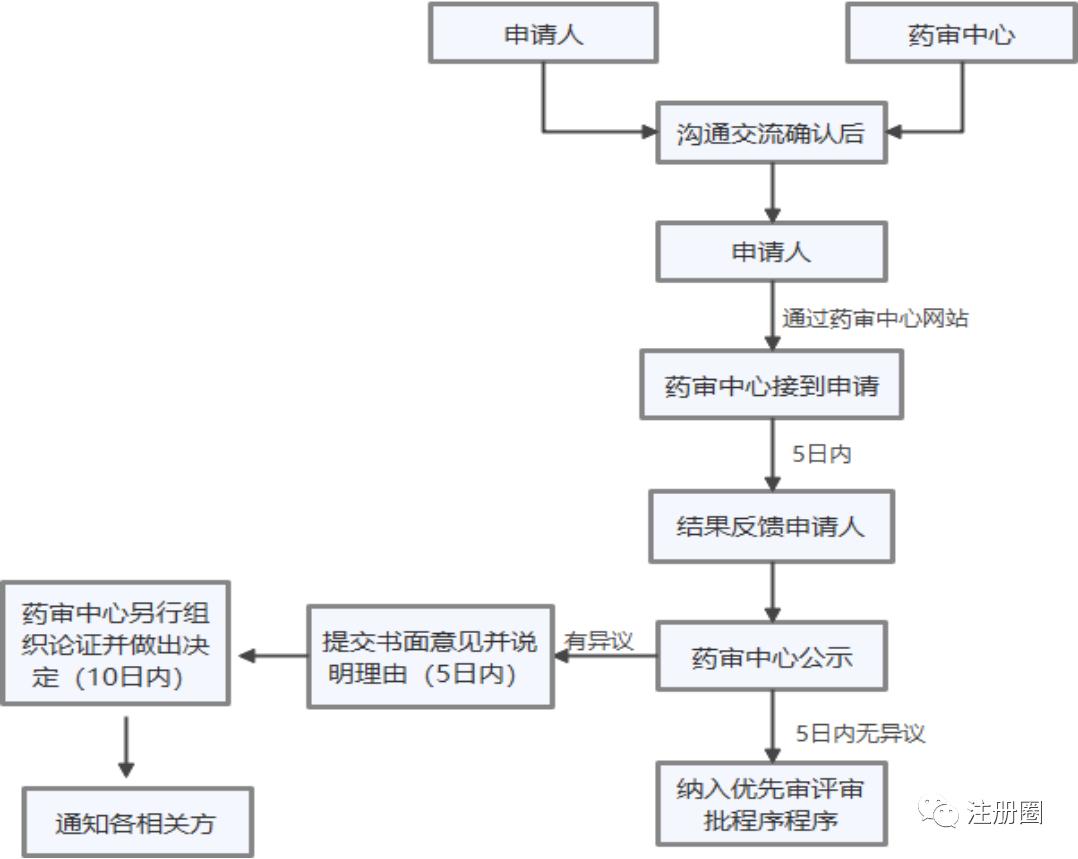
3.3附条件批准
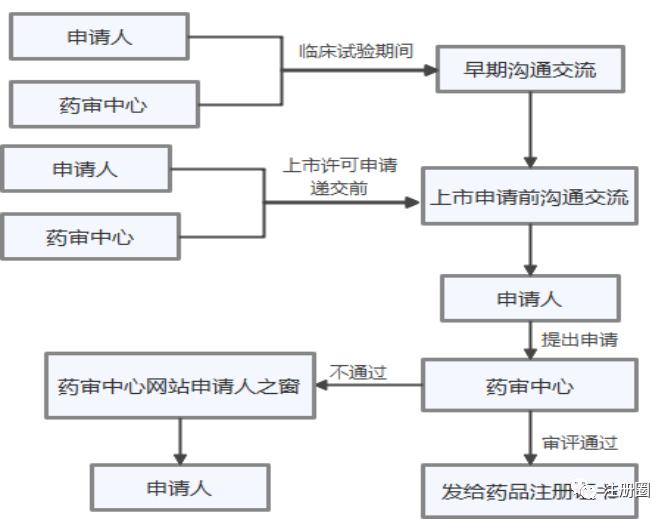
3.4特别审批
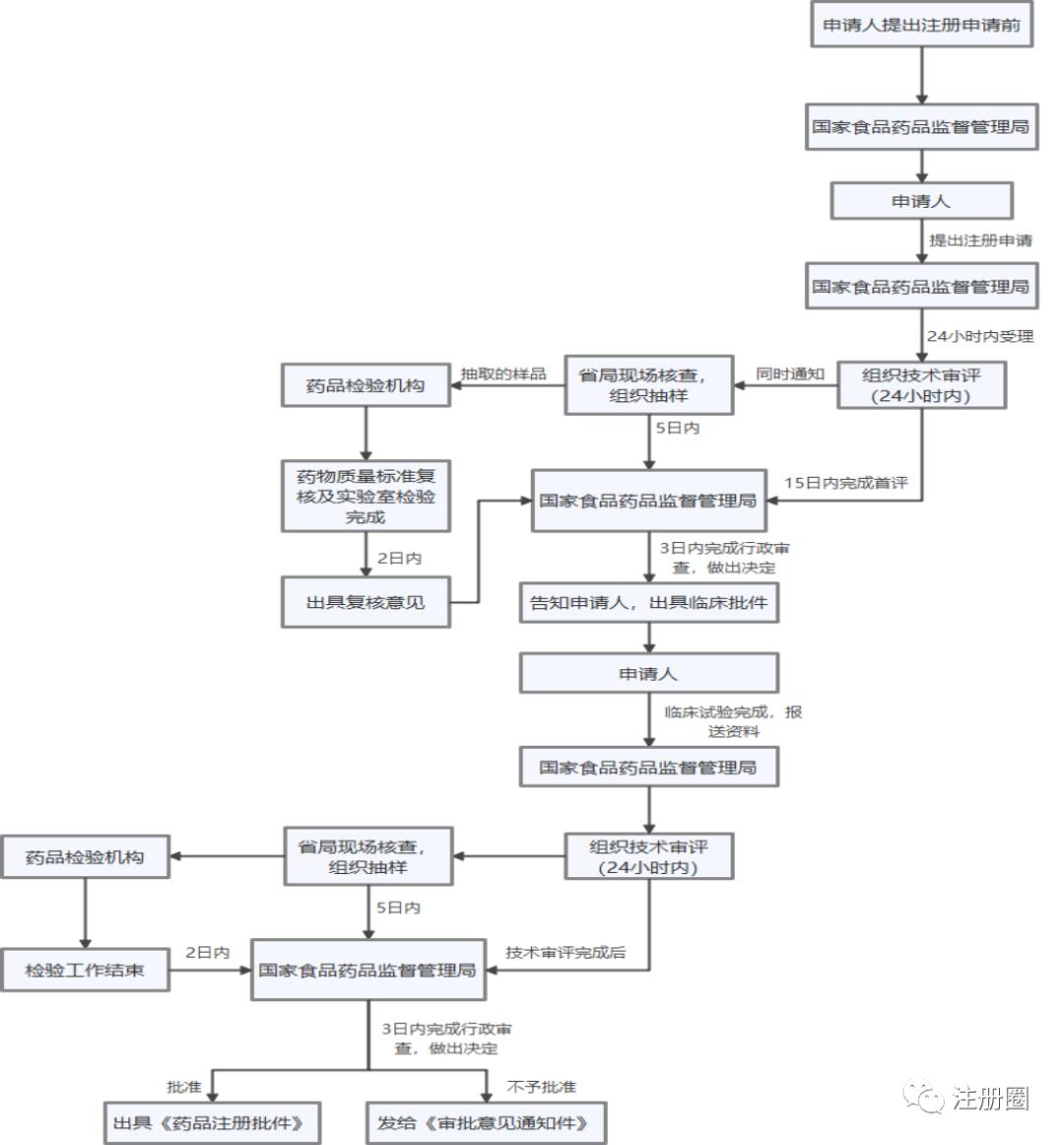
4、审评时限-优先审评审评程序

此文为原创文章,对以上观点,有任何不妥之处,欢迎大家积极斧正,评论留言交流。
更多其他资讯与服务请关注:注册圈。
注册圈,让注册人不再孤单!齐聚各层制药人,加入交流圈一起分享行业知识吧~