2022 ASCO GU | 董柏君教授:前列腺癌分子诊断突破传统,人工智能多方助力临床决策
温馨提示:以下内容仅限医疗卫生专业人士学术交流使用,如为非医疗卫生专业人士请主动退出浏览与阅读,否则由此产生的相关风险与后果应自行承担。
编者按: 随着前列腺癌领域诊断标志物、机器学习和神经网络技术的进步,分子诊断和人工智能在指导前列腺癌临床诊断、治疗和资源投入等方面产生了巨大影响,不仅在影像学方面推动了前列腺癌治疗决策优化,也对前列腺癌预后预测进行了更精准评估。本次2022 ASCO GU会议就前列腺癌新型分子影像学诊断、双示踪剂PET/CT前列腺穿刺活检以及人工智能预后评估等热点进行了前沿报道。本期《肿瘤瞭望》特邀 上海交通大学医学院附属仁济医院泌尿科董柏君教授 对以上内容进行精彩点评。

视频加载中...
1. Abstract 9:在疑似前列腺癌复发患者中 1 8F-rhPSMA-7.3PET的检出率:一项Ⅲ期、前瞻性、多中心研究(SPOTLIGHT)结果 [1]
背景:
18F标记的前列腺特异性膜抗原(PSMA)正电子发射断层扫描(PET)相比68Ga-PSMA有更长的半衰期和更高的空间分辨率。本研究报告了一种具有低膀胱活性和高治疗性PET配体亲和力的18F-rhPSMA-7.3的检出率。
方法:
SPOTLIGHT(NCT04186845)研究采用双主要终点,即18F-rhPSMA-7.3患者水平的正确检测率(CDR:≥1个真阳性病灶的患者比例)和区域水平的阳性预测值(PPV:所有PET阳性区域),采用组织病理学和/或传统影像学作为复合真实标准(SoT)。在仅有组织病理学SoT的患者亚组中也评估了以上指标。预设的统计学阈值为CDR≥36.5%,PPV≥62.5%。总检出率根据PSA分层。接受根治性治疗后PSA升高疑似生化复发的前列腺癌复发患者静脉注射296 MBq 18F-rhPSMA-7.3后50-70分钟进行PET检查。PET检查后60天内进行影像学引导下的PET阳性病灶活检,如需确认性影像学检查应在90天内进行。3位盲态中心阅片者评估的影像学结果作为最终结果。每位患者均建立了SoT。
结果:
389例接受18F-rhPSMA-7.3扫描的患者(中位[范围]PSA:1.10[0.03-134.6] ng/mL)的总体检出率为83%,详见图1。在有复合SoT的366例患者(中位[范围] PSA,1.27 [0.03-134.6] ng/mL)中,患者水平的CDR为56.8%(95% CI,51.6-62.0),达到预设阈值;区域水平的PPV为59.7%(54.7-64.7),未达预设阈值。在仅有组织病理学SoT的亚组中,患者水平的CDR和区域水平的PPV更高,分别为81.2%(69.9-89.6)和71.6%(62.5-80.7),均达到预设阈值。
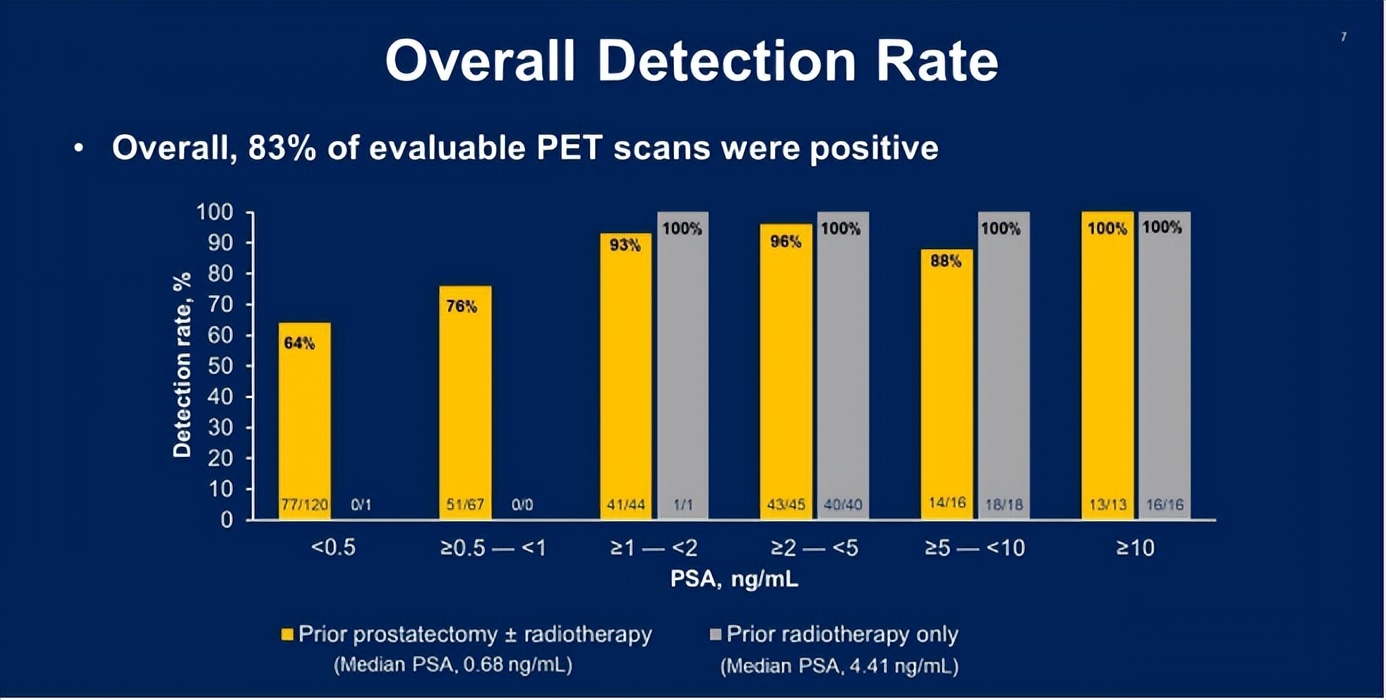
图1. 不同PSA区间范围的18F-rhPSMA-7.3-PET检出率
结论:
18F-rhPSMA-7.3可获得有临床意义的CDR,达到预设阈值。区域水平的PPV未达预设阈值,因为具有复合SoT的患者的数据受到较高(92%)比例的前列腺/床扫描(依赖常规影像学,并非最优SoT)的限制。而每例患者有至少一个区域组织病理学SoT的亚组PPV较高,95% CI下限已大于预设阈值。这些数据支持18F-rhPSMA-7.3PET在有较宽PSA范围的复发性前列腺癌患者中的临床应用。
董柏君教授特邀点评:
本篇研究报道了18F-rhPSMA-7.3标记PET在前列腺癌诊断中的应用,支持新型分子影像可用于鉴别前列腺癌根治术后是否出现生化复发。在前列腺癌患者根治术后生化复发的判断中,需区分临床复发和单纯PSA进展,而在临床复发层面,还需进一步判断局部复发和远处转移,以指导患者后续治疗。对生化复发患者病灶部位和肿瘤负荷的判断,有利于采取更有针对性治疗措施。新型分子影像具有良好的前列腺癌病灶检出率,同时与最终病理结果具有高度一致性。因此本研究的一大亮点在于, 对临床实际中部分难以用病理证实的前列腺癌病灶,可以基于18F-rhPSMA-7.3标记PET结果来制定精准治疗方案。
随着多学科协作诊治理念的普及以及国内对临床研究的逐渐重视,以分子影像学诊疗为代表的前列腺癌核医学科进展成为前列腺癌多科合作的重要组成部分,核医学科在前列腺癌中的应用特色体现在: ①精准诊断。 不仅提示肿瘤位置,更能体现肿瘤活性。 ②核素治疗。 177Lu-PSMA于今年获得FDA批准,成为晚期前列腺癌的最新疗法;国内也正在同步进行177Lu-PSMA相应的临床研究,中国前列腺癌患者目前可通过参加临床研究从该疗法中获益。此外,Ra-223作为前列腺癌的经典核素治疗,在国内临床已开始常规应用。
未来的前列腺癌分子影像学诊断,首先需不断探索前列腺癌特异性分子标志物,以进一步 提高诊断效能 ;其次希望出现国人自主研发的分子标志物,使诊断和治疗技术在 经济性和可及性方面更符合中国国情 ;最后 核素治疗将进一步作为放疗、手术等转移性前列腺癌传统治疗的有效补充 ,让患者临床获益。
2. Abstract 34:双示踪剂PET/CT引导的活检、mpMRI引导的活检、系统活检以及联合活检用于前列腺癌的诊断[2]
背景:
越来越多证据表明多参数MRI(mpMRI)和PSMA PET/CT引导的靶向活检用于前列腺癌诊断的有效性,但尚无mpMRI与PSMA PET/CT靶向活检的直接比较。由于胃泌素释放肽受体(GRPR)在前列腺癌中高表达,可弥补PSMA在前列腺癌中的不稳定表达,因此,本研究旨在比较mpMRI、双示踪剂(GRPR和PSMA)PET/CT靶向活检、系统活检以及联合活检在前列腺癌诊断中的有效性。
方法:
此项前瞻性、有效性比较研究于2020年9月至2021年6月纳入了112例疑似前列腺癌患者。双示踪剂PET/CT或mpMRI阳性的患者接受靶向活检,靶向活检后所有患者接受系统活检。主要终点为不同活检方式的前列腺癌检出率。次要终点为3种成像方法的诊断效能、漏诊率以及不同活检方式样本相对前列腺切除术中样本的病理升级和降级情况。
结果:
在112例患者中,34.82%(39/112)为有临床意义的前列腺癌(csPCa, ISUP分级组≥2),4.46%(5/112)为无临床意义的前列腺癌(ISUP分级组=1)。68Ga-PSMA PET/CT靶向活检的前列腺癌检出率(69.77%)和活检阳性针比例(0.44)与系统活检(39.29%和0.12)和mpMRI靶向活检(36.14%和0.23)相比均更高(P < 0.005),详见图2。双示踪剂PET/CT可避免52.67%(59/112)的不必要活检,而双示踪剂 PET/CT靶向活检联合系统活检可获得高达77.36%的检出率,且无csPCa误诊。
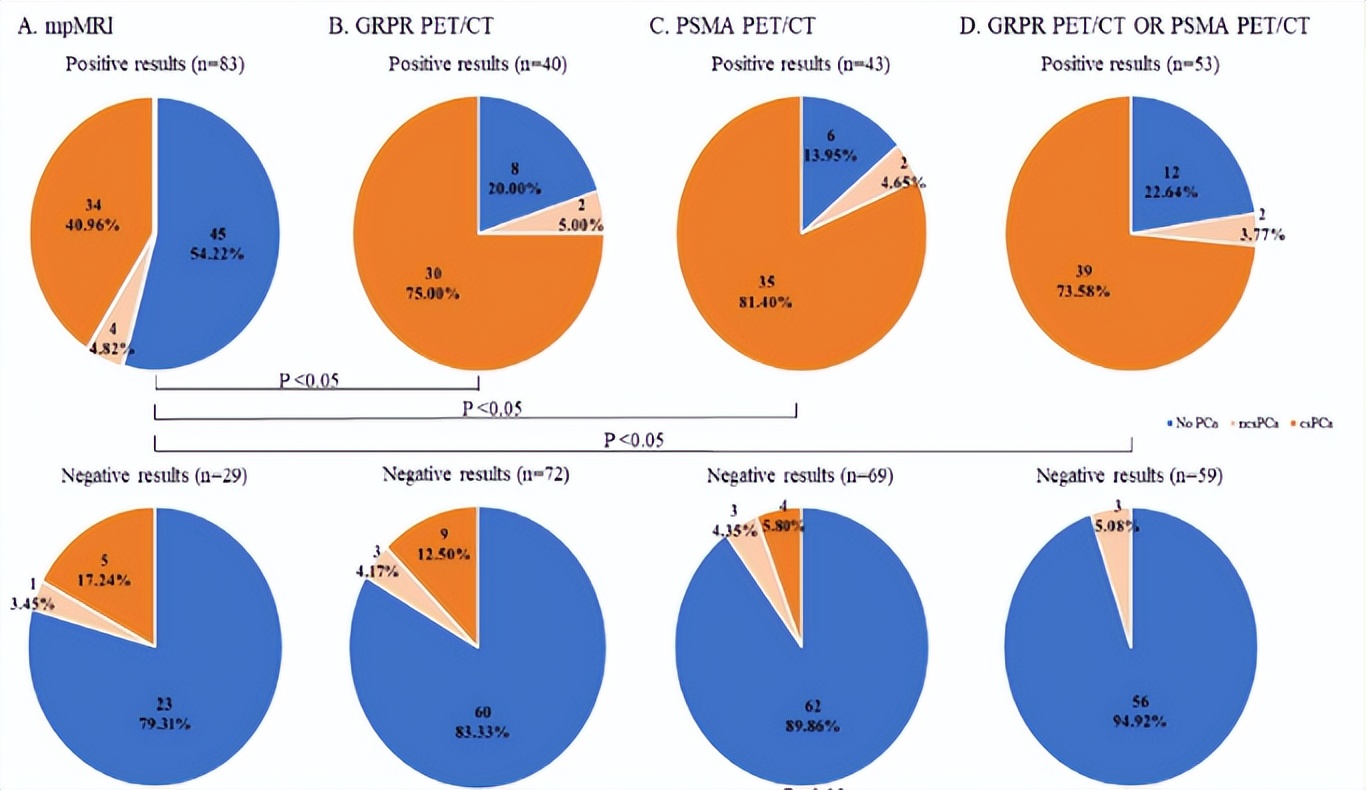
图2. 不同影像学引导下的前列腺癌诊断效能
结论:
双示踪剂PET/CT可用于筛查以避免不必要的活检。与mpMRI靶向活检相比,双示踪剂PET/CT靶向活检联合系统活检对于cSPCa的诊断或许更有效且更有前景。
董柏君教授特邀点评:
常规前列腺穿刺基于PSA、直肠指诊以及mpMRI三项指标进行判断,经典方式为经直肠B超引导下前列腺穿刺活检途径。当mpMRI有影像学提示意义时,可通过mpMRI与超声融合进行靶向联合系统穿刺活检。
本篇ASCO GU摘要来自于我国的湘雅医院泌外团队,在常规前列腺穿刺模式的基础上,联合双示踪剂(GRPR和PSMA)PET/CT靶向活检,研究结果提示双示踪剂PET/CT不仅可发现更多有临床意义的前列腺癌,更可以减少不必要的前列腺穿刺活检。
mpMRI虽然是目前前列腺癌诊断最佳的无创影像学检查,但在早期前列腺癌诊断以及不典型病灶的影像学评估等方面,PSMA PET与mpMRI能够进行相互补充:
- 对于mpMRI评估后病灶 PI-RADS评分4分或5分 的患者, 通过mpMRI-超声融合靶向联合系统活检后的穿刺阳性率可达70%~80% ,因此具备该特征的患者应用新型分子影像评估的临床价值不高;
- 处于 PSA灰区或PI-RADS评分3分 的患者,传统穿刺方式的阳性率仅20%,因此结合 新型分子影像诊断,能更清晰提示病灶部位和范围,有助于提高穿刺阳性率 ,以PSMA标记为主的影像学评估在该人群中具有临床应用价值。
- 随着冷冻消融、HIFU等前列腺癌局灶治疗的应用推广, 新型分子影像诊断在肿瘤病灶大小、位置的精准定位方面将有助于提高局灶治疗的有效性和安全性。
- 对于穿刺前怀疑有淋巴结转移的患者, 分子影像有助于提供更为准确的临床分期。
分子影像不仅是前列腺癌诊断的重要工具,在穿刺、治疗等前列腺癌全面评估中都将发挥极大价值。
3. Abstract 222:在局限性前列腺癌NRG肿瘤Ⅲ期临床试验中,采用数字化组织病理学多模式深度学习开发并验证预后AI生物标志物 [3]
背景:
局限性前列腺癌的预后预测依赖于非特异性模型,可导致患者治疗过度或治疗不足。各种基于组织的分子生物标志物试图填补这项未满足的需求,但大多缺乏前瞻性随机试验的验证。本研究通过数字化组织病理学的多模式深度学习,利用5项Ⅲ期随机试验的数据训练并验证了局限性前列腺癌的预后生物标志物。
方法:
由5项NRG肿瘤Ⅲ期前列腺癌放疗随机对照试验(RTOG 9202、9408、9413、9910 和 0126)中的治疗前活检切片采集组织病理学图像数据,随机分为训练队列(80%)和验证队列(20%)。开发了一种多模式人工智能(MMAI)架构,输入临床病理学和基于图像的(组织病理学)数据,以预测二元结果。采用该架构训练多种模型以预测相关临床终点:生化复发(BCR)、远处转移(DM)、前列腺癌特异性生存(PCaSS)和总生存(OS)。采用基于时间的曲线下面积(AUC)验证这些模型的预后鉴别能力,详见图3。

图3. MMAI预后模型的开发
结果:
7957患者中的5654例(71.1%)有可用的临床病理学和组织病理学图像数据,从16204个治疗前活检样本的组织病理学切片中生成了16.1TB的数据。经过训练模型、锁定模型并在验证队列中评估,发现MMAI预后模型在以下方面均优于NCCN模型(PSA、T分期和Gleason评分):5年DM(AUC:0.84 vs.0.73)、5年BCR(AUC:0.69 vs.0.58)、10年PCaSS(AUC:0.79 vs.0.66)和10年OS(AUC: 0.65 vs. 0.58)。在验证队列的每个单独临床研究的所有临床终点中,MMAI模型均优于NCCN风险分组。
结论:
这是首个利用多项大型Ⅲ期临床试验数据开发并验证的局限性前列腺癌预后生物标志物。成功验证了MMAI预后生物标志物在识别BCR、DM、PCaSS和OS方面均优于标准的临床和病理学参数。这项可大规模扩展应用的技术有助于前列腺癌患者的个体化管理。
董柏君教授特邀点评:
本篇研究报道结果证实,相较于传统基于PSA和Gleason评分的临床危险分层模型,人工智能和深度学习通过多种信息整合,为临床提供了更为精准的预后判断模型。传统危险分层模型,无法对肿瘤的侵袭特性、转移特性、耐药特性进行预后判断,而 人工智能将肿瘤细胞形态、肿瘤细胞占比和肿瘤细胞负荷等信息进行重组,从肿瘤全貌及微环境特征进行整体判读,将可能改变未来前列腺癌临床诊疗策略或提供重要参考。
人工智能在未来的临床转化过程中,需围绕具体临床路径和临床场景进行更有针对性的临床研究。期望人工智能通过对大数据的深度学习,帮助医生做出最佳临床决策,以体现其真正临床价值。
总结
前列腺癌领域新型分子诊疗和人工智能应用在未来具有极大潜力,其突破性进展将极大可能改变前列腺癌诊断、治疗和预后判断的当前治疗格局,也期待更多前沿进展通过严谨的临床研究科学论证,为更多前列腺癌患者带来临床获益。
参考文献:
[1]2022 ASCO GU-Abstract 9: Detection Rate of 18F-rhPSMA-7.3 PET in Patients with Suspected Prostate Cancer Recurrence: Results from a Phase 3, Prospective, Multicenter Study (SPOTLIGHT).
[2]2022 ASCO GU-Abstract 34: Dual-tracer PET/CT-targeted, mpMRI-targeted, systematic biopsy, and combined biopsy for the diagnosis of prostate cancer.
[3]2022 ASCO GU-Abstract 222: Development and validation of a prognostic AI biomarker using multi-modal deep learning with digital histopathology in localized prostate cancer on NRG Oncology phase III clinical trials.
声明
本视频/资讯/文章是由益普生医学团队编辑/医疗卫生专业人士撰写提供,旨在用于医疗卫生专业人士间的学术交流,不支持以任何形式转发给非医疗卫生专业人士;如有违反,责任自负;转发给其他医疗卫生专业人士时,也请自觉保护知识产权。
本视频/资讯/文章的内容不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。内容中出现任何药品并非为广告推广目的,医疗卫生专业人士如进行处方,请严格遵照该药品在中国批准使用的说明书。益普生不承担任何相关责任。
DIP-CN-008203 有效期至2023年3月31日