作为众病之王的癌症,如同对人类的原罪,带给了人们太多的伤痛。但人类攻克肿瘤的信念一直在坚持。基于医学的进步和发展,世界卫生组织(WHO)2006年起把癌症明确定义为一种慢性病。所谓慢性病,就是病理变化缓慢、病程长、短期内不能治愈或终身不能治愈的疾病,换句话说,人们现在可以在某种程度上像对待高血压、糖尿病一般来对待癌症。
这也意味着更多的癌症病人面临的是一场旷日持久、此消彼长的拉锯战,而且极有可能将多学科的多种治疗手段统统用上,通常是一个治疗方案失败了,再换另外一个方案。
那么,如何判断某个方案对肿瘤治疗是否有效呢?
传统内科实体瘤疗效评价标准
医学上对实体瘤疗效的评价标准也随着医学的进步和发展而优化。1970年代先是提出WHO标准,并于1981年正式发表,这是“第一代”疗效评价标准;2000年,RECIST评价标准发表,是在WHO标准基础上进行了改良;到了2009年RECIST评价标准修订版本发布即RECIST1.1,是在RECIST评价标准基础上修订更新而成是目前应用最为广泛的疗效评价标准。随着免疫治疗的兴起,实体瘤疗效评价标准又有了新的变化,后文再详述。
RECIST1.1缓解标准评估指标:
完全缓解(CR,complete response)所有靶病灶消失,全部病理淋巴结(包括靶结节和非靶结节)短直径必须减少至<10mm。
部分缓解(PR,partial response)靶病灶最大径之和比基线水平减少至少30%。
疾病进展(PD,progressive disease)靶病灶最大径之和至少增加≥20%或出现新病灶。
疾病稳定(SD,stable disease)靶病灶最大径之和缩小未达PR,或增大未达PD,介于两者之间。
注:如仅一个靶病灶的最长径增大≥20%,而记录到的所有靶病灶的最长径之和增大未达20%,则不应评价为PD。
临床评估肿瘤疗效常用方法
临床检查
医生通过查体,来了解肿瘤的缩小情况。适用于体表的肿瘤,或者身体内部的肿瘤,但是医生可以用手触到。例如乳腺癌,某些癌症导致的体表淋巴结转移,直肠癌等等。医生通过体格检查,使用直尺等测量工具,可以大致了解肿瘤的退缩情况,有一定的参考价值,但是比较主观。
影像学检查
根据B超,CT,MRI等检查的结果,可以了解肿瘤的大小有没有变化,有没有新发的肿瘤。根据病灶的大小变化,对应RECIST标准,看病情缓解情况。
注:RECIST标准用于实体肿瘤,也就是说病灶是可以测量的。目前,还有人推荐使用PET/CT来评价治疗效果,了解病灶在治疗前后的摄取情况,适用于淋巴瘤,白血病等血液系统肿瘤。
肿瘤标志物
肿瘤标志物是一种比较简单和方便的检查手段,只需要抽血化验即可,有一定的参考价值。以大肠癌为例,了解治疗前后CEA的变化情况,如果CEA下降的越多,说明治疗效果越好。但是,有很大一部分患者,治疗前后,肿瘤标志物的水平始终位于正常范围内,这样就不能利用肿瘤标志物来评价疗效了。
循环肿瘤细胞
循环肿瘤细胞是指人体内的肿瘤细胞,从原发肿瘤中脱落,进入到外周血液当中。检测外周血中循环肿瘤细胞的变化情况,是近年来兴起的一种检测手段。目前,大部分还处于临床研究阶段,没有大范围在临床范围使用,因为价格比较昂贵,技术还不够成熟。目前为止,在乳腺癌和结直肠癌中应用最广泛。
病理诊断
病理诊断是最可靠的,术前做了一段时间的新辅助治疗后,最后将癌变组织切除,然后送去病理科,病理科医生在显微镜下观察肿瘤的退缩情况,有多少肿瘤细胞死掉了。
病理评价新辅助治疗效果是最准确的,最靠谱的,有一个肿瘤消退分级(TRG)标准,专门用来评价肿瘤细胞消退情况。如果肿瘤细胞没有退缩,术后可能就需要更换新的化疗方案了。
传统肿瘤疗效评价标准不能准确评估免疫治疗
免疫疗法的兴起带给很多晚期肿瘤患者希望,但在免疫治疗过程中,疗效评估跟其他治疗不同。肿瘤有可能先变大,然后再变小。这个时候很难判断它是真的不管用了,还是过一段时间以后会缩小。对于先大后小的这种患者,时间上是有效的一种,但是如果肿瘤持续增大,就是没效的一种反应。肿瘤先增大,然后缩小,称之为假性进展,这是因为免疫系统激活后,免疫细胞会聚集在肿瘤周围,看上去就像肿了一样。发生这种情况的时候,在影像上可能表现出肿瘤的体积增大,但如果这个时候给他做穿刺,就会发现肿块里面不是肿瘤细胞在增多,而是炎性细胞在增多。随着后续治疗,炎性细胞把肿瘤细胞杀掉以后,它会逐渐缩小的。
正确区分真性假性进展,才能确认免疫治疗的有效性。
传统的影像学疗效评价标准为众所周知的RECIST 1.1,由于其可能低估免疫治疗的获益,显示出了不足。2009年,一种二维的疗效评价标准——irRC首先问世。2013年,专家组对该标准进行简化,形成了irRECIST标准。后来,为了统一临床研究中评估免疫治疗疗效的评价标准,2017年3月1日,the Lancet Oncology上,RECIST工作组正式提出iRECIST标准(immune response evaluation criteria in solid tumors,iRECIST)。
为了探究三个疗效评价标准在接受PD-1/PD-L1*制剂抑**的NSCLC患者中接受疗效评价的差别,来自法国的研究团队开展了一项回顾性分析。应用RECIST 1.1,irRECIST,iRECIST分别对患者的短期疗效结果进行评价,对比三者的差别。
从2013年2月至2016年12月,共有160名患者纳入该回顾性分析。
最终,共有20例患者(13%)确认为不典型应答(Atypical Responses),其中8例患者(5%)假性进展(Pseudoprogressions, PsPDs),12例(8%)患者呈现分离性应答(Dissociated Responses)。这些患者的OS明显优于确定进展的患者。
有13例(11%)患者根据RECIST1.1评价标准评估为PD,但是最终确认临床获益。
根据RECIST 1.1进行评价,37例(23%)为应答或SD,123例(77%)为PD。但是根据irRECIST或iRECIST疗效评价标准,80例可评价,有15例患者难以进行评估。
结论
irRECIST/iRECIST评价标准与RECIST评价标准的主要区别是在于对新发病灶、疾病进展的评价。
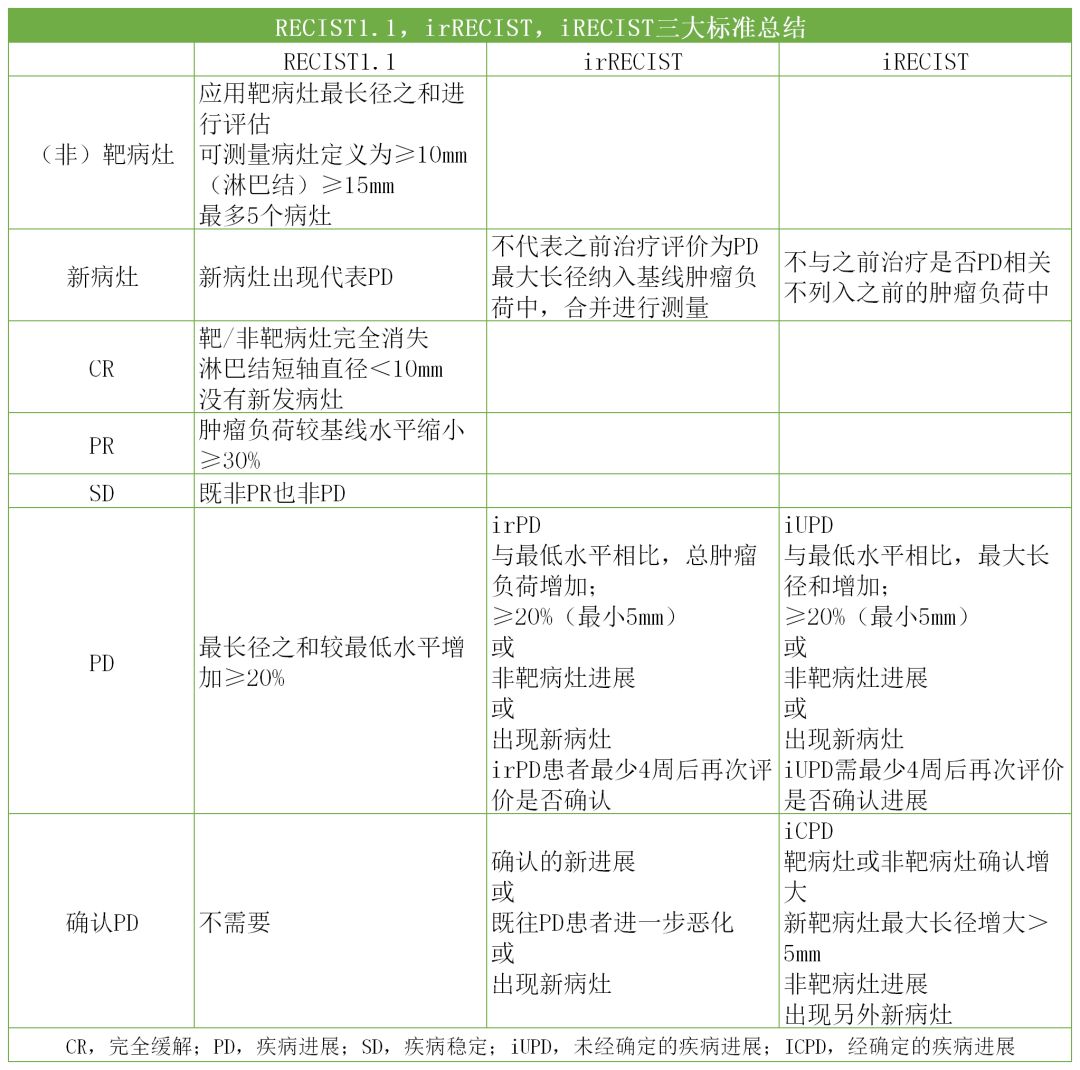
NSCLC患者接受免疫治疗时,可能会发生13%左右的不典型应答,其中包括假性进展(肿瘤先增大后缩小)和分离性应答(一些肿瘤成分增大,一些却缩小),这些患者的OS明显优于真正确认PD的患者。
约11%接受免疫治疗超过6个月患者可能被RECIST标准评价为PD,其实能够临床获益。
免疫治疗临床评估
“假性进展”的表现:
虽然目前没有明确的“假性进展”的判断标准,根据临床经验判断如下表现:
1)首先,患者的症状好转,包括疼痛减轻、食欲好转、体重增加、咳嗽气喘症状好转等,虽然复查CT提示病灶增加,考虑“假性进展”。
2)使用PETCT作为评价标准,治疗前后SUV值没有增加反而降低,考虑“假性进展”。
3)可以对比一下患者的转移灶是否都同时增大,考虑“假性进展”。
4)通过对比抗PD-1/PD-L1用药前后白介素-8的变化,可以较早预测药物疗效,可以辅助诊断假性进展。
5)可以确诊“假性进展”的办法,就是对增大的病灶,穿刺取病理,如果穿刺结果提示免疫T细胞CD3CD4CD8细胞浸润明显增多,基本可以判断为“假性进展”。
肿瘤超进展
1)免疫治疗中肿瘤进展时间小于两个月
2)肿瘤负荷相比于基线期增长超过50%
3)免疫治疗后肿瘤生长速度超过之前速度2倍以上。
对于伴有MDM2/MDM4扩增、EGFR突变的患者也和超进展有关,具体机制尚不明确。
研究显示,老年患者更容易发生肿瘤超进展。
延迟反应
表现为肿瘤最终缩小或达到完全缓解前由一段时间的部分缓解、疾病稳定甚至病情进展。
主要原因是T细胞诱导、活化及浸润肿瘤组织,再到整个机体产生免疫应答的过程需要几周甚至数月的时间。一般8-12周围判断标准。
混合缓解
表现为不同部位肿瘤病灶的缩小、稳定或增大同时存在,虽然没有达到客观有效的标准,但是患者确实有临床获益的表现。主要原因考虑不同器官对免疫治疗的敏感性不同所致。
假性进展和真性进展,有时候从出现的时间,从影像上的表现都很难判断,所以多数情况下要结合病人的一般情况。对于假性进展的判断,一定要经过继续治疗两个周期以后再评估。如果继续用药两个周期以后,肿瘤还在持续进展,这个就一定不是假性进展。基于免疫治疗反应的特殊性,一定需要使用免疫的肿瘤评估指标。
来源:丁丁医聊