疫苗

疫苗是生物制品,是应用传统方法或基因工程等生物技术,由获得的微生物和微生物的蛋白、多糖或核酸等生物材料制成,用于人类疾病的预防和治疗。
根据制备疫苗的技术和疫苗成分,疫苗分为传统疫苗和新型疫苗或高技术疫苗。
传统疫苗包括:灭活疫苗、减毒活疫苗和从微生物及其衍生物分离提取的亚单位疫苗,如蛋白疫苗和多糖疫苗。
新型疫苗包括:基因工程亚单位疫苗、重组载体活疫苗、核酸疫苗、基因缺失活疫苗、遗传重配疫苗及合成肽疫苗等。


疫苗研发的终极目标是通过药监部门的注册,投放市场,解决公共卫生问题。一般由免疫原的发现、候选疫苗的设计、候选疫苗的实验室研究、动物(模型)有效性与安全性验证、临床试验与新药注册等步骤构成。这些步骤可以依次进行,亦可以同时进行。治疗性疫苗与预防性疫苗不同,由于疾病免疫病理机制的复杂性,免疫原的确定、候选疫苗的设计及疫苗临床试验终点的选择更为复杂与耗时。当实验室研究与动物实验积累了足够的信息,且无法进一步预测候选疫苗应用于人体的效果时,意味着临床试验阶段的到来。

疫苗的临床研究
1
Ⅰ期临床试验:着重于疫苗的人体安全性评价,初步评价疫苗的免疫源性、剂量效应等特征。
2
Ⅱ期临床试验:着重验证疫苗在目标人群中的免疫原性、安全性及剂量效应,并初步评价疫苗的有效性(效力),包括人体攻毒试验。
3
Ⅲ期临床试验:目的在于确认疫苗针对目标人群的有效性(效力、疗效)与安全性,为疫苗注册申请提供充分的依据。
4
Ⅳ期临床试验:指疫苗获准上市后的研究,只涉及药监部门批准的适应症。
尽管疫苗的临床研究被分为4个周期,但这种“周期”并不等同于临床研究的分类。同一类型的临床研究可以出现在不同的周期。因此,ICH 指南中采用了更为合理的、根据研究目的的分类系统,即依次为人体药理学、治疗作用探索、治疗作用确证与临床应用。


临床试验的设计
1
随机化:可以确保试验组与对照组受试对象的可比性,从而避免那些可能影响研究结论的组间系统误差。
2
对照:该选择会对临床试验结果的推论、效力评价中的偏倚、实施过程中的可行性,甚至药政部门对研究数据的可接受性均产生影响。常见的对照包括:安慰剂对照、空白对照、阳性对照和外部对照。
3
盲法:采用盲法,使受试对象和研究人员都不知道受试对象的分组和服用药物情况,可以消除受试对象和(或)研究人员主观因素的影响。盲法包括:单盲、双盲和三盲。
4
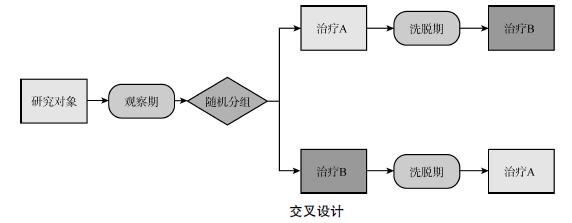
设计类型:常见的临床试验设计分为平行设计与交叉设计。对于平行设计,每个研究对象仅接受1次治疗或干预措施;而对于交叉设计,每个研究对象则接受2次及以上的治疗或干预措施。


临床试验的质量保证与
质量控制
1
临床试验管理规范:为了保证临床试验结果的真实与准确性,并保护试验对象的权利、完整性和机密性,由ICH编纂的《药品临床试验管理规范》(good clinical practice,GCP)为各国药政当局所采纳,成为临床试验设计、实施、执行、监察、稽查、记录分析和报告的国际标准。ICH GCP共提出了13项原则。

2
临床试验注册:目前,我国大陆开展的临床试验多选择在世界卫生组织国际临床试验注册协作网内的中国临床试验注册中心(http://www.chictr.org.cn)或美国国立卫生研究院的ClinicalTrials.gov(http://www.clinicaltrials.gov)上注册。两个数据库的注册都被国内外杂志承认。
3
临床试验的网络:临床试验,特别是新型疫苗效力评价的临床试验往往耗时、昂贵,涉及多个机构、组织。这些共同合作的组织包括研究机构、制药公司、合同研究组织、政府药政部门、机构审查委员会(伦理委员会)、独立的数据和安全监察委员会等。这些机构和组织各行其职,通过一定的机制形成了临床试验的质量控制和受试对象的权利保护网络。


本文部分文字摘自《治疗性疫苗》(第2版),随着临床医学研究的进展,近10年来,治疗性疫苗作为一种新的治疗技术,已取得大量重要的理论与实践成果。本书第2版在全面更新治疗性疫苗的作用机制及应用经验基础上,加强了产业化、成品化的内容并部分拓宽至免疫治疗。全书共分两部分:总论部分从整体理论和技术方面进行阐述,概括了疫苗及其种类,持续性感染,治疗性疫苗的历史、理论和实验基础、动物模型,各种类型的治疗性疫苗,以及治疗性疫苗的临床研究、验证和质控等;各论则深入介绍了一些具体的治疗性疫苗,包括乙肝、丙肝、艾滋病、人乳头状瘤病毒、结核病、细菌持续性感染、肿瘤、自身免疫病及神经退行性疾病治疗性疫苗等。本书适合临床医学、免疫学,以及从事疫苗等生物制品研究和开发的科技人员、教学人员及研究生参考使用。



科学出版社赛医学(sci_med)
科学出版社医药卫生分社订阅号