导 语
乳腺癌是全球女性中最常见的恶性肿瘤之一,5年生存率约为70%-90%。“治愈”成为了早期乳腺癌治疗所追求的“主旋律”,而在围术期就更早地给予有效治疗方案将大大增加患者治愈机会。普遍认为,新辅助治疗目的是降期手术、降期保乳、降期保腋窝,或者决定体内药敏试验,具体看新辅助治疗后肿瘤退缩情况。但如果仅以体内药敏试验作为新辅助治疗目的,至少得有很好的治疗策略。所以临床实践中需通过早期新辅助疗效来抉择后续治疗策略。
同时,生物制剂在全球范围内的应用日益广泛,在肿瘤治疗及肿瘤支持治疗领域占越来越重要的地位,随着原研药物专利到期,生物类似药便应运而生,热潮涌动。在乳腺癌领域,曲妥珠单抗原研药已上市18年,其生物类似药国内即将上市,生物创新药的价值以及在临床使用中如何合理选择也成为学者们关心的问题。
一、新辅疗效决定后续治疗策略
选择新辅助治疗之后,何时进行疗效判断?
辅助化疗是一个“全盲”的化疗模式,无法获得药敏信息(同样的方案可能会得到不确定的疗效);传统新辅助化疗是一个“半盲”的化疗模式,药敏信息获得太晚(全程既定新辅方案,pCR预后相对较好,non-pCR可强化辅助);疗效引导的新辅助化疗,强调基于早期疗效评估(如果敏感给予足量敏感治疗,豁免不必要毒性,如果早期判断耐药则尽早局部治疗干预,更换全身治疗方案),真正利用好药敏信息。
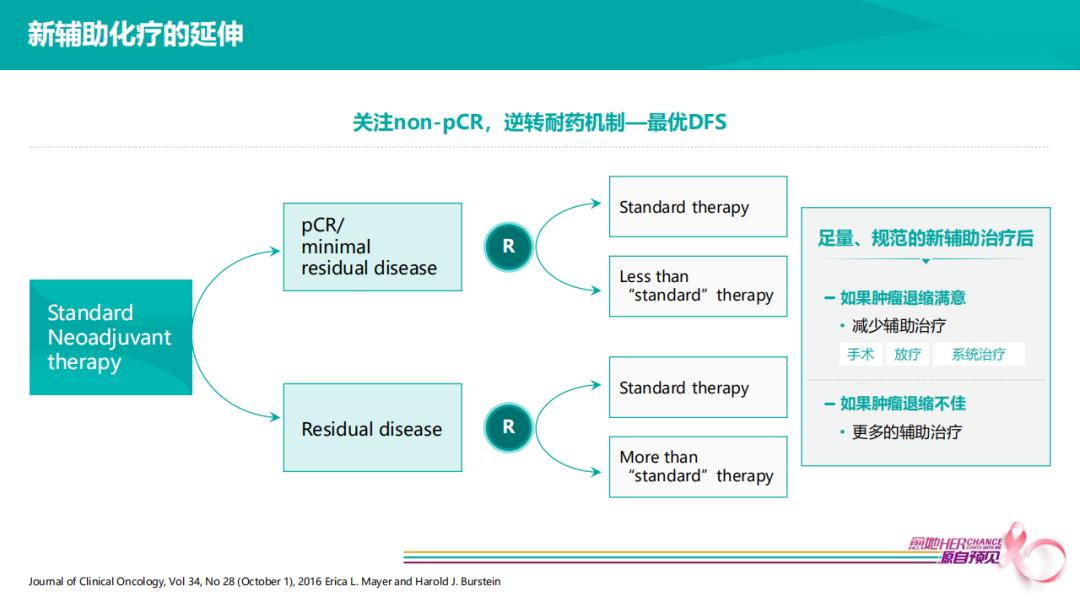
按照以上流程图将患者进行新辅助治疗,达到pCR患者预后很好,可尝试降阶梯治疗,non-pCR患者肿瘤退缩较差,可尝试进行辅助升阶梯治疗,但要获得最优DFS,有三个关键因素。
第一,完成足量、规范新辅助治疗后,才能在选择手术时,根据pCR/non-pCR选择升/降阶梯。例如,HER2+4个疗程EC,non-pCR时选择T-DM1辅助强化,并不符合当前循证医学证据;
第二,HER2+患者,即便全程双靶治疗达到pCR,仍有复发可能,所以在没有足够证据表明pCR患者可以选择降阶梯治疗时,当前对降阶梯仍需持谨慎观点,当患者达到pCR应乘胜追击完成后续足疗程双靶治疗。
第三,对于残留肿瘤,需通过全疗程筛选之后,non-pCR患者才能进行辅助强化。
早期如何判断疗效,如果早期疗效判断出不同结果,临床实践中如何优化后续治疗,值得进一步探索。

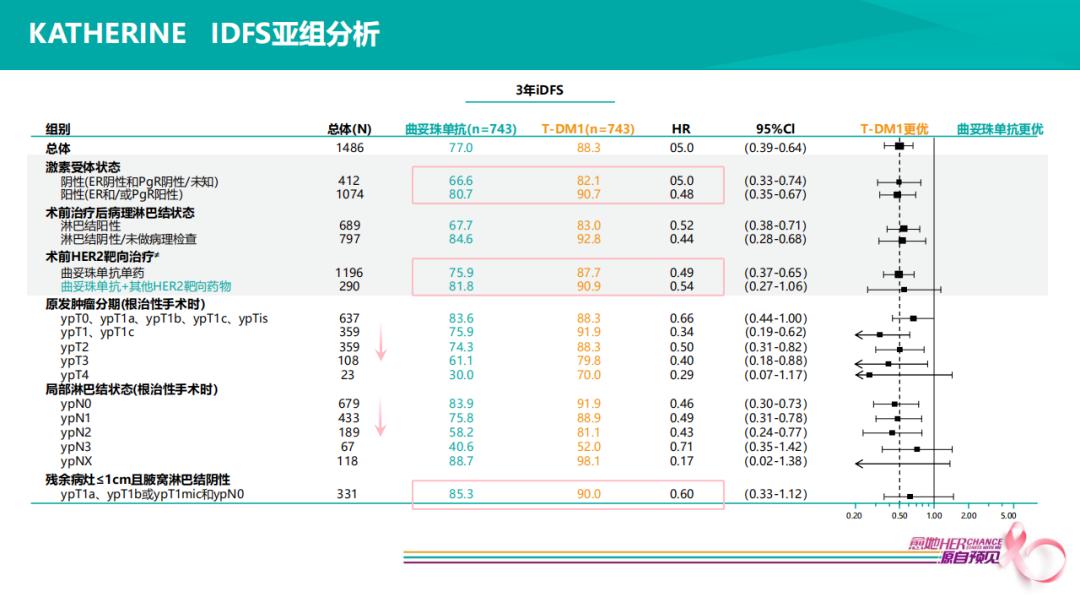
KATHERINE研究表明,HER2+患者选择6个疗程新辅治疗后,至少9周紫杉醇或9周抗HER2治疗后non-pCR患者,使用14个周期的T-DM1对比14个周期的曲妥珠单抗,iDFS降低50%,non-pCR患者,三年预后仍可控制在88%的高位,非常了不起的一个循证医学证据。
KATHERINE iDFS亚组分析显示,在术前HER2靶向治疗亚组,曲妥珠单抗组,双靶20% non-pCR患者,预后81.8%,单靶75.9%,T-DM1组,分别是90.9%和87.7%,提示双靶在新辅助阶段,不仅可以提高pCR率,也使得pCR和non-pCR的自然预后均得以改善。在残余病灶亚组,肿瘤残留越大,复发风险越高,预后越差,但似乎T-DM1逆转能力变得更强,HR值越好,即便肿瘤残留只有几毫米、N-、HER2+患者,通常认为选择好的新辅助治疗之后,4-5㎜ N-的残留已是这类患者中预后非常好的人群,T-DM1仍可降低复发风险40%(HR=0.60)。
KATHERINE研究带给我们哪些启示?
1、 新辅阶段如有残留,说明残留肿瘤细胞对新辅助治疗所采用方案耐药。
2、CREATE-X研究,卡培他滨对TNBC患者(HR:0.58);KATHERINE研究,T-DM1对于HER2+患者(HR:0.50)。卡培他滨是蒽环、紫杉治疗失败后,二线治疗策略,T-DM1是紫杉联合抗HER2治疗失败后二线治疗首选。Non-pCR提示体内耐药株的存在,需采用没有交叉耐药的方案进行辅助强化,可改善获益。如果可提早预测non-pCR肿瘤状态,那这部分患者没有必要人为延长带瘤时间,可选择行根治性手术,再行辅助强化治疗。
3、在临床实践中T-DM1可作为辅助强化治疗首选策略;如果因经济条件受限无法使用T-DM1,可考虑双靶方案,但T-DM1可以成为二线治疗首选策略,足以说明其逆转耐药能力最强。
4、以上所有方案均可在辅助阶段进行强化,但HR值或许达不到0.50,对于部分肿瘤退缩较好、残留负荷非常少的患者,完全可以期待PEONY临床实验将于2021年公布的5年随访结果,全组患者中,pCR/non-pCR是否双靶同样优于单靶,届时揭晓。Non-pCR肿瘤残留较小的患者,如果双靶比单靶能够获得非常漂亮的HR值,T-DM1或者曲妥珠单抗联合帕妥珠单抗都可作为辅助强化的可选治疗策略。
HER2+ EBC 新辅助策略
1、 有一定肿瘤负荷(T2N1及以上),或者有降阶梯、保乳、保腋窝需求的HER2阳性eBC患者,优选新辅助治疗,并选择PCHP为初选方案。
2、 根据早期疗效评估,有效患者应完成足疗程的PCHP方案,最终达到pCR,辅助PH维持一年全程治疗;non-pCR患者,辅助T-DM1强化治疗。
3、 如果患者疗效不佳,推荐尽早手术,此时采用两个疗程PCHP之后完成手术,辅助阶段补足4个疗程EC,随后根据KRISTINE研究方案,用帕妥珠单抗+T-DM1进行全程辅助强化治疗。
二、生物创新药不可复制的旅程
生物创新药研发、上市历程:万里挑一、身经百战
生物创新药的研发历程可谓万里挑一、十年磨一剑:从成千上万个化合物中挑选药物进行临床前研究(3-6年),再进行6-7年的临床试验,筛选出1种经FDA等审批机构获批的上市药物,大规模应用于临床。
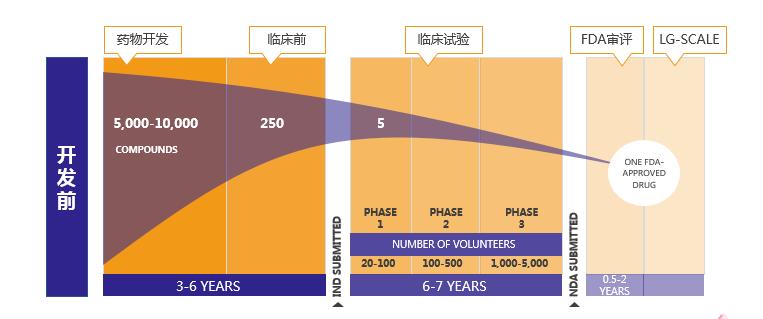
以曲妥珠单抗为例,从发现HER2/neu基因至进入临床研究就已经历了10年历程,而后十多年时间里又逐步实现乳腺癌全疗程的覆盖。每一个适应症的背后都有大量的临床证据验证其疗效和安全性。
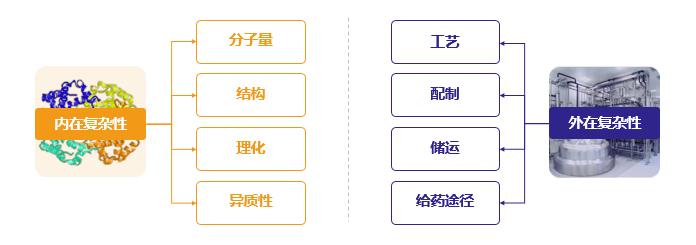
生物制剂的特点:无法完全复制
生物制剂的内在、外在复杂性致使生物类似药难以完全复制:生物制剂分子量较大;存在多级复杂结构;异质性大,潜在变异体可能有1亿个;生产工艺复杂;理化性质与内部结构高度相关,任何微小的改变均可能影响生物制剂的疗效和安全性。
生物制剂的临床应用:需要谨慎选择
生物创新药除了药物本身无法被完全复制以外,其临床验证、适应症的获得过程同样为不可复制的创新探索之旅。
1. 原研创新药以给患者带来明确生存获益的临床研究为基础,生物类似药的开发过程需逐步递进地与原研药进行相似性评价,重临床前研究而轻临床研究;
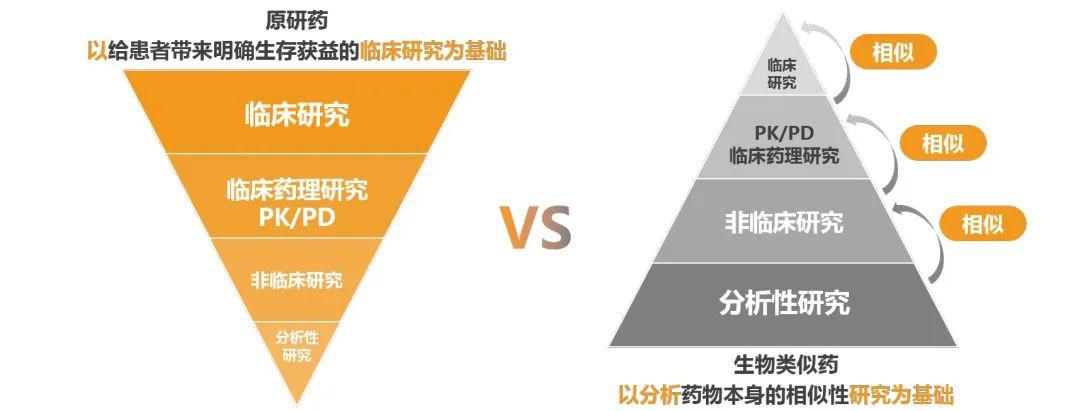
2. 原研创新药采用优效性评价疗效和安全性,生物类似药是等效性评价,与参照药相似即可。然而目前监管机构对等效界值的设定尚无具体要求和标准;
3. 原研创新药需在不同人群中进行研究,以曲妥珠单抗为例,通过从乳腺癌晚期到早期的不断探索,才筛选出如今的“敏感”人群,而生物类似药可以只选择敏感均一的研究人群;
4. 原研创新药与生物类似药的临床研究终点也有所不同。原研药多采用OS、PFS等作为临床研究终点,生物类似药多采用ORR。但是研究证实,OS是判断肿瘤药物疗效的金标准,ORR仅为替代终点;
5. 原研创新药每一个适应症的获得均基于充足的临床证据,生物类似药在一种适应症中取得相似评价后即可外推至原研药已获批的其他适应症。但由于临床研究的不足,其在其他适应症中的疗效和安全性存在一定的不确定性。
由此可见,生物类似药在临床应用中尚存在一些问题:长期疗效与安全性、免疫原性、适应症外推/互换等。上市后仍需要强有力的药物警戒和风险管理。
基于不同的开发过程,生物药临床应用需谨慎:以能给患者带来明确生存获益的药物为首要考虑因素,以不能给患者带来安全风险为前提,以药物经济学为考虑出发点,持续的药物警戒监管。
*本文未经过同行评议,仅供医学专业人士参考。
参考文献【略】
