简单的DNA和RNA纯法方法大幅推动了基因组和基因表达的分析和鉴定。人们需要快速、方便地从多种细胞来源分离DNA和RNA,包括哺乳动物、植物和细菌培养物来源的细胞和组织。传统DNA分离和纯化方法基于多步骤程序,涉及苯酚/氯仿、阴离子交换或硅胶交换系统。RNA纯化通常涉及离液盐和苯酚/氯仿,且针对mRNA需采取进一步的oligo-dT纯化步骤。更多内容请到默克生命科学官网查看:www.sigmaaldrich.cn
PCR或RT反应物中的模板材料质量对于数据结果可靠性有深远的影响1。因此,必须确保靶标质量经过鉴定和报告实证2,最好使用最高质量的核酸。本章着眼于纯度和完整性,深入分析了靶标质量对于得到的qPCR和RT-qPCR数据的影响。
对于大部分分子生物学的实验来说,核酸纯化是首要要求。DNA和RNA样品通常通过“粗制”制备。现有的这些纯化方法快速、直接,尤其PCR/RT-PCR只需少量样品DNA或RNA时更为适用。部分应用需要通过传统方法纯化的样品;最终应用场景决定了要选择的最佳方法。需要确保来自生物材料的核酸完整无损、纯净、浓缩且不含下游酶促反应*制剂抑**时,提取过程需要添加离液剂。
离液剂是一种通过破坏分子的三维结构从而使得蛋白质、DNA或RNA变性的物质。离液剂妨碍由非共价力介导的分子内相互作用稳定性,例如氢键、范德华力和疏水作用。常用的离液剂包括尿素(6-8M)、盐酸胍(6M)和高氯酸锂(4.5M)。异硫氰酸胍是一种比盐酸胍更强效的蛋白质变性剂,通常在分离完整的核糖核酸时被用来消除RNase活性。许多RNA分离方案中除了离液剂之外还添加巯基乙醇,以提供还原环境,使得核糖核酸酶A(RNase A)的八个半胱氨酸残基之间形成的四个二硫键变性。离液剂和还原剂如巯基乙醇的组合导致核糖核酸酶展开并完全丧失活性。
粗提
Extract-N-Amp™试剂盒使用简单的单管方案,几乎可从所有类型样品中快速有效地提取用于PCR的基因组DNA(gDNA)——仅需15分钟或更短时间,具体时间因样品而异。Extract-N-Amp试剂盒已用于从全血、毛囊、小鼠尾巴标记、组织培养细胞、口腔拭子细胞、果蝇、各种植物和种子等样品中提取gDNA。与完全纯化程序不同,该方法避免了机械破坏、有机萃取、柱纯化或DNA沉淀。该试剂盒含有DNA提取和扩增试剂,可用于PCR/qPCR分析等许多下游应用。
基因组DNA纯化
几乎所有细胞或组织来源样品均可分离出DNA。gDNA纯化既要从细胞中分离DNA,又要避免其自身的降解。分离程序也必须足够温和,以保护DNA长链免受机械应力。首先用磷酸盐缓冲液(PBS)等缓冲液中处理样品——此类缓冲液中通常含有Triton™ X-100或十二烷基硫酸钠(SDS)等用来裂解细胞、溶解蛋白质和脂质的去垢剂。加入蛋白酶 K,通过蛋白酶消化来分离成簇的细胞和组织,并使酶失活。乙二胺四乙酸(EDTA)是一种螯合剂,可作为溶液中金属离子的清除剂,添加到DNA纯化缓冲液中以去除镁离子(Mg2+)。Mg2+是DNase的必需辅助因子,因此去除Mg2+会使DNase失活,从而阻止DNA降解。RNase常用来降解细胞中存在的RNA。
在裂解细胞并降解RNA、蛋白质和脂质后,必须将DNA与这些材料的剩余残余物分离。传统纯化方法使用苯酚/氯仿3去除蛋白质,留下DNA和其他水溶性物质。TRI Reagent®改进了该方法。通过改用GenElute™ gDNA纯化试剂盒等体系,可将DNA吸附到二氧化硅基膜(单柱和96孔板)上,在存在离液盐的情况下破坏蛋白质结构。从植物材料纯化DNA时,必须首先在液氮中研磨机械破坏组织,而全血或细菌则与酶预培养以确保有效的裂解细胞和释放DNA。在DNA与膜结合后进行洗涤,然后通过改变盐浓度进行洗脱,随后用去垢剂和离液剂释放DNA。用沉淀法除去蛋白质、多糖和细胞碎片,随后用过滤柱进行离心。
细胞RNA纯化是研究基因表达或其他RNA调控细胞功能所必需的步骤。总RNA是从细胞DNA(gDNA和线粒体DNA即mtDNA)转录的RNA,通常含有:核糖体、转运和信使RNA(rRNA、tRNA和mRNA)并且不包含microRNA(miRNA)或更小的非编码RNA(ncRNA)的样品。总RNA是针对基因表达分析而分离的目标组分。
RNA分离之所以困难,是因为细胞和组织中普遍存在的核糖核酸酶(RNases)会快速降解RNA。因此,在纯化过程中会使用RNase*制剂抑**。最常用的纯化方法是异硫氰酸胍-苯酚/氯仿萃取。这是TRI Reagent®的原理,后者是一种含有苯酚和硫氰酸胍的单相溶液。将组织或细胞样品在TRI Reagent中进行均质化或破碎,将氯仿与裂解物混合,然后通过离心将混合物分成三相。除去含有RNA的水相,用异丙醇沉淀RNA。在细胞裂解后,可利用GenElute RNA分离试剂盒将RNA捕获到硅树脂上。当分离总核和细胞质RNA时,GenElute试剂盒使用硫氰酸胍和2-巯基乙醇使RNase失活。存在硫氰酸胍时,由于蛋白质二级结构丢失,蛋白质易于溶解,细胞结构瓦解,核蛋白从核酸解离。此外,由于硫氰酸胍比盐酸胍更有效,因此RNase的变性是永久的。将裂解物通过过滤柱旋转离心以除去细胞碎片并剪切DNA。然后将滤液加到高容量硅胶柱上以结合总RNA,然后用不含RNase的水或缓冲液进行洗涤和洗脱。
在总RNA样品中,主要部分是rRNA(~80%),而mRNA部分仅为2-5%。对于一些程序,可能需要从大量的rRNA和tRNA中纯化mRNA。GenElute mRNA试剂盒提供了一种方便程序,用来从之前制备的总RNA或直接从哺乳动物细胞和组织中分离多聚腺苷酰mRNA。如需直接制备mRNA,可以用SDS /蛋白酶K消化破坏细胞或组织以释放RNA并消除RNase。随后使用与1 μm聚苯乙烯微球共价连接的Oligo dT30通过杂交法捕获多聚腺苷酰mRNA。聚苯乙烯微球在杂交过程中保持悬浮状态,无需混合或摇动。在微量离心自旋过滤器上洗涤mRNA-微球复合物,然后洗脱纯化的mRNA。
用于纯化“总RNA”的许多提取方法会特异性地选择较大的分子,因此不适合用来分离较小的ncRNA,包括miRNA。有专门设计的用于纯化较小RNA种类的试剂盒,当目标模板为上述RNA时可以选用。
小分子RNA (miRNA) 和非编码RNA(ncRNA)纯化
由于长度较短,miRNA和其他更小的ncRNA分子的纯化更具挑战性。重要的是选择适当的RNA分离方法来保留小RNA,避免使用总RNA纯化试剂盒,除非厂家明确指出总RNA包括<100个碱基的小RNA。ncRAN的提取方法针对RNA分子与其他污染因子的差异,使用特异性柱结合或沉淀法进行。RNAzol®是一种酸性硫氰酸胍-苯酚混合物,可破坏细胞和组织,并且,通过加入氯仿或溴氯丙烷,可将所有RNA种类与蛋白质和DNA分离。随后的纯化方法允许单独制备小RNA、mRNA或总RNA样品,使得可以在下游应用中平行分析所有这些片段。miRPremier® microRNA分离试剂盒是基于硅胶的结合-洗涤-洗脱试剂盒,专为回收小RNA而设计。miRPremier试剂盒使用盐析法在小RNA与柱结合之前去除较大的分子,因为将小RNA与硅(二氧化硅)结合所需的乙醇量也会使蛋白质和其他大分子沉淀,形成粘性悬浮液,从而阻塞柱并阻止RNA的有效回收。避免该问题的另一种方法是使用预清除步骤去除大分子,例如使用RNAzol或预结合柱进行提取,从而可以加入足够的乙醇来结合小RNA而不堵塞RNA结合柱。
样品处理和核酸提取的程序是可变的,因此确定一个可靠方案分析样品质量和数量并且在出版物中详述该分析的细节至关重要2。RNA的数量很大程度上取决于rRNA的产率,而RNA的质量取决于RNA分子的纯度(无*制剂抑**)和完整性。然而,在测定样品质量时,纯度和完整性会影响结果;对于低浓度样品,难以确定其纯度和完整性,同时杂质的存在会干扰定量。有许多技术可用于评估核酸数量和质量,但其中没有一种能够单独提供充分描述样品所需的全部信息。因此,重要的是要考虑一系列选项,以确保样品质量不会影响最终的分析数据1。
核酸定量
紫外光谱
通常使用分光光度计测量UV吸光度来对核酸进行定量。在260nm和280nm处读取稀释的DNA或RNA样品的吸光度。基于比尔-朗伯定律,以260nm处的光密度(OD)来确定溶液中的RNA或DNA浓度,该定律预测了吸光度和浓度之间的线性相关性。
比尔-朗伯定律
A = εbc A = 吸光度b = 比色皿的路径长度,以cm为单位(通常为1cm)c = 分析物浓度ε = 消光系数 对于RNA, ε = 40 μg/mL对于DNA, ε = 50 μg/mL
当260nm处的OD值(A260)读数为1.0时,相当于约40 μg/mL的纯RNA和50 μg/mL的纯双链DNA。然而,比尔-朗伯定律仅当OD读数在2以内有效,并且所述OD /浓度关系取决于样品的纯度。显然,污染物质在260nm或280nm处的吸收将影响估计的OD读数。纯RNA的A260/A280为2.1,而纯DNA的A260/A280为1.8。
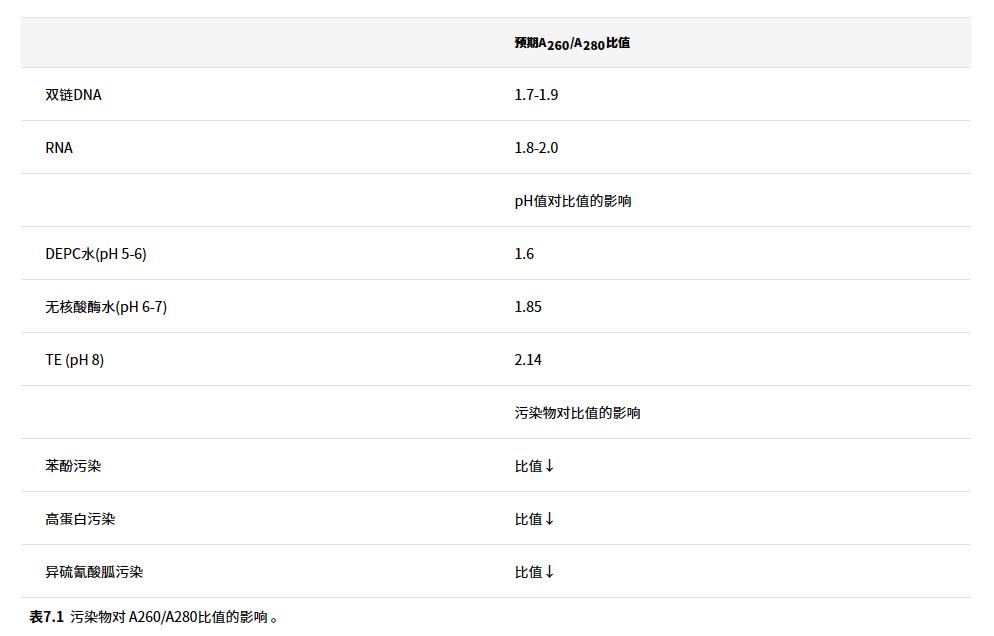
如果在280nm和230nm测量样品的吸光度(分别为A280和A230,),也可以确定潜在的污染物如蛋白质、离液盐和苯酚的OD值。因此,A260/A280和A260/A230的比值可以用作样品纯度的指标。但是,应该注意的是,这种方法对DNA中蛋白质污染的测定非常不敏感4。
此外,缓冲液的pH值和离子强度也会干扰OD读数。研究发现,当使用不同来源的水进行分光光度测定时,A260/A280的比值存在显著差异。例如,当用来悬浮RNA的水的pH值从pH5.4变化到7.5-8.5时,RNA的A260/A280比值显著增加,大约从1.5到2.05。
重要的是的A260/A280比值和A260/A230比值都接近2.0(表7.1)。