
问题: 酪氨酸激酶*制剂抑**在治疗骨肉瘤中具有一定的疗效,且能够增强患者的化疗敏感性。那么,酪氨酸激酶*制剂抑**联合化疗对骨肉瘤患者的疗效如何?
结果: 本研究共分为两个阶段,第一阶段为确定联合治疗的药物剂量(3A,15例),第二阶段为扩展患者队列的验证(3B,20例)。
研究结果显示,35例入组患者中有18例患者4个月的无疾病进展生存率为51%(95% CI 34-69)。安全性方面,35例患者中有26例出现治疗相关不良事件,但无治疗相关死亡。
结论: 本研究显示,对于难治性或复发性骨肉瘤患者,酪氨酸激酶*制剂抑**(乐伐替尼)联合化疗(依托泊苷和异环磷酰胺)初步显示出了一定的抗肿瘤活性以及可控的安全性。

发表期刊:Lancet Oncol.
影响因子:41.32
发表时间:2021 Sep
01
研究背景
难治性或复发性骨肉瘤是临床治疗的一个挑战,这类患者预后较差,且尚无确定的治疗标准。
根据欧洲肿瘤医学会指南,难治性或复发性骨肉瘤的系统性治疗主要为化疗(异环磷酸酰胺联合依托泊苷或卡铂;吉西他滨联合多烯紫杉醇等),或酪氨酸激酶*制剂抑**治疗(索拉菲尼或瑞戈非尼)。
酪氨酸激酶受体通路相关基因突变,包括VEGF、FGF和PDGF等,与骨肉瘤的生长、侵袭和转移有关。众所周知,酪氨酸激酶*制剂抑**对包括骨肉瘤在内的多个癌种具有一定的活性。也有研究表明,酪氨酸激酶*制剂抑**能过通过修正患者血管结构,从而提高肿瘤细胞对化疗药物的敏感度。因此,酪氨酸激酶*制剂抑**联合化疗可能是治疗骨肉瘤的新思路。前期对骨肉瘤PDX模型实验证明,乐伐替尼联合依托泊苷和异环磷酰胺具有抗肿瘤活性,但是目前临床研究结果尚无数据。
本研究是一个多中心、开放性1/2期临床试验,招募了2-25岁的有可检测或可评估病灶的复发性/难治性骨肉瘤患者,且要求既往VEGF或VEGF受体靶向治疗次数不超过2次,预期寿命至少还有3个月。1期(3A队列)目的是探索联合方案的剂量,2期(3B队列)进行扩展研究。1期的主要终点是通过评估剂量限制性毒性,明确最佳推荐的2期使用剂量,2期的主要终点是患者4个月时的无进展生存期。

▲ 患者入组及分析流程
02
研究结果
2.1 患者PFS分析
2016年5月-2019年6月,3A队列筛选入组了30位患者;2018年9月-2019年7月,3B队列筛选入组了22位患者。3A队列和3B队列分别纳入了22位和20位符合要求的患者。
在该研究联合方案中,乐伐替尼推荐的最佳2期剂量设为14 mg/m2·天(每日上限为 24 mg)。1期(3A队列,n = 15)和2期(3B队列,n = 20)共35位患者接受了乐伐替尼最佳的2期剂量治疗,并被汇总进行预后分析。预后分析显示,35例患者的4个月无进展生存期率为51%(95% CI 34-69)。
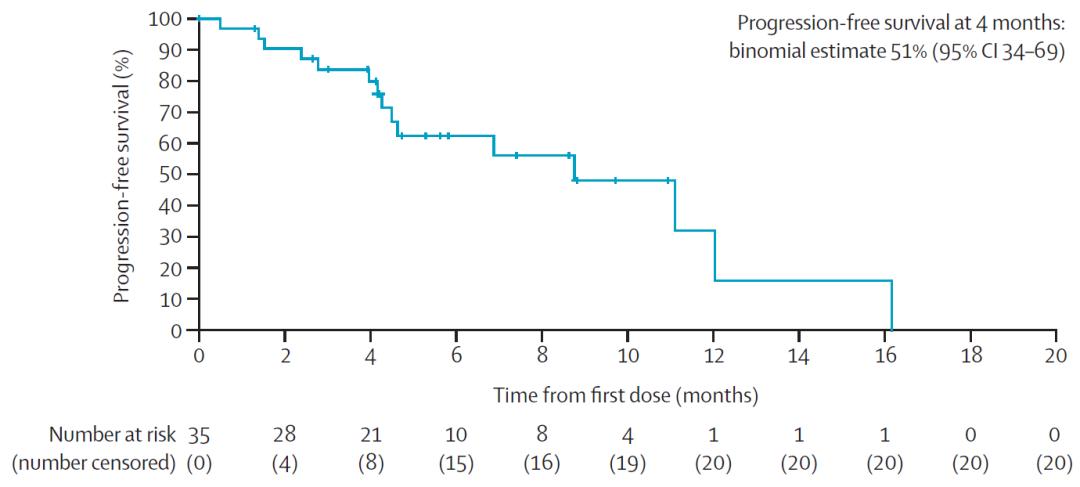
▲ 患者OS和PFS分析
2.2 安全性评估
在安全性方面,患者最常见的3-4级治疗相关不良事件主要有中性粒细胞减少(77%)、血小板减少(71%)、贫血(54%)和白细胞计数降低(54%)。35例入组患者中有26例(74%)发生了严重的治疗相关不良事件,但无治疗相关死亡病例。整体而言,乐伐替尼联合依托泊苷和异环磷酰胺具有可控的安全性。
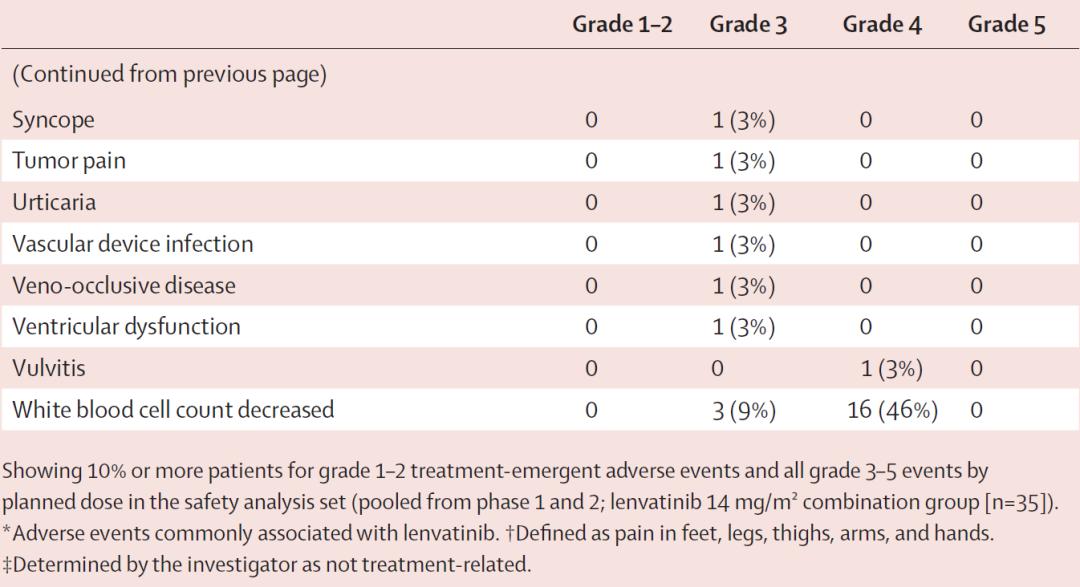
▲ 患者安全性分析
03
研究结论
本研究证实,“乐伐替尼+依托泊苷+异环磷酰胺”的联合治疗方案在复发性/难治性骨肉瘤患者中展现出了令人期待的抗肿瘤活性及可控的安全性。 后期进行扩大研究队列的3期临床试验将能够进一步验证这一组合疗法,为骨肉瘤患者提供新的治疗选择。
参考文献
1. Zhang Y, Yang J, Zhao N, et al. Progress in the chemotherapeutic treatment of osteosarcoma. Oncol Lett. 2018; 16: 6228–37.
2. Omer N, Le Deley MC, Piperno-Neumann S, et al. Phase-II trials in osteosarcoma recurrences: a systematic review of past experience. Eur J Cancer. 2017; 75: 98–108.
3. Yang J, Yang D, Sun Y, et al. Genetic amplification of the vascular endothelial growth factor (VEGF) pathway genes, including VEGFA, in human osteosarcoma. Cancer. 2011; 117: 4925–38.
4. Kaya M, Wada T, Akatsuka T, et al. Vascular endothelial growth factor expression in untreated osteosarcoma is predictive of pulmonary metastasis and poor prognosis. Clin Cancer Res. 2000; 6: 572–77.
5. Yonucu S, Yιllmaz D, Phipps C, Unlu MB, Kohandel M. Quantifying the effects of antiangiogenic and chemotherapy drug combinations on drug delivery and treatment efficacy. PLOS Comput Biol. 2017; 13: e1005724.
6. Goorin AM, Harris MB, Bernstein M, et al. Phase II/III trial of etoposide and high-dose ifosfamide in newly diagnosed metastatic osteosarcoma: a pediatric oncology group trial. J Clin Oncol. 2002; 20: 426–33.
7. Berger M, Grignani G, Ferrari S, et al. Phase 2 trial of two courses of cyclophosphamide and etoposide for relapsed high-risk osteosarcoma patients. Cancer. 2009; 115: 2980–87.
