
以PD-1/PD-L1单抗为代表的免疫治疗药物,明显延长了非小细胞肺癌的患者的生存期。
目前认为肿瘤组织PD-L1的表达是PD-1/PD-L1单抗治疗前选择获益人群比较合理的生物标志物。但通过免疫组化检测肿瘤组织的PD-L1表达也存在取样难,存在时空异质性的局限。
近年来检测血液中生物标志物技术有了很大发展,比如检测血浆中的可溶性PD-L1、ctDNA、TMB(肿瘤突变负荷)等都成为了可能,但这些血液生物标志物用于选择PD-1/PD-L1单抗治疗获益人群、疗效监测等仍未成熟,不属于常规检测,仍需更多研究。
肿瘤组织PD-L1表达的局限性
要检测肿瘤组织的PD-L1表达需要通过外科手术或穿刺获取肿瘤组织样本,但要获取肿瘤组织通常会对患者造成一定的创伤,很多患者因为肿瘤大小位置,体能状态而不适合进行外科手术或穿刺,也就无法得知肿瘤组织的PD-L1表达了。
肿瘤组织PD-L1表达还存在时间和空间上的异质性,时间上的异质性可以表现为治疗前后PD-L1的表达会发生变化,空间上的异质性则是肿瘤不同位置以及身体不同部位的转移瘤的PD-L1表达会有差异。由于肿瘤组织PD-L1表达时空异质性,仅仅一次取样有时无法反映肿瘤PD-L1表达的全貌。但我们知道获取肿瘤组织是有创伤,因此也不能频繁地进行检测。
通过血液检测生物标志物有可能避免肿瘤组织检测的局限性,血液检测只要抽血,创伤很小,可以多次检测,动态监测生物标志物的变化,而且可以监测全身的肿瘤状态。
免疫治疗相关的血液生物标志物
目前研究较多的免疫治疗相关的血液生物标志物包括可溶性PD-L1、ctDNA、血液TMB,这三项研究较多,是我们着重介绍的。
01
可溶性PD-L1
可溶性PD-L1存在于实体瘤患者的外周血中。研究表明,肺癌患者的可溶性PD-L1水平高于健康人群。可溶性PD-L1有预测肺癌患者预后的作用,一些研究显示可溶性PD-L1浓度高的患者,手术、放化疗后的生存期较短。那可溶性PD-L1浓度是否影响非小细胞肺癌免疫治疗疗效?
一项纳入39例晚期非小细胞肺癌患者的日本的研究显示,纳武利尤单抗(O药)治疗前可溶性PD-L1浓度较高的非小细胞肺癌患者疗效较差,在这个研究里面可溶性PD-L1浓度高低的界线为3.357 ng/mL。具体疗效差异见下表:
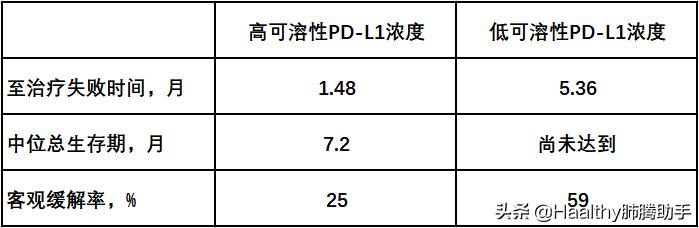
(图一 可溶性PD-L1浓度与非小细胞肺癌纳武利尤单抗疗效相关)
多因素分析显示,至治疗失败时间仍与治疗前可溶性PD-L1浓度显著相关,低浓度患者治疗失败风险降低63%(HR: 0.37, p = 0.041)。
而Costantini A等人的研究则不仅在纳武利尤单抗治疗前检测可溶性PD-L1的浓度,在首次治疗后2个月(首次疗效评估)也检测了可溶性PD-L1浓度,从而动态地监测纳武利尤单抗单抗的疗效。
研究纳入43例晚期非小细胞肺癌患者,结果显示,纳武利尤单抗治疗后肿瘤有缩小的患者,首次疗效评估时可溶性PD-L1浓度显著低于肿瘤没缩小的患者(中位浓度:32.94 pg/mL vs. 67.64 pg/mL)。
而纳武利尤单抗治疗临床获益(客观缓解+疾病稳定6个月以上)的患者,首次疗效评估时可溶性PD-L浓度显著低于无临床获益患者(中位浓度:34.14 pg/mL vs. 67.64 pg/mL)。
首次疗效评估时可溶性PD-L1浓度的高低同样能预测疗效,浓度高度界线为33.97 ng/mL。
低浓度患者的中位无进展生存期相比高浓度患者显著延长(11.8个月vs.2.2个月),低浓度患者的中位总生存期相比高浓度患者同样显著延长(未达到vs.6.2个月)。
此外首次疗效评估时可溶性PD-L1浓度相比治疗前浓度升高的患者疗效较差,详见下表:
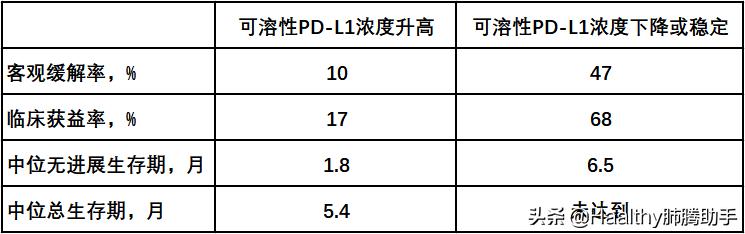
(图二 治疗前后可溶性PD-L1浓度变化与疗效相关)
上述研究的结果显示可溶性PD-L1有作为选择PD-1单抗获益人群生物标志物的潜力,但目前仍有未解决的问题:
1、可溶性PD-L1浓度高低的截取值是多少?这个目前是没有共识的
2、检测可溶性PD-L1的方法也没有标准化
3、肿瘤并不是可溶性PD-L1的唯一来源,非肿瘤疾病例如炎症、过敏、自体免疫性疾病、糖尿病,传染病等都会造成可溶性PD-L1浓度升高
4、其他:衰老、怀孕也与可溶性PD-L1浓度升高相关,这些与肿瘤因素导致的可溶性PD-L1浓度升高如何区分?
综上,可溶性PD-L1用于免疫治疗的生物标志物仍需进一步研究。
02
ctDNA
ctDNA是肿瘤患者外周血中游离的肿瘤DN*片A**段,目前对ctDNA的检测已经比较成熟,临床上也用于辅助指导非小细胞肺癌的靶向治疗。一些研究也显示ctDNA可预测免疫治疗的疗效。
例如Goldberg SB等人的研究显示,ctDNA水平的变化可预测免疫治疗的疗效,研究纳入49例晚期非小细胞肺癌患者,患者在免疫治疗前检测ctDNA,之后在整个随访期间定期检测ctDNA。研究将ctDNA缓解定义为第二次连续测量确认的ctDNA水平降至治疗前的50%以下。
研究结果显示ctDNA缓解与影像学评估的肿瘤缓解有很强的相关性,在24例影像学评估肿瘤部分缓解的患者中有10例ctDNA缓解。免疫治疗后肿瘤缩小的患者与无缩小的患者相比,ctDNA水平下降的幅度更大。
此外ctDNA缓解的出现领先于影像学缓解,具体来说,出现ctDNA缓解的中位时间为治疗后的24.5天,而出现影像学缓解的中位时间为治疗后的72.5天。
此外ctDNA缓解的患者免疫治疗时间显著更长(205.5天 vs. 69天,p <0.001),疾病进展风险显着降低71%(HR = 0.29,p = 0.03),死亡风险降低78%(HR = 0.22,p = 0.053),但未达统计学差异。
上述研究显示ctDNA有潜力作为免疫治疗疗效监测的生物标志物。但目前为止,ctDNA用于免疫治疗监测的数据仅是从非常小的患者队列中收集的,大部分是回顾性的,证据等级不高。
而对于免疫治疗特有的进展模式,如假进展和超进展,ctDNA水平会如何变化,目前仍不清晰。此外ctDNA检测的技术和评估标准仍未建立。总之,ctDNA前景不错,但仍需更多研究工作。
03
血液TMB
TMB(肿瘤突变负荷)是指肿瘤组织每兆碱基中突变的数目,通常需用肿瘤组织检测。 除了用肿瘤组织评估TMB,现在也可以通过检测ctDNA的方式来评估TMB,这就是血液TMB。
肿瘤组织TMB和血液TMB能否作为预测免疫治疗的疗效预测标志物仍有争议。
CheckMate-026和POPLAR/OAK研究的探索性分析中提示高组织TMB/血液TMB患者能从免疫治疗中获益。但在KEYNOTE系列研究的探索性分析的结果显示组织TMB与疗效无相关性,无论组织TMB的高或低,帕博利珠单抗(K药)+化疗在鳞状和非鳞状非小细胞肺癌患者的一线治疗中均显示出生存获益。
TMB的评估技术方式,评估标准也缺乏共识。评估TMB的最佳技术是全外显子测序(WES),由于WES昂贵因此不能广泛使用。目前多数是通过搭配癌基因检测模板(CGP)的二代测序(NGS)技术评估TMB。
当前存在几种CGP,例如纪念斯隆·凯特琳癌症中心的MSK-IMPACT,Foundation One CDx(FICDx),Guardant 360,PlasmaSELECT 64和Foundation ACT。由于CGP不是真正的全外显子测序,那么不同基因检测公司用GCP评估的TMB与真正全外显子测序评估的TMB的一致性有多高呢?
目前只能说,GCP包含的基因数量越多,其评估的TMB与真正全外显子测序评估的TMB的一致性越高,简单说就是测的基因越多越一致,至少测150个基因才能与全外显子测序有稳定的一致性。
TMB高低截取值也没有标准,就是说多高的TMB才算高,每个研究,每个基因检测公司都不太一样,各说各话,而且这种一刀切的截取标准就一定能预测患者的疗效吗?也不能。总之,TMB目前仅供参考。
小结
血液检测免疫治疗相关的生物标志物有很多优点,创伤小,可动态监测,可监测全身肿瘤状态,但目前相关检测技术,标志物的有效性依然有很多问题,因此并未进入临床广泛应用,但相关研究依然在进行,相信不久的将来免疫治疗也会像靶向治疗一样,验个血就能方便的指导治疗。