本期内容如下:
适用人群:高一新生 一轮复习时基础薄弱的高三学生
高中化学的第一座山

如果你在学习物质的量的相关内容时感觉学习比较吃力,不要觉得意外,大多数初学者都和你一样。物质的量就是高中化学学习过程中要翻越第一座山。虽然刚开始学习爬着很吃力,但是当你回头看的时候你会发现此时的你应该在山脚下,也许连半山腰都算不上。事实上物质的量的相关知识就是将来化学学习的基石。未来它也许就像乘法口诀,你已经感受不到,但已经自然而然地在应用了。
物质的量的通俗理解

微观粒子都非常小,肉眼不能分辨,但是同样存在计数的需求。因此我们就把阿伏伽德罗常数(6.02×1023)个微粒看做一个整体来计数。我们把阿伏伽德罗常数个微粒定义为1mol。这样微观粒子的计数就不用一个一个去计数,而是1mol、1mol的去计数。
如果你还没有理解,可以举一个生活中的例子。如果我们学校给每个学生采购一定数量的曲别针,假设总共需要五万个。采购员与对方交易的时候会不会一个一个去清点数目呢?肯定不会!厂家可以把100个装成一盒,再把100盒装成一箱,这个时候一箱曲别针就有10000个,那么采购员只需要知道厂家的装箱标准1000个每箱,购买五箱就可以。这个过程中就是按10000个为一个计数单位来计数的。而物质的量就是以阿伏伽德罗常数个微粒为计数单位来计数的一种方式。
引入这个新的物理量以后我们就可以把宏观的体积和质量与微观粒子的数目联系起来了。还应对物质和化学反应有新的认识。比如CO2,你在初中就知道每个二氧化碳分子含有一个碳原子和两个氧原子,现在我们同样可以理解为每1摩尔的二氧化碳中含有一摩尔碳原子和两摩尔氧原子。比如反应H2SO4+2NaOH=Na2SO4+2H2O,在初中我们认为是一个硫酸分子和两个氢氧化钠反应生成一个硫酸钠和两个水,现在我们还可以看成是每一摩尔的硫酸和两摩尔氢氧化钠反应生成一摩尔硫酸钠和两摩尔水。
基本解题思路
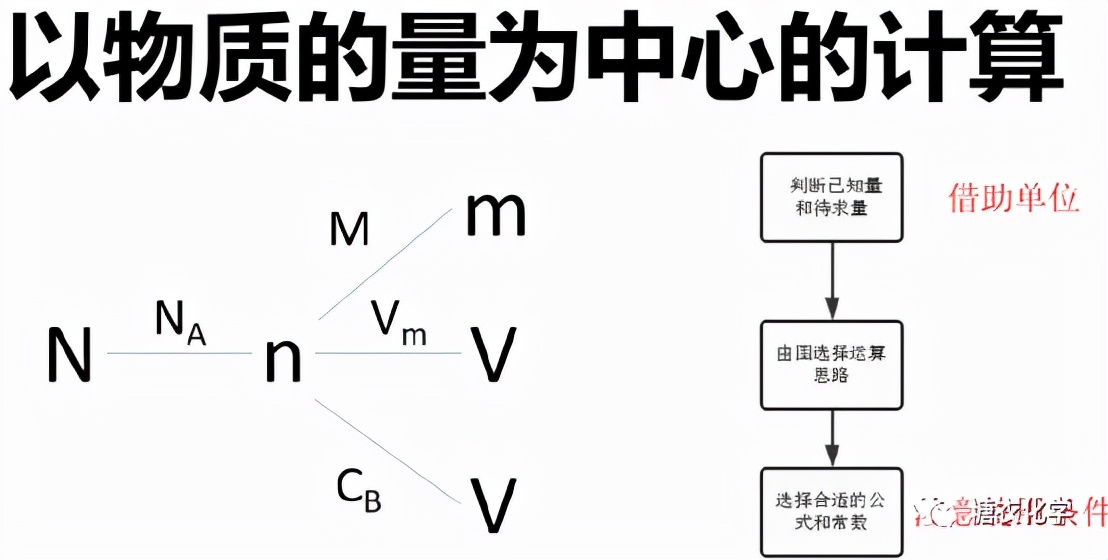
【化学学科核心素养】 宏观辨识与微观探析 变化观念和平衡思想