
撰文 | 咸姐
分子肿瘤分析 ( MTP ) 是一种基因组测试形式,旨在将肿瘤中的分子靶点与同源疗法联系起来。MTP涉及检测肿瘤样本以识别任何基因组或分子改变,以指导治疗选择,从而有利于发现针对癌症的个性化治疗,例如识别潜在地用于治疗特定癌症的新药物或提高治疗效果,同时减少不必要的副作用。在技术进步、患者需求和更有效癌症治疗需求的推动下,MTP已进入临床实践 【1】 。目前,美国食品和药物管理局 (FDA) 已经完全批准了五种针对晚期实体恶性肿瘤的靶向下一代测序 (NGS) 检测,并批准了几种额外的MTP试验的开发。这些FDA批准和预批准的实体恶性肿瘤的MTP检测使用石蜡包埋的肿瘤样本对DNA或RNA进行测序,并发布了数百个癌症相关基因突变和拷贝数改变以及少量的基因融合报告。然而,支持生物标记物验证、随后的靶向NGS检测和FDA批准的新的治疗性的临床试验并不包括患有实体恶性肿瘤的儿童,因此,目前没有关于儿童实体恶性肿瘤MTP的全国覆盖范围的确定的或实践指南。不仅美国,这一现象在欧洲和亚洲也是存在的。
其实一些患有实体恶性肿瘤的儿童患者已经在一些学术机构接受了靶向MTP治疗,来自7所机构的2000多名年龄在18岁及以下的颅外实体肿瘤患者的靶向测序数据已被存入美国癌症研究协会项目“基因组证据新生血管信息交换”数据库 【2】 。儿科肿瘤医生也使用商业化的靶向MTP,在2017年报道了711例儿科实体恶性肿瘤的测序结果 【3】 。最近发表的几项研究表明,对儿童癌症进行包括全基因组、全外显子组和全转录组在内的全面测序,可以在相当一部分儿童癌症患者中识别出临床相关的基因变异,其中一些患者将接受匹配的靶向治疗(MTT) 并对其产生了反应 【4, 5】 。然而,目前儿童实体瘤的MTP并不是通用的,癌症患儿缺乏MTP的国家护理标准以及获得现代分子分析的机会不均是如今一个重要的涉及健康公平和护理获得的问题。
近日,来自美国波士顿儿童医院的 Alanna J. Church 团队在 Nature Medicine 在线发表题为 Molecular profiling identifies targeted therapy opportunities in pediatric solid cancer 的文章, 对来自12个机构的345例颅外实体瘤儿童患者进行了前瞻性观察队列研究以评估MTP在实体恶性肿瘤患儿中的临床效果,从而促进了美国由数据驱动的保险范围决策和检测指南的制定,并为临床环境中的分子测试实践提供了信息。

GAIN/iCat2研究 (NCT02520713) 是一项多中心前瞻性观察队列研究,纳入了在全美12个儿科肿瘤中心确诊时年龄≤30岁的复发/难治性或高风险颅外实体瘤患者。所有患者都进行了靶向DNA组试验——OncoPanel的MTP,被选定的患者还同时进行了RNA测序 (RNA-seq) ,包括全转录组和靶向融合基因。本研究纳入分析人群的患者包括345名在2018年12月31日之前入组且在2019年4月4日前完成至少1次OncoPanel测序的患者,他们确诊时的中位年龄为12岁(0-27.5岁之间)。试验期间,对345名患者一共进行了438次成功的OncoPanel测试 (失败率7%) ,在其中50名患者的54份样本上成功地进行了RNA融合组试验,同时,全转录组测序和融合分析成功44例 (失败率为17%) 。利用这些分析结果,研究人员先后评估了这些基因组改变对治疗、预后和诊断的意义,并且发现添加全转录组和靶向RNA分析可以提高MTP效率。
首先,本文研究人员根据iCat证据等级评估将检测到的变异作为MTT潜在反应生物标志物的证据。在分析队列中,69%的患者至少有1个基因变异,并且已经对其提出了iCat治疗建议,在与iCat治疗建议相关的408个变异中,110(27%)个为基因融合、144个(35%)为拷贝数改变、154个(38%)为序列变异。第1级和第2级iCat治疗建议通常基于BRAF、SMARCB1、PIK3CA的改变和高肿瘤突变负荷 (TMB) ,而且超过5%的iCat建议的改变通常是较低级别的。iCat推荐的MTT代表了广泛的治疗类别,不过最常见的是DNA损伤反应*制剂抑**(23%)、表观遗传修饰剂(18%)、Ras-MAPK*制剂抑**(12%)和PI3K-Akt-MTOR*制剂抑**(11%)。进一步地,240名患者接受了可用于选择MTT的iCat治疗建议,其中有29名患者接受了MTT,其中24%的患者表现出客观反应或经历了持久的临床获益,而且除了一例以外,所有受试者均接受了与编码信号蛋白的基因融合相匹配的靶向治疗。
随后,按照分子病理学协会 (AMP) /美国病理学家学院 (CAP) /美国临床肿瘤学会 (ASCO) 指南,根据1级或2级证据,有56名(16%)患者出现1种或多种可能影响预后的改变。这些患者中没有一个在治疗方面发生改变,而且与诊断和治疗变异型不同,没有一种预后改变是基于基因融合的。
最后,根据临床影响解释的专业指南,有209名(61%)患者出现了诊断意义上显著的变异,其中168例(80%)具有结构变异,许多导致了特殊罕见儿童癌症特有的诊断的基因融合。MTP结果明确了17例患者的诊断分类,其中13例的分子改变为基因融合,在每个病例中,已确定的改变都会对患者的诊断分类和临床团队的管理产生直接影响。将本研究中使用的测序方法的诊断率与FISH和免疫组织化学 (IHC) 等传统检测方法进行比较,209例具有显著诊断结果的患者中有80例(38%)在传统检测方法中被漏诊,125例(60%)患者获得部分信息,4例(1.9%)患者的诊断改变可被准确识别,大约63% (209名患者中的131名) 的患者可被诊断,根据国家综合癌症网络指南,目前建议将分子检测作为一种潜在的分析方法。
综上所述,本研究对MTP对实体肿瘤患儿的临床影响进行了全面分析,其模型和工作流程直接适用于拥有针对NGS测试的监管批准和共识指南的美国和其他医疗保健系统。本研究中的肿瘤样本是在全国各地的医院按照自己的程序收集的,MTP是利用FFPE组织采用靶向分组试验进行的,负责治疗的肿瘤科医生收到MTP和临床解释报告后作出独立的患者护理决定。就是在这种分布式交付模型中,大多数患者都具有临床显著的MTP结果,345例患者中有298例(86%)有1个或1个以上具有诊断、预后和/或治疗意义的变异 (图1) 。 这些结果为“儿童”这一类患者群体的分子检测方法和未来儿科肿瘤研究工作的重点提供了信息。
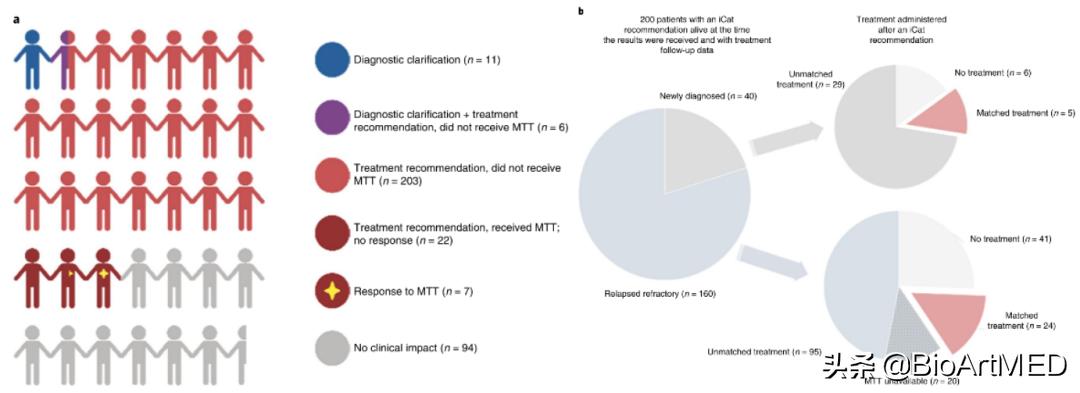
图1
原文链接:
https:/ / doi.org/10.1038/s41591-022-01856-6
制版人:十一
参考文献
1. Megan C Best, Nicole Bartley, Chris Jacobs et al. Patient perspectives on molecular tumor profiling: "Why wouldn't you?". BMC Cancer. 31;19(1):753 (2019).
2. AACR Project GENIE: Data (American Association for Cancer Research, 2022).
3. Chmielecki, J. et al. Genomic profiling of a large set of diverse pediatric cancers identifies known and novel mutations across tumor spectra. Cancer Res. 77, 509–519 (2017).
4. van Tilburg, C. M. et al. The pediatric precision oncology INFORM registry: clinical outcome and benefit for patients with very high-evidence targets. Cancer Discov. 11, 2764–2779 (2021).
5. Wong, M. et al. Whole genome, transcriptome and methylome profiling enhances actionable target discovery in high-risk pediatric cancer. Nat. Med . 26, 1742–1753 (2020).
转载须知
【原创文章】BioArt原创文章,欢迎个人转发分享,未经允许禁止转载,所刊登的所有作品的著作权均为BioArt所拥有。BioArt保留所有法定权利,违者必究。