
2020年3月,美国国家综合癌症网络(NCCN)发布了前列腺癌指南2020年第一版,相较于2019版第四版,新版指南有哪些更新要点呢?让我们一探究竟。
前列腺癌诊断(PROS-1)
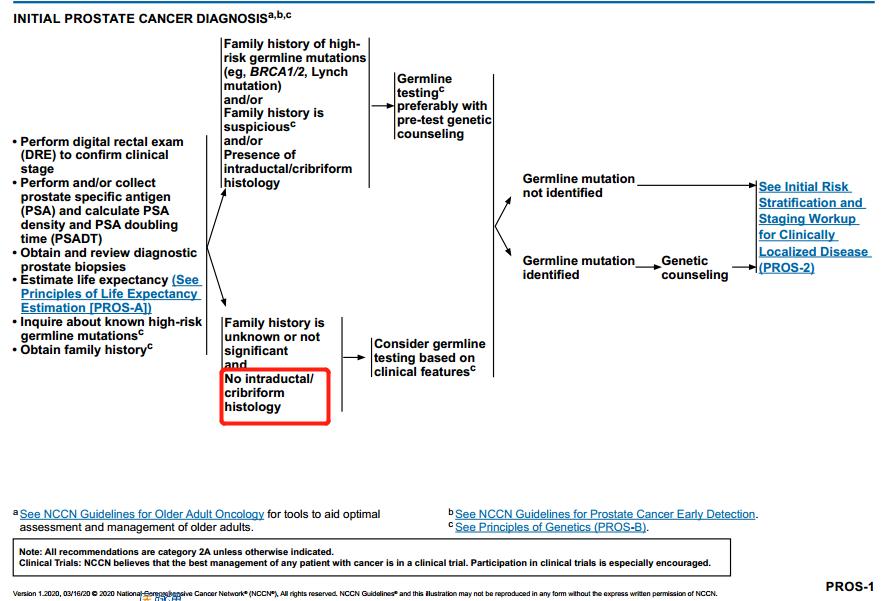
如果未发现胚系突变,则移除:如果基于家族史进行检测,则需进行遗传咨询以评估是否需要进行额外的检测。
将“导管内组织学”改为“导管内/筛状组织学”。
局限性前列腺癌的初始风险分层和分期(PROS-2)
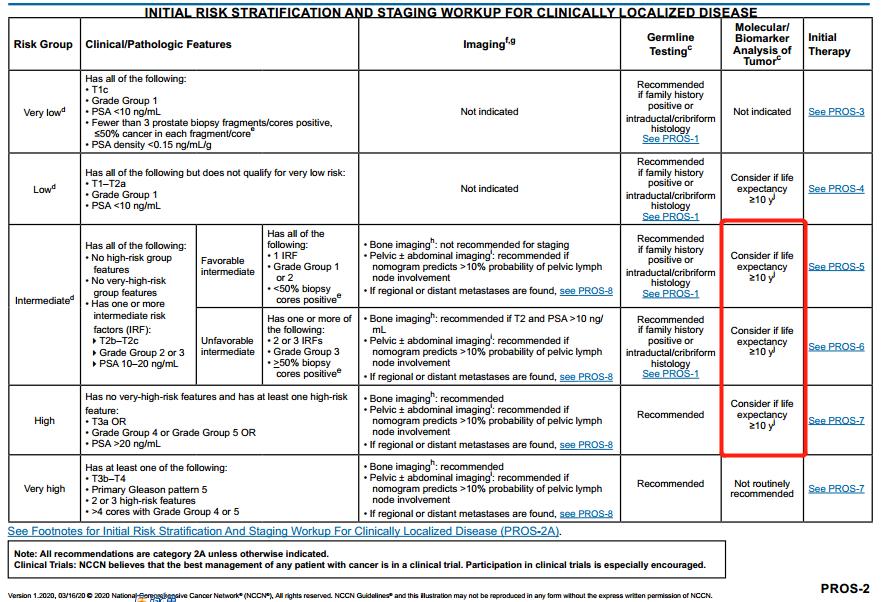
在中高风险组中,分子/生物标志物分析中,由“不常规推荐”改为“若预期寿命≥10年”。
PROS-2A
脚注修改为:对于无症状极低、低和中等风险组且预期寿命≤5年患者,在患者出现症状之前,不需要进一步的影像学检查或治疗,此时应给予雄激素剥夺治疗(ADT)。
新脚注:对于腹部/盆腔分期,mpMRI优于CT。
脚注修改为:对于低风险或预后良好中等风险且预期寿命10年以上患者,可考虑使用以下的分子检测:Decipher、前列腺癌Oncotype DX、Prolaris和ProMark。对于预后不良中等风险和高风险组且预期寿命10年以上患者,可考虑使用Decipher和Prolaris分子检测。

极低风险组(PROS-3),PROS-4,PROS-5,PROS-6,PROS-7
在极低风险组中,对于预期寿命20年以上的患者,根治性前列腺切除术(RP)初始治疗后若出现不良特征:辅助治疗可用外放射治疗(EBRT)± ADT(6个月)改为EBRT ± ADT(PROS-3)。
在低风险组中,对于预期寿命10年以上的患者,RP初始治疗后若出现不良特征:辅助治疗可用EBRT ± ADT(6个月)改为EBRT ± ADT(PROS-4)。
在预后良好中等风险组中,对于预期寿命10年以上的患者,RP±PLND(若预测淋巴结转移≥2%)初始治疗后若出现不良特征且无淋巴结转移:辅助治疗可用EBRT ± ADT(6个月)改为EBRT ± ADT(PROS-5)。
在预后不良中等风险组中,对于预期寿命10年以上的患者,RP±PLND(若预测淋巴结转移≥2%)初始治疗后若出现不良特征且无淋巴结转移:辅助治疗可用EBRT ± ADT(6个月)改为EBRT ± ADT(PROS-6)。
在高风险和极高风险组中,对于预期寿命5年以上的患者,RP±PLND初始治疗后若出现不良特征且无淋巴结转移:辅助治疗可用EBRT ± ADT(6个月)改为EBRT ± ADT(PROS-7)。

低风险组(PROS-4)、预后良好中等风险组(PROS-5)
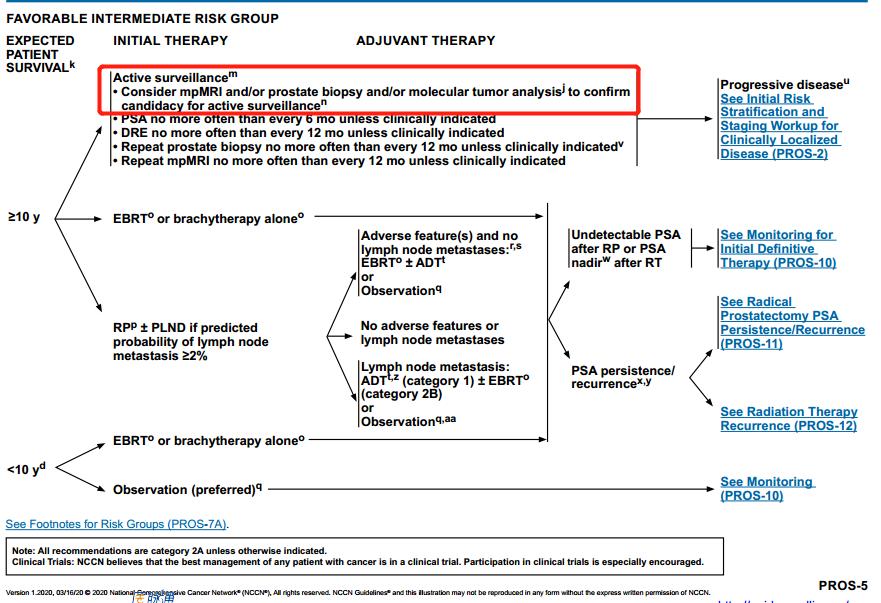
在低风险组中,对于预期寿命10年以上患者主动监测,修改为:推荐考虑mpMRI和/或前列腺活检和/或分子分析作为积极监测方法以确定合适患者。

在预后良好中等风险组中,对于预期寿命10年以上患者主动监测,修改为:推荐考虑mpMRI和/或前列腺活检和/或分子分析作为积极监测方法以确定合适患者。
预后不良中等风险组(PROS-6)
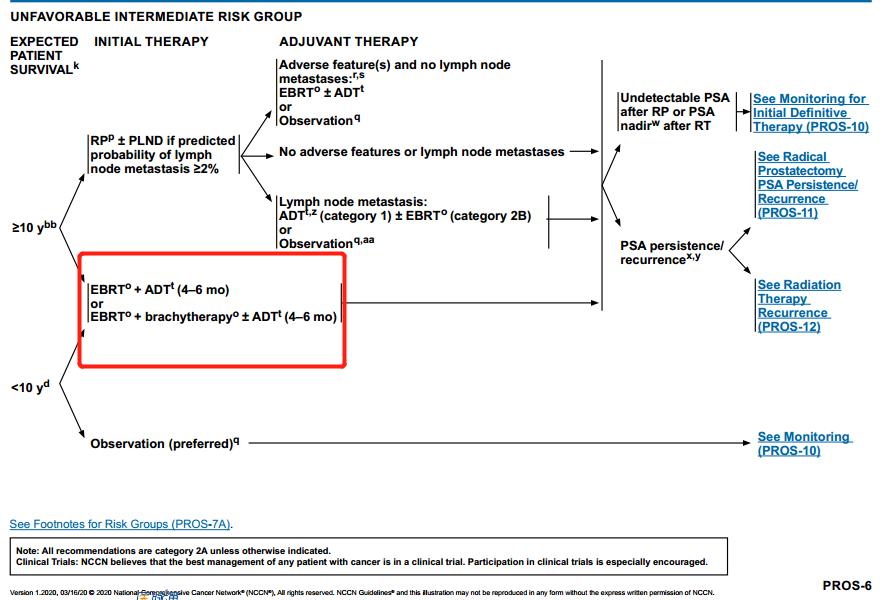
在预后不良中等风险组中,推荐初始治疗为EBRT±ADT(4个月)改为EBRT+ADT(4-6个月)。
在预后不良中等风险组中,EBRT+近距离放射治疗±ADT(4个月)改为EBRT+距离放射治疗±ADT(4-6个月)。
高风险组和极高风险组(PROS-7)
在高风险和极高风险组中,对于预期寿命5年以上或有症状患者,初治治疗可用EBRT+ADT(1.5-3年,1类)±多西他赛(1类,仅极高风险)。
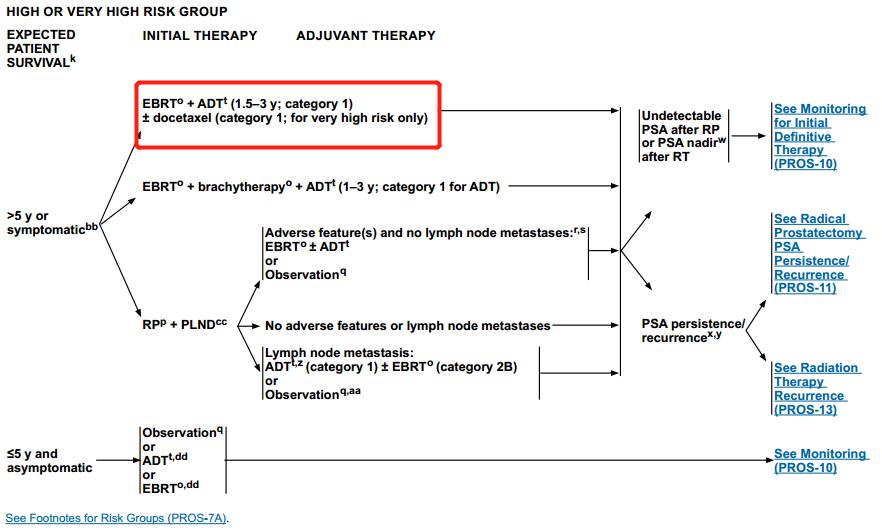
PROS-7A
增加以下脚注:
若RP后出现不良特征,推荐采用Decipher分子检测以指导辅助治疗。
不鼓励重复进行分子检测。
pN1分期患者选择观察时,若PSA不可检测,对于初始治疗后的监测应查阅PROS-10;对于pN1疾病和PSA持续的患者,请查阅PROS-11。
若发现更高级别和/或更高的T分期,查阅PROS-2。
对于N1期患者进行ADT的监测,查阅PROS-11
修改脚注:PSA最低点是指EBRT或近距离放射治疗后达到的最低值。

晚期前列腺癌的基因检测和分子标志物分析(PROS-8)
转移风险组的分子标志物分析改为:推荐进行HRRm检测,并考虑MSI或dMMR检测。

PROS-9,PROS-13,PROS-16
阐明了阿比特龙的不同剂型:“阿比特龙”和“小颗粒(Fine-particle)阿比特龙 ”

监测、复发(PROS-10)
改为:N1进行ADT治疗或观察时,应进行体格检查+每3-6个月进行PSA检测
增加:有症状或PSA升高患者进行影像学检查
删除:有症状患者每6-12个月进行骨影像学检查
修改脚注为:若ADT后进展应记录去势术后睾酮水平,进展后的检查应包括骨成像、胸部CT、腹部/盆腔CT或腹部/盆腔MRI,若无转移证据,考虑11C-胆碱PET / CT或PET/MRI或F-18 fluciclovine PET/CT或PET/MRI对软组织和骨进行进一步检测,或18 F-氟化钠PET/CT或PET/MRI对骨进行进一步检测。

根治性前列腺切除术后PSA持续/复发(PROS-11)
删除:“未使用去势治疗(castration-naive)”用于定义在疾病进展时不处于ADT的患者。NCCN前列腺癌指南使用术语“castration-naive”,即使患者已经接受过新辅助治疗,同步或辅助ADT作为放射治疗的一部分,只要他们已经恢复*丸睾**功能。

放射治疗复发(PROS-12)
改为:高强度聚焦超声改为“2B类”
替换:“ADT(尤其骨扫描阳性时)或观察”见PROS-13

未经去势前列腺癌的系统治疗(PROS-13)
在未经去势前列腺癌中,M1期患者使用ADT联合以下优选方案:阿帕鲁胺(1类);阿比特龙(1类);多西他赛(75mg/m2/6周期,1类);恩杂鲁胺(1类);其他方案:小颗粒阿比特龙 (2B类)。
将“每6-12个月对有症状患者进行骨成像”替换为“有症状或PSA升高进行影像学检查”。
增加脚注:建议进行MSI-H或dMMR检测和胚系同源重组突变检测(见PROS-B);正在观察的 M0分期患者应接受适当的治疗方案(对于非去势疾病)。

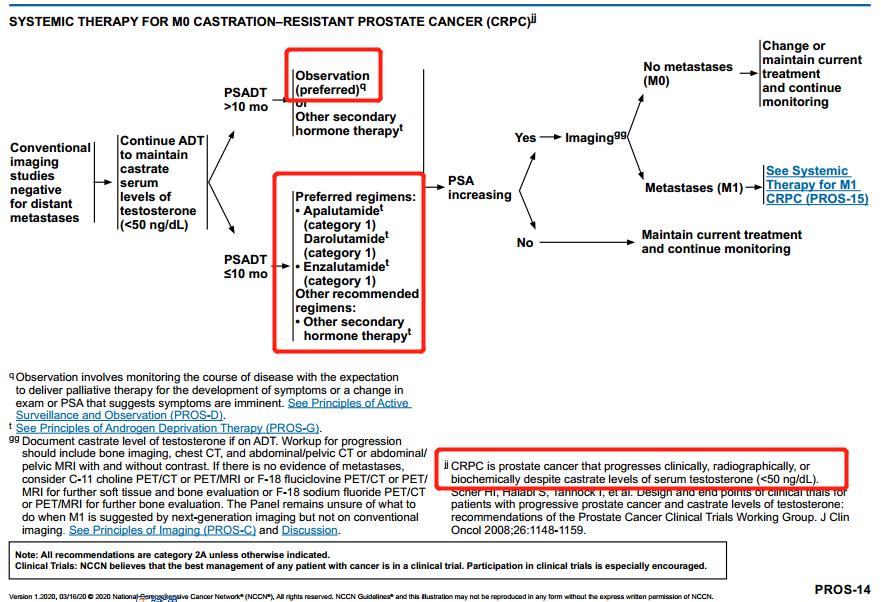
M0期去势抵抗性前列腺癌(CRPC)的系统治疗(PROS-14)
PSA>10个月,增加“观察(优选)”
PSA≤10个月,优选方案:阿帕鲁胺(1类),Darolutamide(1类),恩杂鲁胺(1类);其他推荐方案:其他二线激素治疗
增加脚注:尽管血清睾酮水平<50ng/dL,CRPC可能会发生临床进展、影像学进展或生化进展(参考文献略)。
M1期CRPC的系统治疗(PROS-15)
对于传统影像学检查阳性的转移性CRPC,推荐之一改为:“转移灶活检”。
对于传统影像学检查阳性的转移性CRPC,推荐之一改为:“若之前未进行,推荐MSI-H或dMMR检测”。
对于传统影像学检查阳性的转移性CRPC,推荐之一改为:“若之前未进行,推荐胚系同源重组基因检测”。
删除:其他方案:免疫治疗联合sipuleucel-T(1类)(见PROS-G)。
删除:“内脏转移”和“无内脏转移”。
小细胞前列腺癌/神经内分泌前列腺癌的一线和后续治疗化疗方案:增加“阿替利珠单抗/卡铂/依托泊苷(3类)”。
修改脚注:其他后续方案,查阅“NCCN Guidelines for Small Cell Lung Cancer”。

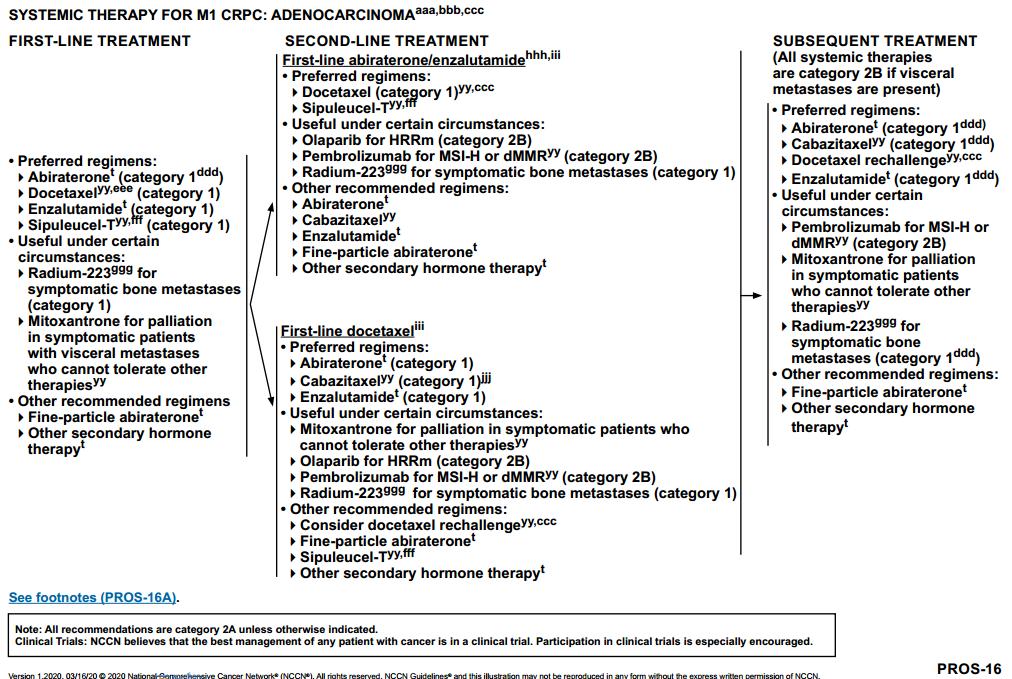
M1期CRPC的系统治疗:腺癌(PROS-16)
由2019版V4“M1 CRPC系统治疗:无内脏转移腺癌”和“M1 CRPC系统治疗:有内脏转移腺癌”合并而来。
一线治疗:优选方案:阿比特龙(1类),多西他赛(1类),恩杂鲁胺(1类),sipuleucel-T(1类);特定情况下的治疗方案:镭-223(骨转移症状)(1类);米托蒽醌用于不能耐受其他治疗的有内脏转移症状的姑息治疗(2A类);其他推荐:Fine-particle 阿比特龙(2A类)、其他二线激素治疗(2A类)。
二线治疗(一线阿比特龙/恩杂鲁胺):优选方案:多西他赛(1类),sipuleucel-T;特定情况下的治疗方案:奥拉帕利(HRRm)(2B类),帕博利珠单抗(MSI-H或dMMR)(2B类),镭-223(骨转移症状)(1类);其他推荐:阿比特龙(2A类),卡巴他赛(2A类),恩杂鲁胺(2A类),fine-particle阿比特龙(2A类),其他二线激素治疗(2A类)。
删除:最佳支持治疗。
二线治疗(一线多西他赛):优选方案:阿比特龙(1类),卡巴他赛(1类),恩杂鲁胺(1类);特定情况下的治疗方案:米托蒽醌用于不能耐受其他治疗的有内脏转移症状的姑息治疗(2A类),奥拉帕利(HHRm)(2B类),帕博利珠单抗(MSI-H或dMMR)(2B类),镭-223(骨转移症状)(1类);其他推荐:考虑多西他赛重新治疗(2A类),fine-particle阿比特龙(2A类),sipuleucel-T(2A类),其他二线激素治疗(2A类)。
删除:最佳支持治疗。
后续治疗:优选方案:阿比特龙(1类),卡巴他赛(1类),多西他赛(1类),恩杂鲁胺(1类);特定情况下的治疗方案:帕博利珠单抗(MSI-H或dMMR)(2B类),米托蒽醌用于不能耐受其他治疗的有内脏转移症状的姑息治疗(2A类),镭-223(骨转移症状)(1类);其他推荐:fine-particle阿比特龙(2B类),其他二线激素治疗(2B类)。
删除:最佳支持治疗。
参考文献:
NCCN Guidelines Version 1.2020 Prostate Cancer
