前言
1990年,被称为“基因治疗之父”的美国医学家William French Anderson领衔进行了一项长期临床实验,他们对一名患有腺苷脱氨酶缺乏症(ADA缺乏症)的4岁女孩进行了基因治疗。女孩由于基因存在缺陷,自身不能合成ADA,免疫功能低下,只能生活在无菌的隔离仓中。他们利用逆转录病毒将ADA基因转移到分离的T细胞中,然后将这些改造后的T细胞回输⾄患者体内,经过一段时间的治疗后,女孩的免疫功能日趋健全,最终过上了正常的生活。这是世界上第一个基因治疗成功的范例,该案例也成为了基因治疗发展史上一个重要的里程碑,自此之后全世界陆续开展各种基因治疗的临床实验。在本篇,小编将带领大家了解基因治疗和细胞治疗的区别、基因治疗相关载体及基因治疗的研究进展等内容。
基因治疗和细胞治疗的区别
细胞是所有生物的基本组成部分,基因是具有遗传效应的DN*片A**段,基因支持着生命的基本构造和性能,如图1所示。细胞治疗和基因治疗并不容易划分清楚,为了更好的对其进行概括,业界普遍的做法是将细胞治疗和基因治疗合并在一起,统称为细胞基因治疗。
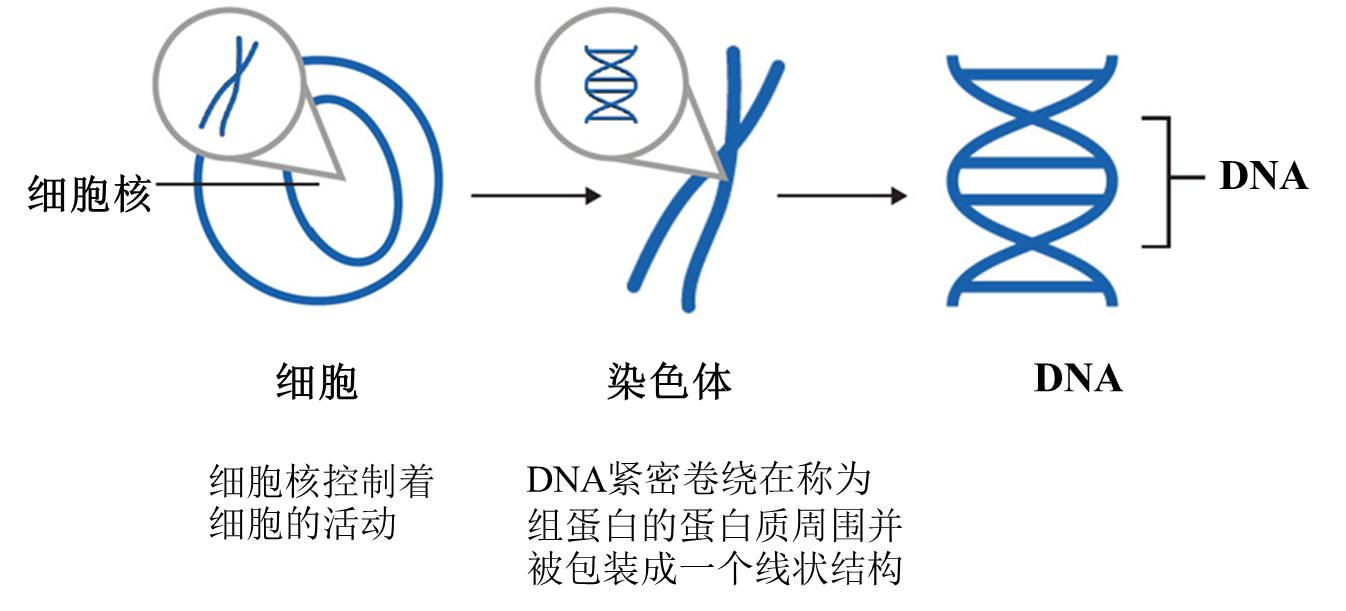
图1|DNA和细胞的关系
细胞治疗通常是指利用某些具有特定功能的细胞的特性,采用生物工程方法获取或通过体外扩增、特殊培养等处理后,使这些细胞具有增强免疫、杀死病原体和肿瘤细胞、促进组织器官再生和机体康复等治疗功效,从而达到治疗疾病的目的。近些年,细胞治疗在癌症、糖尿病、遗传病等疾病的治疗上显示了越来越高的应用价值。
基因治疗指的是通过替换、使基因失活或将基因引入细胞来治疗疾病,可以是体内的细胞,也可以是体外的细胞。目前,随着基因治疗领域的不断发展,已经逐渐形成了多个细分领域。从基因层面可以分为基于DNA的基因治疗和基于RNA的基因治疗。基于mRNA开发的生物制剂在最近几年逐渐受到大家的广泛关注,一方面用于治疗病毒的RNA疫苗,另一方面用于遗传病、肿瘤等疾病的治疗。
一般来说,细胞治疗和基因治疗按照技术类别进行区分会更容易些,如图2所示。
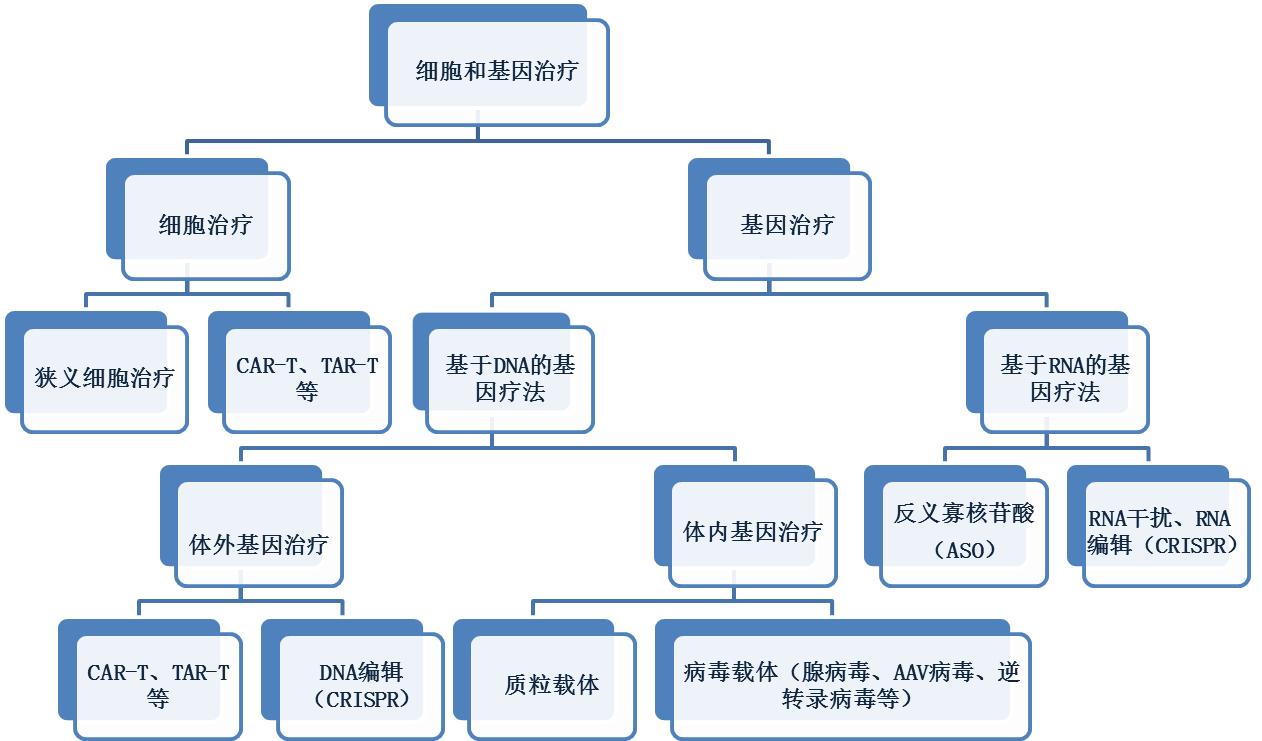
图2|基因疗法和细胞疗法分类
基因治疗产品分类
FDA将基因治疗产品按照技术方式分为五类,分别是质粒DNA基因治疗产品、病毒载体基因治疗产品、细菌载体基因治疗产品、基因编辑治疗产品和细胞基因治疗产品。
- 质粒DNA:指的是通过基因工程可以将携带治疗性基因的环状DNA分子进入人类细胞。
- 病毒载体:指的是对病毒进行改造去除其引起传染病的能力 这些修改后的病毒就可以作为载体,将治疗性基因携带到人类细胞中。
- 细菌载体:是指通过对细菌(如沙门氏菌)进行改造,使其不引起传染病,然后将其作为载体,携带治疗性基因进入人体组织。
- 基因编辑产品:指的是能够精确对生物体基因组的特定目标基因进行修饰,从而达到破坏有害基因或者修复变异基因的目的。
- 细胞基因治疗产品:是指从患者体内提取细胞,经过基因改造(通常使用病毒载体),然后返回患者体内。
基因治疗相关载体
基因治疗,准确的说就是将基因递送到靶细胞上,基因递送的方式和效率直接决定了药物的治疗效果,所以基因治疗载体的选择显得尤为重要。理想的基因治疗载体需要具备靶向特异性、无毒性、高稳定、易制备等多种特性。目前常用的基因递送系统主要包括病毒载体和非病毒载体。非病毒载体主要是裸露的DNA、质粒、脂质体等其他物质,该类载体具有低成本、易规模化和低免疫原性等多种优点,但是存在转染效率低、细胞毒性等问题。病毒载体包括腺相关病毒、慢病毒、腺病毒和逆转录病毒等。自1998年以来,已有22种基因治疗药物被批准用于人类疾病的治疗,包括裸核酸、非病毒载体、病毒载体和细胞介导的基因治疗产品,如图3所示。尽管病毒载体相较于非病毒载体可传递基因容量较小,但病毒载体的高传递效率使其在未来的研究中应用更为广泛。目前大多数的细胞和基因治疗项目所采用的载体都是病毒载体,相较于腺病毒和逆转录病毒来说,腺相关病毒(AAV)载体安全性较好,所占临床试验的⽐例近年来也在逐步增加。接下来简要介绍一下AAV的递送机制以及在基因治疗的产品生产中所面临的一些挑战和应对策略。
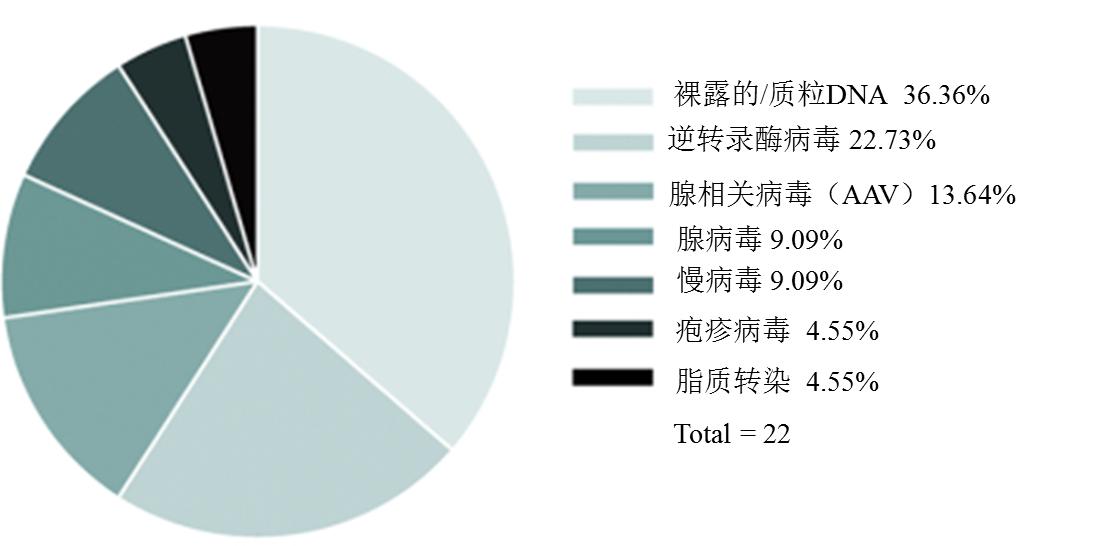
图3|1998-2019年间批准的基因治疗药物所用载体的情况概览(来源:Biotechnol Adv)
AAV是⼀种单链DNA病毒,外形为正⼆⼗⾯体,由蛋⽩⾐壳和长度为4.7kb的单链DNA基因组构成。目前已经发现12种AAV血清型和100多种AAV突变型,不同的AAV具有不同的衣壳蛋白,从而导致其对组织或细胞的转染效率有所不同。AAV的递送机制:首先,AAV颗粒与靶细胞表⾯的糖化受体结合后,通过⽹格蛋⽩介导的内吞作⽤进⼊细胞;其次,在内吞形成的内涵体酸化之后,病毒⾐壳构象发⽣变化,使得病毒可从内涵体脱离,并通过核孔进⼊细胞核,或经泛素化途径被降解;最后,进⼊细胞核的AAV颗粒释放⽬标基因,⽬标基因在核内聚合酶的作⽤下形成完整双链,转录、翻译可得治疗性蛋白质,如图4所示。AAV的外源基因的携载量一般不能超过4.7Kb,对于很多大片段基因的导入,需要对其非功能区进行截短,或者大片段基因分成两半后各有一个AAV携带。据统计40-80%的人体内含有针对AAV的抗体,导致AAV作为基因治疗传递药物的载体直接被免疫系统摧毁,降低了转基因的表达效率。目前,科学家们从理性设计、定向进化、联合方式和计算机辅助设计这4个维度对AAV的衣壳蛋白进行修饰,以提高AAV的递送效率和逃避免疫反应的能力,如图5所示。
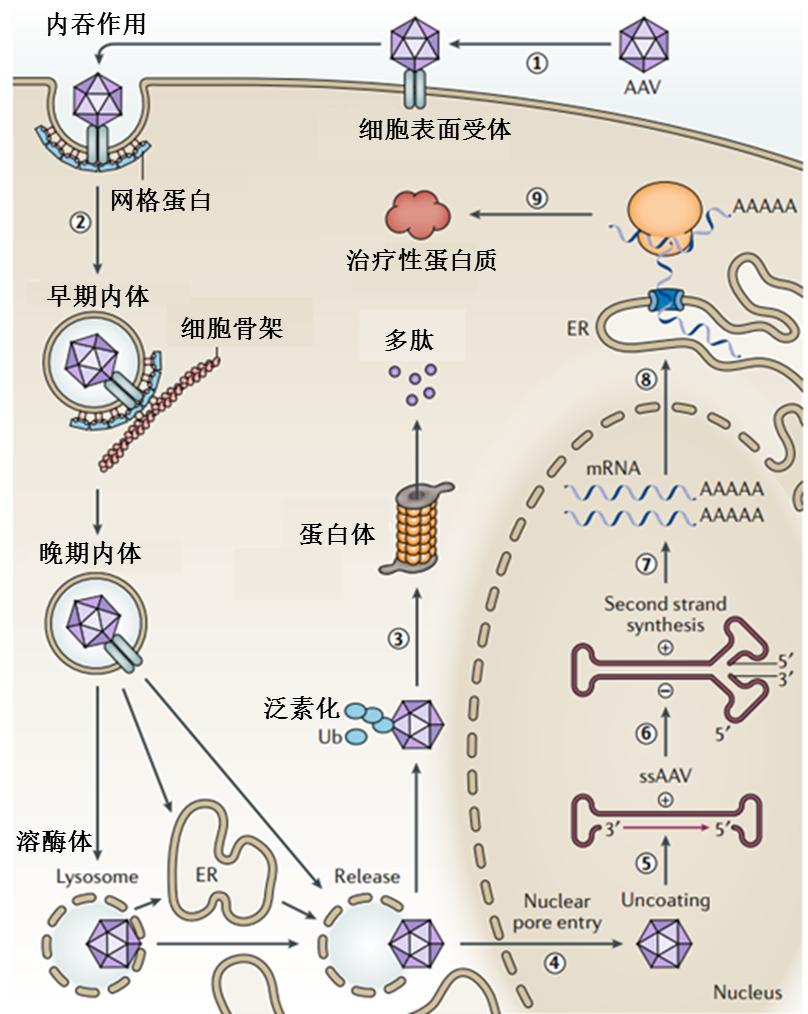
图4|AAV的递送机制(来源:Nat Rev Genet)
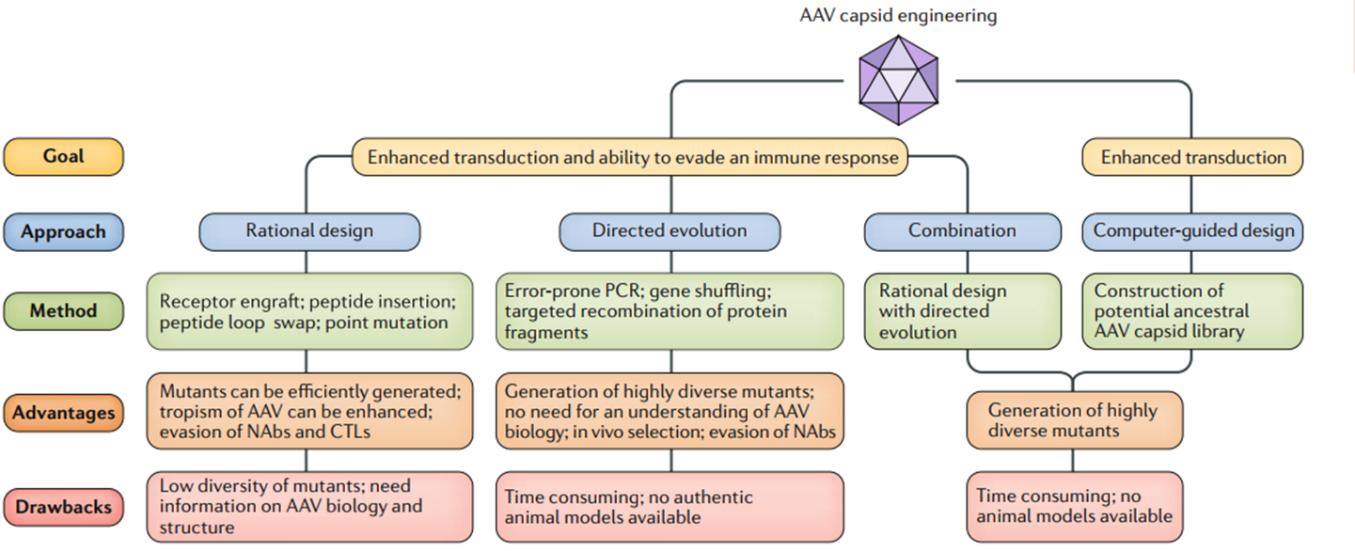
图5|AAV 衣壳蛋白的修饰(来源:Nat Rev Genet)
基因治疗的研究进展
经历了几十年的螺旋式发展,基因治疗至今已经在治疗获得性疾病和遗传病上取得了令人激动的临床实验进展,截止到2019年9月,已有20多种基因治疗药物上市。这些基因治疗产品类型涵盖了寡核苷酸类、溶瘤病毒、CAR-T疗法、干细胞疗法以及其他基于细胞的基因疗法。从1998年Vitravene获批上市开始,到2019年5月24日Zolgensma获批上市,可以看出基因治疗正在朝着一个光明的方向蓬勃发展,目前已经有越来越多的基因治疗产品上市。
基因编辑技术自问世至今,已有30年的历史。自从CRISPR横空出世,基因编辑技术愈发成熟。然而目的基因的递送技术发展滞后,基于CRISPR技术的基因编辑治疗的临床应用困难重重,科学家们一直在努力探索递送技术的突破。令人惊喜的是,Nature Biomedical Engineering和Nature Biotechnology杂志分别于近日发表了递送CRISPR/Cas9 mRNA的最新技术。该技术是一种介于病毒载体与非病毒载体之间的类病毒体(VLP)技术,是由上海交通大学的蔡宇伽教授团队和复旦大学附属医院洪佳旭团队合作开发的全球首创的基因治疗递送载体技术。技术人员利用mRNA茎环结构与噬菌体衣壳蛋白特异识别的原理,通过病毒工程技术,将两者的优点完美的结合起来,创造了新型递送技术VLP-mRNA。VLP技术利用病毒的外壳提高了感染细胞的效率,基于mRNA自身瞬时性的特点提高了安全性。通过VLP技术递送CRISPR/Cas9 mRNA,该技术在老年黄斑变性等眼科疾病的治疗领域展现了巨大的潜力。


总结和展望
回顾基因治疗过去几十年的发展历程,在基因治疗发展初期,外源基因如何导入细胞中是一个重大的挑战,直到病毒载体的出现,这一问题才得到解决。然而,1999年,患有鸟氨酸转氨甲酰酶缺陷(OTC)的Jesse Gelsinger参与了基因治疗临床实验,接种4天后,死于免疫反应导致的多器官衰竭。接下来,FDA陆续暂停了多项基因治疗临床实验。自此,基因治疗领域迎来了黑暗时刻。直到2012年,欧盟药物管理机构批准了基因治疗产品Glybera,这是世界上第一款治疗遗传病的基因治疗产品,此后多款基因治疗产品也陆续获批上市,自此基因治疗领域迎来了高光时刻。
基因治疗的发展与进步为许多疾病的治疗提供了新的思路,基因编辑技术的兴起让基因治疗领域再一次迈进了全新起点。然而,目前的基因治疗仍旧存在诸多挑战,其中包括提高基因递送效率,预防基因编辑脱靶引起的细胞毒性,避免载体或者基因编辑产物引起的体内免疫反应等。基因治疗能否取得突破很大程度上取决于基础科学的发展,可以从基因编辑工具的升级改造、病毒载体的优化以及靶向基因组整合策略等方面进行深入研究,从而推动基因治疗领域的发展。尽管基因治疗研究还存在以上诸多待解决的技术难题以及一些法律或伦理等方面的问题,但这并不妨碍人们对其治愈重大疾病寄予厚望,相信在不久的将来,基因治疗会成为人类战胜疾病极其重要的帮手。
参考文献
Ma Cui-Cui, Wang Zhen-Ling, Xu Ting et al. The approved gene therapy drugs worldwide: from 1998 to 2019.[J] .Biotechnol Adv, 2020, 40: 107502.
Li Chengwen, Samulski R Jude, Engineering adeno-associated virus vectors for gene therapy.[J] .Nat Rev Genet, 2020, 21: 255-272.
Shahryari Alireza, Saghaeian Jazi Marie, Mohammadi Saeed et al. Development and Clinical Translation of Approved Gene Therapy Products for Genetic Disorders.[J] .Front Genet, 2019, 10: 868.
Yin Di, Ling Sikai, Wang Dawei et al. Targeting herpes simplex virus with CRISPR-Cas9 cures herpetic stromal keratitis in mice.[J] .Nat Biotechnol, 2021.
Ling Sikai et al. Lentiviral delivery of co-packaged Cas9 mRNA and a Vegfa-targeting guide RNA prevents wet age-related macular degeneration in mice.[J]. Nature Biomedical Engineering, 2021.