“桃之夭夭,灼灼其华。”
疫 散 花 开
3月初,奉化的桃花开满了枝头。。。

桃花盛开
在桃花盛开的季节,宁波市奉化区人民医院医共体、宁波市奉化区肿瘤防治临床指导中心、罗氏制药于2021年3月12日下午召开了“妥妥愈她学术交流会:奉化锦山论坛--乳腺癌多学科论坛”,来自宁波一院、宁波大学附属医院、宁波病理中心、奉化区人民医院、奉化区中医院的乳腺癌MDT团队及宁波市奉化区人民医院医共体副高前医生、轮转医生、宁波大学实习医生共40余人参加会议。会议由奉化区人民医院医共体血液肿瘤科主任孙密芬副主任医师主持。

首先由宁波一院郭宇教授讲解《HER2阳性早期乳腺癌多临床决策点》,然后由宁波大学附属医院岑律军教授、奉化区人民医院林寒冰副主任医师、奉化区中医院王鸿主任医师分别介绍诊治过的进展期乳腺癌病例,参会的乳腺外科、肿瘤内科、病理科、放疗科、影像科、临床药师等专家充分沟通和讨论,共同为患者制定完善的治疗方案。

宁波一院郭宇教授讲解《HER2阳性早期乳腺癌多临床决策点》
、

宁波大学附属医院岑律军教授

奉化区人民医院林寒冰副主任医师

奉化区中医院王鸿主任医师
MDT的全称是多学科团队,是指临床上多个学科针对一个临床疾病或者一个患者,重点商讨诊疗中的问题,通过多学科的讨论会议,对患者病情做出综合评估,共同制定科学、合理、规范的治疗方案。这是目前医学行业最新的诊疗模式。
乳腺癌发病率越来越高,已成为中国女性最常见的恶性肿瘤。多学科诊疗(MDT)是提升乳腺癌诊治水平的重要模式,通过MDT制定规范的诊治将惠泽更多的乳腺癌患者。
宁波市奉化区人民医院医共体副院长、 宁波市奉化区肿瘤防治临床指导中心主任王晓亮主任医师介绍了奉化区人民医院的MDT历程,并强调今天的MDT讨论会更是一个MDT教学会,让副高前医生、轮转医生、实习医生了解到多学科专家在MDT平台上如何开展诊治讨论、在探讨中开拓思维、在交流中借鉴经验,共同提高专病的综合治疗水平,希望我们的年青医务工作者通过下午的MDT教学能学习掌握这种循证的、相互协作的、共同提高的临床思维拓展模式,为以后顺利开展临床工作打下诊治思维基础。


共识/指南
中国进展期乳腺癌共识指南
2020(CABC3)
前言
目前乳腺癌相关指南日益完善,本指南集合了乳腺癌领域知名专家多年学习和丰富的临床经 验,在 2015 年发表的《中国进展期乳腺癌共识指南 (CABC 2015)》的基础上[1],从 2016 年 5 月到 2020 年7月,由中国女医师协会乳腺疾病研究中心和北 京大学肿瘤医院共同在北京召开的复发转移乳腺 癌年度专题讨论会上形成和完善,是国内外专家 的集体智慧结晶。
内容提要
本指南主要针对进展期乳腺癌的诊疗进行详 细论述,包括对疾病的认识和治疗理念,多学科诊 疗团队治疗进展期乳腺癌的基本原则,新药的临 床应用效果和不良反应的管理,相关重要概念的 定义,进展期乳腺癌患者的急症,以及检查与评估 的频率。同时针对不同分子亚型的药物治疗进行 了详尽阐述,并完善了特殊转移部位的肿瘤的治 疗原则。尤其对临床中几个重点问题做了详细的 描述:①鼓励患者参加临床研究,近年来更多针对 分子靶点的新药进入临床,为患者提供了更多的 治疗机会,临床研究亦可成为患者最佳的治疗选 择;②激素受体阳性乳腺癌的内分泌治疗联合周 期蛋白依赖性激酶(cyclin-dependent kinase,CDK) 4/6*制剂抑**治疗;③HER2阳性乳腺癌靶向治疗的联 合和序贯;④三阴性乳腺癌的治疗进展;⑤分子检 测对于治疗进展期乳腺癌的意义;⑥欧美国家已 经上市,但国内尚未批准乳腺癌适应证或国内尚 未上市的新药的合理使用;⑦不良反应的管理;⑧ 鼓励患者参与治疗决策的制定;⑨开展患者教育 活动的意义。同时本指南还补充添加了更多来自 中国的数据,使其更适合中国的医生和患者。
中国进展期乳腺癌共识指南
(CABC 2020)
Chinese Consensus Guidelines for Advanced Breast Cancer 2020 (CABC2020)
既往研究认为进展期乳腺癌不能治愈,但可以 治疗,随着新药的不断涌现,尤其是针对不同分子 靶点的靶向治疗药物,有望延长进展期乳腺癌患 者的生存时间,甚至提高5~10年的治愈率。因此, 对于进展期乳腺癌的治疗,在延缓疾病进展、改善 患者生活质量、延长患者生存时间的基础上,合理 优选治疗方法十分重要。进展期乳腺癌没有绝对 的标准治疗方案,但也有规律可循。进展期乳腺 癌的诊疗和管理相对复杂,需从多方面考虑,包括 疾病层面,例如患者辅助治疗后的无病生存时间、 既往治疗药物及其疗效、分子类型、肿瘤负荷以及 是否有需要快速控制的疾病症状和体征;同时还 需要考虑患者层面,例如患者的意愿、年龄、月经 状态、是否有其他慢性病、经济状况、社会和家庭 的支持以及患者的心理因素等。
1 进展期乳腺癌诊疗的一般原则
1.1 多学科专家团队
进展期乳腺癌的治疗团队需要整合内科、外 科、放疗科、影像科、病理科、心理医生、社会工作 者、护士和姑息治疗专家等多学科的专业人员。肿 瘤专科护士或医生助理也应加入这一团队[13-14]。建 议该团队应使具有学术研究兴趣的成员尽可能涵 盖实验室、转化和临床试验研究,后者尤其为患者 提供了早期获得新药和治疗方案的机会。
1.2 鼓励患者参与治疗决策
在中国,多数患者不参与治疗决策过程,治 疗 决策多由患者家属参与并做出选择。由于进展期 乳腺癌的治疗是一个长期的过程,患者的依从性 可影响治疗效果,所以专家组建议患者应积极参 与治疗方案的制定,并确保患者对治疗决策有充 分的知情权。通常一旦被确诊为乳腺癌,患者需 要大量的信息,包括如何治疗疾病、家庭的经济负 担及对疾病的感受和承受能力。一方面,中国的 大多数家庭选择对患者隐瞒病情,他们担心疾病 对患者的打击,甚至希望医生开具一张隐瞒病情 的诊断书,不告诉患者自身疾病的恶性程度;另一 方面,如果患者没有医疗保险,其诊治费用主要由 子女承担,患者不希望给家庭带来负担,从而选择 不告诉家属自己的病情,而这两种做法都是不恰 当的。因此,专家组鼓励患者及其家属共同参与 治疗决策,并且由患者起主导作用。在可能的情 况下,应鼓励患者由支持他们的人(如家庭成员、 护理人员、支持群体)陪伴,被邀请参与制定治疗 决策。
1.3 进展期乳腺癌有望治愈
经全面评估和确诊为进展期乳腺癌后,相关人 员应对治疗的目的进行讨论,并告知患者,进展期 乳腺癌患者可以有较长的生存时间,应该使用易 懂的语言进行谈话,尊重患者的隐私和文化差异, 并尽可能地提供书面信息。
1.4 特殊治疗药物的选择策略
帕妥珠单抗[15]、依维莫司[16]、CDK4/6*制剂抑**[17]、 多腺苷二磷酸核糖聚合酶*制剂抑**[poly(ADP- ribose)polymerase inhibitor,PARPi]、Alpelisib[一种磷 脂酰肌醇-3-羟激酶(phosphatidylinositol 3-hydroxy kinase,PI3K)*制剂抑**][18]、西达本胺、T-DM1 等都已 经获得美国食品药品管理局(Food and Drug Administration,FDA)的批准,并已上市应用于乳腺癌 的治疗,其中帕妥珠单抗、依维莫司、CDK4/6 抑制 剂和 T-DM1[19] 也在中国获批上市。PARPi 在中国 先被批准用于治疗卵巢癌[20],目前已被批准用于治 疗 乳 腺 癌 易 感 基 因(breast cancer susceptibility gene,BRCA)1/2 突变的乳腺癌[21-22];西达本胺在中 国被批准用于 HER2 阴性、绝经后、经内分泌治疗 复发或进展的局部晚期或转移性乳腺癌患者[23];Alpelisib 在国外被批准用于治疗乳腺癌,在中国并 未获得批准,但仍是乳腺癌可选择的治疗药物,其在 中国的应用需谨慎考虑。自CABC2发表后,已经有 很多新的药物被报道改进了乳腺癌患者的生存情 况,包括氟维司群[24-25]、帕妥珠单抗、CDK4/6*制剂抑**。
1.5 治疗相关不良反应的管理
对治疗相关不良反应进行客观可靠的评价,是 进展期乳腺癌患者生活质量管理的重要部分。每 个患者对治疗不良反应的耐受性均存在差异。 医 生应该使用标准的、经验证的工具或患者自我评 价量表(patients reported outcomes,PRO)来评估药 物的安全性,通常使用不良反应常用术语标准 (common terminology criteria for adverse event, CTC-AE)对不良反应的类型和严重程度进行评价 (http://outcomes.cancer.gov/tools/pro- ctcae.html)[4], 这样可以更准确地反映患者的治疗获益和治疗危 害。同时,专家组推荐采用癌症治疗的功能评估 (functional assessment of cancer therapy,FACT)量 表评价乳腺癌患者的生活质量。还可通过建立公 众号,定期推送药物相关不良反应的知识,并通过 患者教育课堂传递相关知识。
1.6 生活质量
从诊断为进展期乳腺癌开始,在医护的日常工 作中患者应接受适当的心理疏导、支持护理和相 关症状的干预。医生必须施以个性化的干预方 法,以满足患者的个体需要。
1.7 治疗成本和医疗资源配备
医学界应了解进展期乳腺癌治疗成本的问题, 应在平衡患者获益、生存时间和患者意愿等所有 情况下做出决定。
1.8 鼓励患者加入临床研究
在进展期乳腺癌的治疗中,目前越来越多的新 药可使患者获益,有些患者甚至可以长期生存。但是新药费用昂贵,且新药在国内获批的时间较 长,而新药临床试验可为患者提供另一个选择。如果患者有意愿参与,在经过患者知情并同意后, 将患者纳入精心设计的、前瞻性、随机对照的临床 试验也是一个优先选择的治疗方案。
1.9 患者教育的重要性
患者教育可以提高治疗依从性,可能会改善预 后;同时可改善患者的生活质量,延长患者的生存 时间。
1.10 提倡线上医疗
随着网络的广泛覆盖和人们对线上医疗的逐 步认可,尤其受新冠肺炎疫情的影响,线上医疗将 成为患者获得治疗建议的重要方式,尤其是成为 患者了解病情、治疗效果监测、不良反应管理、随 访期康复等过程的便捷优化形式。
2 进展期乳腺癌相关的重要定义
乳腺癌的治疗在国内外并不统一,尤其是进展 期乳腺癌,包括治疗方法以及治疗科室均不统 一。鉴于乳腺外科、乳腺内科、肿瘤内科或普外科 均可治疗乳腺癌且该病治疗的复杂性,本文对进 展期乳腺癌治疗相关的几个重要定义进行了阐 述。明确重要定义不仅对临床研究具有指导意义,而且在临床实践中也发挥重要作用,可协助医 生尽量避免对耐药的患者重复治疗,使患者从治 疗中得到最大获益。
2.1 内脏危象
内脏危象的定义:不仅有内脏转移,疾病进展 迅速,而且可通过症状和体征、实验室检查结果评 估器官功能障碍的严重程度。在这种情况下,内 脏转移的病情需要得到快速缓解,因此需要给予 有效且能快速缓解疾病的治疗方法。虽然指南中 推荐应用有效的治疗方法(如化疗)来改善疾病状 况,但临床中存在严重器官功能障碍的患者可能 不适合化疗,因此,医生需谨慎处理。
2.2 内分泌治疗耐药
2.2.1 原发性内分泌治疗耐药
指术后辅助内分 泌治疗2年内出现复发转移,或转移性乳腺癌一线 内分泌治疗6个月内出现疾病进展。
2.2.2 继发性内分泌治疗耐药
术后辅助内分泌 治疗过程中,治疗≥2年后出现复发转移,辅助内分 泌治疗结束后 12 个月内出现复发转移,或转移性 乳腺癌一线内分泌治疗≥6个月后出现疾病进展。明确这些定义后,在治疗患者的过程中,如果 患者出现原发性内分泌治疗耐药,可以考虑联合 靶向治疗来逆转耐药。对不能选择靶向治疗的患 者(比如经济原因),也可以考虑选择化疗[10]。如果 联合靶向治疗或化疗均被认为是不合适的,则可 以采用进一步的单一内分泌治疗,但是在这种情况 下,患者的临床获益率很低(﹤20%)。这与患者对 先前的内分泌治疗表现出敏感性并随后发展为获 得性耐药的情况有所不同,后者采用进一步的单一 内分泌治疗的临床获益率很高(60%~70%)[26]。
2.3 HER2的检测
HER2 的规范化检测和阳性的判定应参照美 国临床肿瘤学会(American Society of Clinical Oncology,ASCO)/美国病理学会(College of American Pathologists,CAP)指南或中国相关的指南。一 般是指:①免疫组化(immunohistochemistry,IHC) 3+;②荧光原位杂交(fluorescence in situ hybridization,FISH)或显色原位杂交(chromogenic in situ hybridization,CISH)显示 HER2/CEP17 比值≥2.0;③HER2 基因拷贝数≥6 个信号/细胞。目前还有一 些新的方法可用于检测 HER2 状态,尤其对于复发 转移乳腺癌,可采用液体活检技术进行检测,如循 环肿瘤细胞(circulating tumor cell,CTC)检测、循环 肿瘤 DNA(circulating tumor DNA,ctDNA)检测[27]、 微小RNA(microRNA)检测等[28]。
2.4 HER2阳性乳腺癌曲妥珠单抗耐药
是否和内分泌治疗一样,抗 HER2 的曲妥珠单 抗治疗也存在耐药?临床实践中的确存在一些患 者接受曲妥珠单抗治疗没有效果。
2.4.1 原发性曲妥珠单抗耐药
是指转移性乳腺 癌经曲妥珠单抗治疗 8~12 周内出现疾病进展,或 第1次影像学疗效评价即出现疾病进展;早期乳腺 癌术后辅助曲妥珠单抗治疗过程中出现复发转 移;或曲妥珠单抗治疗结束后 12 个月内出现复发 转移。
2.4.2 继发性曲妥珠单抗耐药
是指转移性乳腺 癌行曲妥珠单抗治疗,首次进行疗效评价有效,在 后续治疗过程中出现疾病进展[29]。虽然曲妥珠单抗耐药的定义还需要进一步的 循证证据支持,但这些概念可能会有助于医生的 治疗决策。临床回顾性研究发现,对于曲妥珠单 抗一线治疗反应时间较短的患者,仅换化疗并不 能带来更多获益。而对于曲妥珠单抗一线治疗失 败的患者,可以换用小分子酪氨酸激酶*制剂抑**或 者 T-DM1。随着抗 HER2 靶向治疗药物的增加,新 的抗HER2靶向治疗药物可能成为优选[30]。2.5 进展期乳腺癌相关急症 此类急症指有症状的脑转移、骨转移患者出现 脊髓压迫、上腔静脉综合征、肿瘤破裂出血、化疗 后出现发热性粒细胞减少等,均需积极治疗。
3 检查与疗效评估
3.1 基线检查
专家组建议:在全身性治疗前进行最基本的分 期检查,包括病史、症状和体征、血液学检查、肝肾 功能、血清电解质(包括血钙)、肿瘤标志物(尤其 是影像学检查不能评估病灶时)、心电图、胸部计 算机体层成像(computed tomography,CT)、腹部 CT、骨扫描和美国东部肿瘤协作组(Eastern Cooperative Oncology Group,ECOG)评分。值得提出的 是,症状和体征依然是临床一线医生的第一手资料, 绝不容忽略。虽然近年来影像学检查技术不断发 展,但影像学表现仍存在不典型性,容易导致误诊, 而症状体征可以帮助医生判断如何进行辅助检查。
3.2 病灶的活检
在开始治疗前,专家组建议进行肿瘤病灶的活 检,用于提供组织学检查和生物学指标的检查[包 括 ER、PR、雄激素受体(androgen receptor,AR)、 HER2 和 Ki-67]。在转移阶段,建议进行至少 1 次 生物学指标(尤其是 ER、PR、AR、HER2 和 Ki-67) 的再次评价[31-32]。
3.3 正电子发射断层显像-计算机体层成像的应用
正电子发射断层显像(positron emission tomography,PET)-计算机体层成像(computed tomography,CT)被用于明确转移病灶,但是基线检查时仍 需行 CT 或磁共振成像(magnetic resonance imaging,MRI)检查。针对无病生存时间短、早期复发而且多部位复发的患者,尤其是三阴性和HER2阳性 的患者,可以行PET-CT检查确定复发的病灶[33-34]。
3.4 头部影像学检查
对于无症状的患者,虽然头部影像学检查并非 常规检查,但在临床实践中部分无症状的患者在 常规复查时发现了脑转移。因此,临床医生应对 复发风险高(如激素受体阴性、HER2 阳性和三阴 性)的患者给予重视。针对无病生存时间较短、一 线治疗多部位复发者(尤其是三阴性和 HER2 阳性 乳腺癌患者),则可以考虑给予头部影像学检查, 以发现无症状的脑转移。
3.5 血清肿瘤标志物检查
血清肿瘤标志物通常检测癌胚抗原(carcinoembryonic antigen,CEA)、糖类抗原 153(carbohydrate antigen 153,CA153)和糖类抗原 125(carbohydrate antigen 125,CA125),这些指标增高可能是肿 瘤复发的早期表现,医生必须谨慎对待。如果是 已经转移的患者,治疗过程中肿瘤标志物增高需 考虑两种可能:其一,治疗无效,需结合影像学检 查来判断是否更改治疗方案;其二,肿瘤对治疗有 反应。因此,如果无可测量转移病灶的患者仅有肿 瘤标志物的增高,仅在极少数的情况下才是治疗有 反应的标志,故不应作为更改治疗方案的依据,但 其持续增高时应警惕肿瘤进展。对于具有可评估 病变的患者,应将肿瘤标志物作为评估治疗反应和 疾病进展的辅助手段。如果不能确定病情进展,则 通常不使用血清肿瘤标志物作为改变治疗方案的 依据,但医生应注意,肿瘤标志物水平增加尤其是 连续测量值持续上升可能标志着肿瘤进展,此时应 考虑进行随访评估。如上所述,如果影像学上没有 可测量或可评估的转移性病变(如硬化性骨转移、 腹膜疾病),则仅肿瘤标志物可用于指导病情评估 和改变治疗方案。有些研究报道了简单的标准(如 生化指标),当使用肿瘤标志物监测转移性疾病的 治疗反应时可以应用这些标准[35-38]。
3.6 骨扫描
骨扫描主要用于骨转移的筛查。明确骨转移 的诊断和随访评价必须进行CT或MRI检查。
3.7 新技术的应用
3.7.1 CTC 的检测
CTC 是指从肿瘤组织脱离并 进入血液循环系统的肿瘤细胞,这种细胞的产生 是患者发生远处转移的必要前提。目前关于 CTC 的检测国内还是以研究为主,尚未批准常规用于 临床,且需要重视检测方法的可靠性。研究表明, 全身治疗前以及治疗后首次随访检测的 CTC 数目 可作为转移性乳腺癌患者无进展生存时间和总生 存时间的独立预测指标[39]。2004 年,CellSearch CTC 检测系统被美国 FDA 批准用于评价转移性乳 腺癌的预后。一项多中心前瞻性研究证实,CTC 在 HER2 阳性或三阴性转移性乳腺癌中同样具有 重要的预后价值[40]。
3.7.2 ctDNA 的检测
ctDNA 是指原发或转移肿 瘤病灶通过凋亡、坏死或直接分泌等方式释放进 入外周血,并携带具有一定肿瘤生物学特征的肿 瘤基因组DN*片A**段。ctDNA检测具有一定的临床 意义[27],例如通过检测 BRCA 基因的状态决定是否 应用铂类或 PARPi[41],通过检测雌激素受体 1(estrogen receptor 1,ESR1)评估氟维司群和芳香化酶 *制剂抑**的选择[42],如果患者要接受选择性雌激素受 体下调剂(selective estrogen receptor down- regulator,SERD)——氟维司群,则不需要检测 ESR1,因 为氟维司群对野生型和 ESR1 突变的肿瘤均有效。在正在进行的口服 SERD 的临床前研究中报道了 类似的结果。当临床医生考虑使用非甾体类芳香 化酶*制剂抑**(如阿那曲唑、来曲唑)或甾体类芳香 化酶*制剂抑**(如依西美坦)时,通过 ctDNA 检测 ESR1可能有用[43]。通过检测磷脂酰肌醇-4,5-二磷 酸 3- 激 酶 催 化 亚 基 α(phosphatidylinositol- 4,5- bisphosphate 3- kinase catalytic subunit alpha;PIK3CA)判断是否适合 PIK3CA *制剂抑**治疗[44- 45]。肿瘤组织的基因检测有助于医生更加充分地了解 乳腺癌的亚型,它是对目前免疫组化分型的一个 补充,例如对于三阴性乳腺癌,如果采用基因检 测,可能会发现管腔雄激素受体(luminal androgen receptor,LAR)阳性,有利于医生制定其他的治疗 方案[46]。
3.7.3 程序性死亡受体配体 1 的检测
由于临床 研究中免疫治疗具有一定的治疗效果,尤其是对 程序性死亡受体配体 1(programmed cell death 1 ligand 1,PDCD1LG1,也称 PD-L1)阳性的乳腺癌患 者疗效更好,因此,检测 PD-L1 有助于进展期乳腺 癌的临床治疗。
3.8 疗效评价的频率
内分泌治疗通常为 2~4 个月评估一次,化疗通 常为 2~3 个月评估一次。随着患者治疗周期数的 增加,可以延长疗效评价的间期。多数患者仅接 受靶病灶的影像学检查即可。对于同一个靶病 灶,通常进行同一种方法检查,但是由于临床中需 要多次对同一个病灶进行评估,可以选择适当简 化的方法,例如肺转移的评估,可以间断选择 CT 平扫代替增强扫描。对于疾病进展缓慢的患者, 医生可以降低影像学检查的频率。总之,需要充 分考虑患者获益和承担的风险来进行各项检查。如果怀疑疾病进展或出现症状,无论是否到了计 划的检查时间,都应迅速给予检查。患者在每次 疗效评价检查时均要接受病史询问和体格检查。
4 进展期乳腺癌的基本治疗原则
4.1 治疗时应该考虑的因素
重点考虑激素受体和 HER2 状态,对于难治的 乳腺癌还可考虑 AR 和 PD-L1 状态以及 Ki-67 表达 水平;其他需要考虑的因素包括既往治疗及其不 良反应、无病生存时间或无进展生存时间、肿瘤负 荷(即转移的部位及数目)、年龄、体能状态、伴随 疾病和患者意愿,尤其需要考虑患者对化疗的接 受程度等人文关怀的理念。
4.2 转移灶的活检和病理
原发灶和转移灶生物标志物不一致时,应该根 据哪个生物标志物结果进行治疗决策目前尚不确 定。因为临床试验难以评价这种情况,所以专家 组推荐:在原发灶和转移灶中至少有一个病灶阳 性,就可依据这个阳性结果选择内分泌治疗和 (或)抗 HER2 治疗[31-32]。但也有专家认为,如果原 发灶和转移灶生物标志物不一致,对一线治疗的 决策而言,转移灶测得的生物标志物可能更重要。
4.3 液体活检
随着液体活检技术的不断改进,目前液体活检 越来越多地应用于临床。若患者的转移灶不宜做 穿刺活检,可以选择液体活检。
4.4 内分泌治疗选择时应考虑其是否绝经
虽然目前乳腺癌临床试验对绝经的定义各异, 但绝经通常是指月经永久性终止,也被用于描述乳 腺癌治疗过程中卵巢合成雌激素的持续性减少。关于绝经,NCCN 指南有几条明确的定义:
① 双侧卵巢切除术后;
②年龄≥60岁;
③年龄﹤60岁, 停经≥12个月,未接受化疗、他莫昔芬、托瑞米芬或 抑制卵巢功能的治疗,且卵泡刺激素(follicle-stimulating hormone,FSH)及雌二醇水平在绝经后的范 围内;
④年龄﹤60 岁,正在服用他莫昔芬或托瑞米 芬,FSH 及雌二醇水平应在绝经后范围内;
⑤正在 接受促黄体素释放激素(luteinizing hormone releasing hormone,LHRH)激动剂或拮抗剂治疗的患者, 无法判定其是否绝经;
⑥正在接受辅助化疗的绝 经前女性,停经不能作为判断绝经的依据,因为尽 管患者在化疗后会停止排卵或出现停经,但卵巢 功能仍可能正常或仍有恢复的可能。
对于化疗引 起停经的女性,如果考虑以芳香化酶*制剂抑**作为 内分泌治疗,则需要进行卵巢切除或连续多次监 测 FSH 和(或)雌二醇水平,以确保患者处于绝经 后状态[47]。化疗导致的闭经不是真正意义上的绝 经,芳香化酶*制剂抑**的应用也要慎重,尤其是对年 轻患者,因为年轻患者化疗后月经恢复的可能性 要高于年龄大的患者[48]。
4.5 患者的年龄不应影响有效治疗的实施
年龄通常不是影响治疗的决定因素。考虑到 年龄大的患者对化疗的耐受差,其治疗方案应以 内分泌治疗和单药化疗为主,但要避免老年患者 的治疗不足问题和年轻患者的治疗过度问题。年 轻患者被确诊为乳腺癌后,将会面临更加复杂的 情况,其治疗决策要考虑身体情况、器官功能、社 会、心理、精神、工作、家庭和儿童看护等因素。
4.6 需要考虑多种治疗模式
患者出现单发转移后,有可能获得完全缓解并 能长期生存,可以考虑接受多种模式的治疗。例 如单发的肝或肺转移,可以考虑给予患者手术切 除、放疗、介入治疗等。
4.7 初治的Ⅳ期乳腺癌
对于初治的Ⅳ期乳腺癌患者,切除原发性肿瘤 的价值还不确定。但在全身治疗有效的前提下, 如果乳腺局部病灶可以达到切缘阴性,腋窝淋巴 结可以分期,就可以接受手术治疗;如果手术能改 善患者的生活质量,也可以考虑手术治疗[49-52]。
4.8 其他
医生需根据是否需要快速控制疾病或症状来 选择治疗方法,同时还应考虑患者的经济因素、心 理因素、目前可采取的治疗措施以及患者本人的 意愿。鼓励患者加入临床研究,由于目前应用于 临床的新药大部分是针对分子靶点的治疗药物, 因此可以使患者明显获益。一般认为肿瘤患者最 好的治疗是参加临床研究,不仅可节省费用,更重 要的是可以尽可能早地获得新药治疗。
5 不同类型乳腺癌的治疗
5.1 激素受体阳性/HER2阴性进展期乳腺癌
目前认为,激素受体阳性乳腺癌是一种慢性疾 病,患者的生存时间长,预后好。大部分这类患者对 内分泌治疗敏感,治疗获益大,因此,推荐首选内分 泌治疗。由于CDK4/6*制剂抑**、氟维司群(500 mg)和 依维莫司等药物的临床证据,乳腺癌的内分泌治 疗迎来了前所未有的机会,使激素受体阳性乳腺 癌治疗的慢性病管理实至名归。但是,对于存在内脏危象、症状严重、明确存 在内分泌治疗耐药的患者,如果其在内分泌治疗 阶段出现疾病进展,可以首选化疗,以便快速减轻 或缓解临床症状,控制肿瘤发展,改善生活质量。也有部分专家认为,即使是激素受体阳性的患 者,也可以优先选择化疗,之后序贯内分泌治疗以 维持治疗效果,患者也可能会获益。所以,辩证地 考虑患者的治疗获益并使其经历更少的不良反 应,是临床选择治疗方案的基本原则[53-54]。临床研 究表明,CDK4/6 *制剂抑**可延长乳腺癌患者的无进 展生存时间,提高客观反应率,减少不良反应,其 疗效优于化疗药物,已成为目前进展期乳腺癌内 分泌治疗的一线标准治疗药物。激素受体阳性/HER2 阴性进展期乳腺癌治疗的基本原则为内分 泌治疗联合 CDK4/6 *制剂抑**,分型低危、寡转移可 选单用内分泌治疗(图1)。
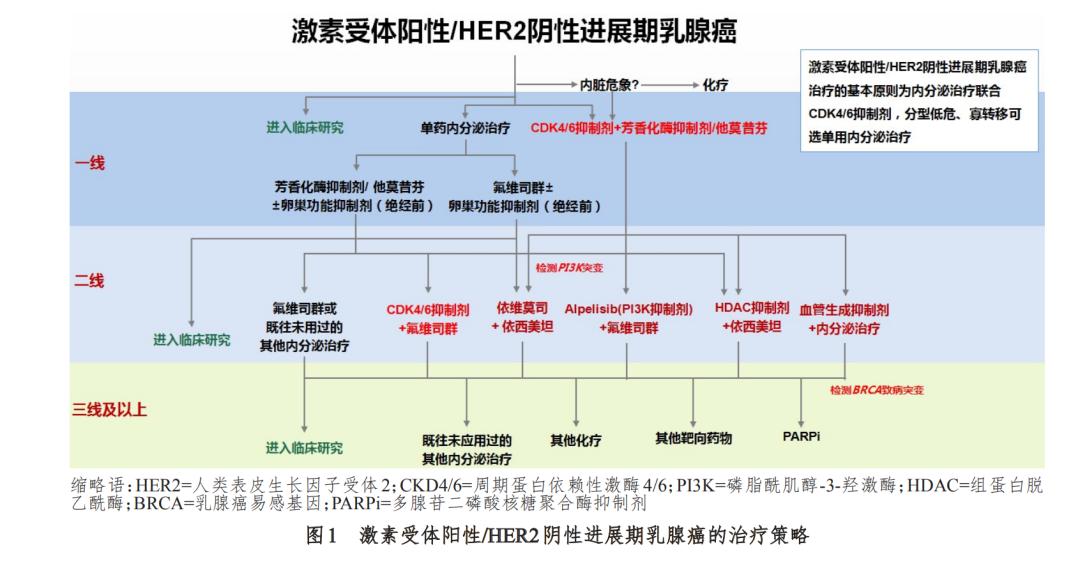
5.1.1 选择内分泌治疗的一般状况
如果没有 内 分泌耐药的证据或没有快速减轻肿瘤负荷的需 要,即使患者存在内脏转移,内分泌治疗也是激素 受体[ER和(或)PR]阳性进展期乳腺癌患者的首选 治疗方案。根据治疗的反应和患者的情况,可以 进行 2~3 线的内分泌治疗。对于进展期乳腺癌 患 者,医生在选择内分泌治疗药物时,一定要考虑患 者在辅助内分泌治疗阶段使用的内分泌药物的时 间和耐药情况[55]。对于无病生存时间大于 2 年、没 有内脏危象、无症状或症状很轻的激素受体阳性 患者,可优先选择内分泌治疗联合靶向治疗,通常 建议给予更少的化疗或者更少的化疗周期。不建 议内分泌治疗和化疗联合应用,但进展期乳腺患 者化疗后的内分泌维持治疗是一个合理的选择, 已在临床实践中被广泛应用。
5.1.2 常用的内分泌治疗药物
选择性雌激素受 体调节剂:他莫昔芬、托瑞米芬、氟维司群;芳香化 酶*制剂抑**:依西美坦、来曲唑、阿那曲唑;逆转内分 泌耐药或联合内分泌治疗的靶向药物:CDK4/6 抑 制剂、依维莫司。内脏危象的存在是化疗的明确 指征。内分泌治疗耐药性的证据是相对的,NCCN 指南确实指出,患者应在可行的情况下进行最多 3 种内分泌治疗。显然,如果对任何治疗均无反应, 则应将肿瘤视为“激素不敏感”。如果患者对先前 的治疗方法未显示任何激素敏感性证据,则选择 是否给予 3 种激素治疗将取决于转移的部位和程 度,以及临床医生是否认为患者有时间尝试另一 种内分泌药物或该疾病立即威胁生命。仅靠症状 可能不是选择化疗的原因,例如通过引流治疗胸 腔积液引起的呼吸困难应进行内分泌治疗,而由 于淋巴管炎癌变引起的呼吸困难应采用化疗。同 样,在等待内分泌治疗以控制肿瘤时,通常可以使 用适当的镇痛药物来控制骨痛。鉴于目前有许多 缓解症状的治疗方法,仅有部分患者因急需缓解 症状选择化疗。
5.1.3 绝经后患者内分泌治疗药物的选择
可以 选择 CDK4/6 *制剂抑**联合芳香化酶*制剂抑**、氟维司 群、他莫昔芬或托瑞米芬[56]。CDK4/6*制剂抑**+氟维 司群、CDK4/6*制剂抑**+芳香化酶*制剂抑**、西达本胺+ 依西美坦、氟维司群+依维莫司、依西美坦+依维莫 司、他莫昔芬+依维莫司等方案可供临床选择。在晚期解救性治疗方面,国内外共识一致推荐 芳香化酶*制剂抑**联合 CDK4/6 *制剂抑**作为激素受 体阳性/HER2 阴性晚期复发转移乳腺癌的一线标 准治疗。存在芳香化酶*制剂抑**治疗禁忌证、曾行 芳香化酶*制剂抑**辅助内分泌治疗且无病生存时间 短的患者,可选择氟维司群联合 CDK4/6 *制剂抑**作 为一线治疗方案。因经济原因或病状极轻、分型 极低危、寡病灶、寡转移的患者,可考虑选择内分 泌单药治疗[57-59]。对于一线内分泌单药治疗后进展的乳腺癌患 者,如芳香化酶*制剂抑**治疗失败,可采用氟维司群 联合 CDK4/6 *制剂抑**作为二线基本治疗方案,也可 以考虑单药氟维司群(每4周500 mg)。CDK4/6抑 制剂联合治疗失败后,可根据患者的实际情况,考 虑以下几种治疗方案:
①西达本胺联合依西美坦;
②依维莫司联合依西美坦、依维莫司联合氟维司群 或他莫昔芬[16, 60-62];
③内分泌治疗,可以选择他莫昔 芬、托瑞米芬、孕激素等;
④基因检测,如果PIK3CA 基因发生突变,可以考虑 PIK3CA *制剂抑**;如果 BRCA基因发生突变,可以选择PARPi;
⑤化疗。
5.1.4 绝 经 前 的 患 者
绝 经 前 患 者 通 常 采 用 CDK4/6 *制剂抑**联合他莫昔芬或托瑞米芬;如果患 者辅助治疗阶段应用过他莫昔芬,也可以考虑卵 巢功能完全抑制(包括药物性卵巢功能抑制),卵 巢功能完全抑制后加用芳香化酶*制剂抑**[63],基本治 疗原则与绝经后相似。这里要强调的是,对于 45 岁以下、未绝经的患者,在给予药物性卵巢功能抑 制加用芳香化酶*制剂抑**时要慎重,需要检测激素 水平(雌二醇和 FSH);因为如果卵巢功能不能被 完全抑制,该疗法的效果不佳。
5.1.5 激素受体和 HER2 均阳性的患者
对于激 素受体和 HER2 均阳性的患者,目前的标准治疗方 案是抗 HER2 治疗联合化疗。如果患者经济条件 允许,也可以考虑 CDK4/6 *制剂抑**联合内分泌治疗 及抗 HER2 治疗。研究表明,CDK4/6 *制剂抑**联合 内分泌治疗及曲妥珠单抗、吡咯替尼或拉帕替尼 等,均显示出了无进展生存时间的获益,尤其是无 化疗时间的延长[64-65]。TAnDEM 研究表明,曲妥珠 单抗联合阿那曲唑组患者的无进展生存时间明显 长于阿那曲唑单药组(4.8 个月 vs 2.4 个月,HR= 0.63,P=0.002);曲妥珠单抗联合阿那曲唑组患者的 总生存时间也长于阿那曲唑单药组(28.5 个月 vs 23.9 个 月),但 差 异 无 统 计 学 意 义(P=0.33)[64]。CDK4/6 *制剂抑**已被证实可以逆转内分泌治疗耐 药,增加内分泌治疗疗效。NA-PHER2研究是一项 单臂、Ⅱ期临床试验,结果显示,CDK4/6 *制剂抑**联 合氟维司群及曲妥珠单抗/帕妥珠单抗方案可进一 步提高ER阳性/HER2阳性乳腺癌患者的病理学完 全缓解率,97%(29/30)的患者获得了临床客观缓 解[66]。对于一些老年、无法耐受化疗的患者,抗 HER2药物联合内分泌治疗可以作为备选。
5.2 HER2阳性进展期乳腺癌
靶向治疗的特点是高效、低毒、耐受性好,能 够选择性地杀死肿瘤细胞,而对正常组织的影响 较小。最早应用于临床的抗 HER2 靶向治疗药物 是曲妥珠单抗。一项关于转移性乳腺癌一线治疗 的Ⅲ期临床研究显示,化疗联合曲妥珠单抗与单 纯化疗患者的肿瘤进展时间分别为 7.4 个月和 4.6 个月(P﹤0.001),反应的时间分别为 9.1 个月和 6.1 个月(P﹤0.001),总生存时间分别为 25.1 个月和 20.3 个月(P﹤0.01)[67]。基于该临床研究结果, 1998年曲妥珠单抗被美国FDA批准用于一线转移 性乳腺癌的治疗。另一篇文献报道曲妥珠单抗治疗 者的中位生存时间被提高到3.5年(3.0~4.4年)[68]。2002 年曲妥珠单抗在中国上市,其在早期乳 腺癌中可以降低 52%的复发风险。在转移性乳腺 癌中,曲妥珠单抗可以提高患者的总生存率,有些 患者可以获得更长的生存时间[29]。目前针对HER1 和 HER2 的小分子酪氨酸激酶*制剂抑**吡咯替尼和 拉帕替尼也在中国上市,其他的抗 HER2 治疗药物 还有帕妥珠单抗和 T-DM1。这些药物应用的一般 原则是,尽可能早地使患者接受抗 HER2 治疗,除 非有禁忌证。HER2 阳性进展期乳腺癌治疗的基 本原则为持续抗HER2治疗(图2)。
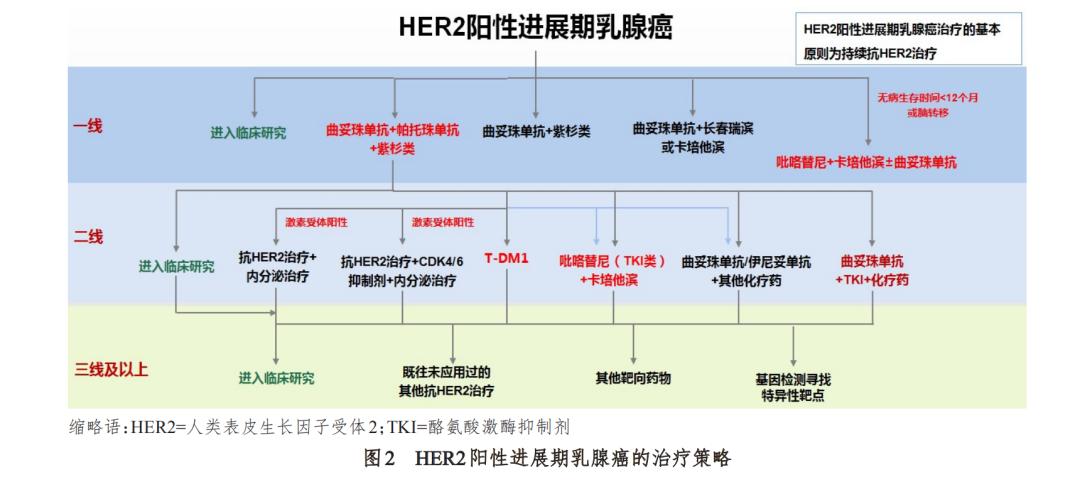
5.2.1 常用的抗 HER2 治疗药物
包括曲妥珠单 抗、吡咯替尼、拉帕替尼、帕妥珠单抗、T-DM1。对 于HER2阳性乳腺癌,化疗+曲妥珠单抗+帕妥珠单 抗是最佳的一线治疗方案,鉴于帕妥珠单抗在晚 期乳腺癌的治疗中未进入医保,费用昂贵,目前推 荐的一线治疗方案仍是化疗+曲妥珠单抗;对于无 化疗适应证的激素受体阳性患者,也可以考虑曲 妥珠单抗、吡咯替尼或拉帕替尼联合内分泌治 疗。对于曲妥珠单抗治疗失败的 HER2 阳性乳腺 癌,吡咯替尼、T-DM1 是最佳的治疗选择,但是 T-DM1 费用较高,因此可以选择吡咯替尼联合卡 培他滨,或继续使用曲妥珠单抗,仅更换化疗或内 分泌治疗方案,也可以考虑曲妥珠单抗联合吡咯 替尼的双靶向治疗。
5.2.2 抗 HER2 治疗失败后抗 HER2 药物的选择
因为对 HER2 通路的持续抑制是有益的,所以对于 抗 HER2 治疗联合化疗或内分泌治疗失败的患者, 通常会继续给予抗HER2治疗。至于是继续应用同 一种抗 HER2 治疗药物,还是选择另一种抗 HER2 治疗药物,需要根据之前治疗有效的时间而定。
5.2.3 进展期乳腺癌抗 HER2 治疗的时间
关于 进展期乳腺癌抗 HER2 治疗的时间,尤其是疾病处 于缓解阶段时,目前仍不明确。
5.3 三阴性进展期乳腺癌
三阴性进展期乳腺癌治疗的基本原则为化疗 和特异性靶向治疗(图3)。
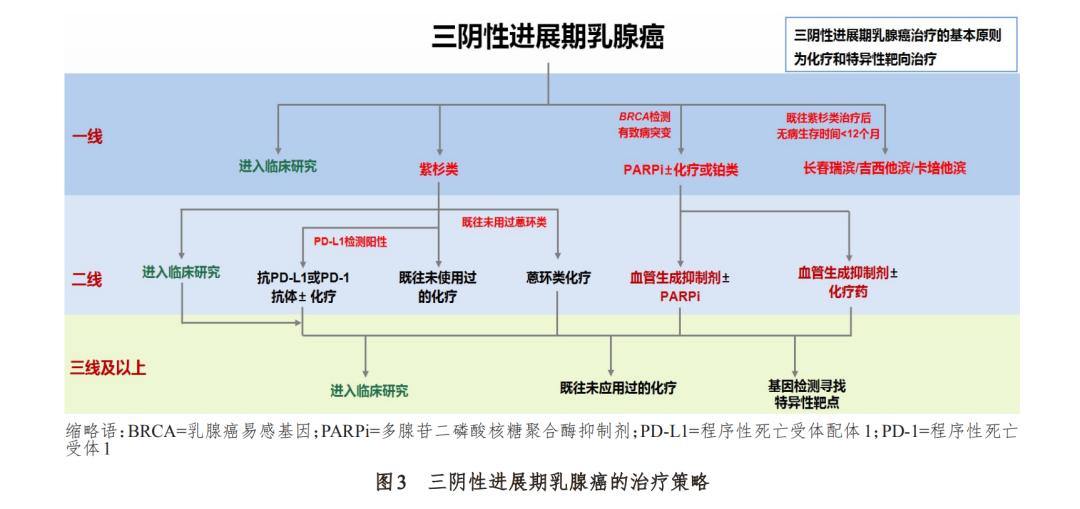
5.3.1 BRCA1 和 BRCA2 突变
BRCA 突变乳腺癌 患者仅占全部乳腺癌患者的3%~5%,因此,很难开 展针对 BRCA 突变转移性乳腺癌的大规模临床试 验。目前,在新辅助治疗领域,有部分研究探讨了 铂类药物对 BRCA 突变乳腺癌的作用。结果显示, 铂类药物可使 BRCA 突变乳腺癌患者的病理完全 缓解率显著提高。2014 年,在圣安东尼奥乳腺癌 会 议(San Antonio Breast Cancer Symposium, SABCS)中,有学者报道了一项卡铂对比多西他赛 一线治疗晚期三阴性乳腺癌或 BRCA1/2 突变乳腺 癌的临床研究(*NTT** 研究)。该研究纳入了 376 例 患者,中位随访 11.0 个月,结果显示,在未经选择 的三阴性乳腺癌患者中,两种药物的主要观察终 点(客观有效率)和次要观察终点(无疾病进展时 间)均相似,无显著差异。而在 43 例存在 BRCA 突 变的患者中,卡铂治疗组患者的客观有效率显著高 于多西他赛治疗组(68.0% vs 33.3%,P=0.03)[69- 70]。该研究提示,在未经选择的三阴性乳腺癌患者中, 卡铂和多西他赛的疗效没有差别,但在BRCA1/2突 变的患者中卡铂治疗存在优势。
5.3.2 PARPi 的使用
2014 年,PARPi 被美国 FDA 批 准 用 于 治 疗 BRCA1/2 突 变 的 卵 巢 癌 患 者 , BRCA1/2 基因突变可使细胞缺乏修复 DNA 双链损 伤的能力,从而为PARPi发挥“合成致死”作用奠定 了基础,与此同时该药对BRCA1/2突变乳腺癌的免 疫治疗也有效[20, 71]。目前 Olaparib 已在国内上市, 主要用于治疗 BRCA 突变相关的进展期三阴性乳 腺癌。在 OlympiAD 临床研究中,Olaparib 与化疗 相比可有效延长乳腺癌患者的无进展生存时间 (7.0 个月 vs 4.2 个月,HR=0.58,P﹤0.001),改善患 者的生活质量,且不良反应较少,其中三阴性乳腺 癌患者的获益最大[72]。
5.3.3 PD-L1免疫治疗
PD-L1*制剂抑**可能在三阴 性乳腺癌的治疗及新辅助治疗中发挥作用。部分 Ⅰ~Ⅲ期临床试验证实了PD-L1*制剂抑**在转移性三 阴性乳腺癌治疗中的安全性和有效性[73-75]。PD-L1 阳性表达、肿瘤负荷较重、肿瘤浸润较多的患者可 考虑免疫治疗。Ⅲ期临床试验 IMpassion130 首次 证实了免疫治疗可使 PD-L1 阳性的转移性三阴性 乳腺癌患者获益,阿替唑单抗联合白蛋白结合紫 杉醇组患者的无进展生存时间明显长于安慰剂联 合白蛋白结合紫杉醇组(7.2 个月 vs 5.5 个月,HR= 0.8,P=0.0025),在 12.9 个月的随访中,接受上述两 种治疗方法的 PD-L1 阳性患者的中位生存时间分 别为25.0个月和15.5个月[76]。
5.3.4 三阴性乳腺癌的特殊性
对于辅助治疗阶 段曾经接受过蒽环类和紫杉类药物治疗的患者, 如果不能入组临床试验,可以考虑铂类药物为基 础的治疗。国外也有指南推荐,对于既往未接受 过蒽环类和紫杉类药物治疗的三阴性局部晚期乳 腺癌患者,可以首选蒽环类和紫杉类药物化疗。
6 进展期乳腺癌常用药物
6.1 CDK4/6*制剂抑**
该药为口服、靶向制剂,能够选择性地抑制CDK4/6 的活性,从而抑制肿瘤细胞增殖。2015 年 3 月 2 日,美国 FDA 批准帕博西尼(Palbociclib)联 合来曲唑作为ER阳性/HER2阴性绝经后晚期乳腺 癌的初始治疗方案,帕博西尼成为了全球首个上 市的 CDK4/6 *制剂抑**[77]。与来曲唑单药治疗相比, 帕博西尼联合来曲唑初治ER阳性/HER2阴性绝经 后晚期乳腺癌时,可将患者的无进展生存时间从 10.2个月延长到20.2个月,但并未带来总生存时间 的不同[17, 78]。2017年3月13日和2017年9月28日, CDK4/6*制剂抑**瑞博西尼(Ribociclib)[79] 和阿贝西尼 (Abemaciclib)[80] 先后上市。
6.1.1 CDK4/6 *制剂抑**在复发乳腺癌一线治疗中的应用
CDK4/6*制剂抑**一线治疗复发乳腺癌的疗效 已在多项Ⅲ期临床试验中得到验证。Ⅲ期临床试 验 PALOMA-2 共纳入 666 例绝经后 ER 阳性/HER2 阴性的亚裔乳腺癌患者,结果显示,帕博西尼联合 来曲唑组患者的中位无进展生存时间长于安慰剂 联合来曲唑组(25.7 个月 vs 13.9 个月)[81]。Ⅲ期临 床试验 MONALEESA-2 纳入了 668 例绝经后激素 受体阳性 HER2 阴性的复发/转移乳腺癌患者,结 果显示,瑞博西尼联合来曲唑组患者的中位无进展 生存时间长于安慰剂联合来曲唑组(25.3 个月 vs 16.0 个月),进展和死亡风险减少了 43.2%(HR= 0.568,P=9.63 × 10- 8)[79]。Ⅲ 期 临 床 试 验 MONARCH3 纳入了 493 例未经系统性治疗的绝经后激 素受体阳性 HER2 阴性进展期乳腺癌患者,结果显 示,阿贝西尼联合非甾体类芳香化酶*制剂抑**组患 者的中位无进展生存时间长于安慰剂联合非甾体 类芳香化酶*制剂抑**组(28.18 个月 vs 14.76 个月, HR=0.540,P=0.000002)[80]。
6.1.2 CDK4/6 *制剂抑**在复发乳腺癌二线治疗中的应用
多项研究显示 CDK4/6 *制剂抑**联合氟维司 群可以作为激素受体阳性 HER2 阴性绝经后进展 期乳腺癌患者二线治疗的新选择。Ⅲ期临床试验 PALOMA-3 纳入了激素受体阳性 HER2 阴性且在 既往内分泌治疗中进展的晚期乳腺癌患者,结果 显示,帕博西尼联合氟维司群组和安慰剂联合氟 维司群组患者的中位无进展生存时间分别为 9.5 个月和4.6个月[10, 82]。2016年美国FDA批准帕博西 尼联合氟维司群用于治疗激素受体阳性 HER2 阴 性且在既往内分泌治疗中进展的进展期乳腺癌患 者[8]。另一项研究显示,帕博西尼联合氟维司群治 疗与氟维司群单药治疗患者的中位生存时间分别 为 34.9 个月和 28.0 个月,前者的生存获益为 6.9 个 月,但差异无统计学意义[83]。Ⅲ期临床试验 MONALEESA-3纳入了345例未经治疗或经一线内分泌 治疗进展的绝经后激素受体阳性 HER2 阴性的乳 腺癌患者,结果显示,瑞博西尼联合氟维司群组患 者的中位无进展生存时间长于氟维司群单药组 (20.5 个月 vs 12.8 个月,HR=0.593,P﹤0.001)[84],总 生存率(overall survival,OS)高于氟维司群单药组 (42个月的OS分别为57.8%和45.9%)[85]。
6.1.3 CDK4/6 *制剂抑**作为一线药物在绝经前晚期
乳腺癌中的应用 Ⅲ期临床试验 MONALEESA-7 纳入了绝经前激素受体阳性 HER2 阴性的进展期 乳腺癌患者,结果显示,瑞博西尼+他莫昔芬或非 甾体类芳香化酶*制剂抑**+戈舍瑞林组患者的中位 无进展生存时间长于安慰剂+他莫昔芬或非甾体 类芳香化酶*制剂抑**+戈舍瑞林组(23.8 个月 vs 13.0 个月,HR=0.55,P﹤0.0001)[86],且 OS 高于安慰剂+ 他莫昔芬或非甾体类芳香化酶*制剂抑**+戈舍瑞林 组(42 个月的 OS 分别为 70.2%和 46.0%,HR=0.71, P=0.00973)。不同种族的总体生存率差异很大,几 乎所有的受益都来自于少数亚洲人群,而几乎占研 究病例三分之二的非亚洲人群则没有任何益处[87]。Ⅲ期临床试验 MONARCH-2 纳入了 669 例既往接 受内分泌治疗进展的激素受体阳性HER2阴性进展 期乳腺癌患者,结果显示,阿贝西尼联合氟维司群 组患者的中位无进展生存时间长于氟维司群单药 组(16.4 个月 vs 9.3 个月,HR=0.553,P﹤0.001)[88], 中位总生存时间也长于氟维司群单药组(46.7 个 月vs 37.3个月,HR=0.757,P=0.0137)[89]。6.2 氟维司群 该药为雌激素受体拮抗剂,有两种给药方式, 低剂量氟维司群(每 4 周 250 mg)和高剂量氟维司 群(每4周500 mg),高剂量氟维司群较低剂量氟维 司群治疗可显著延长患者的中位无进展生存时间 (23.4个月vs 13.1个月),且耐受性良好。高剂量氟 维司群(每 4 周 500 mg)目前也被推荐用于绝经后 患者的一线内分泌治疗[90-92]。对于存在 PI3KCA 突 变的患者,Ⅲ期临床研究 SOLAR-1 显示,α特异性 PI3K *制剂抑** Alpelisib 与氟维司群联合治疗晚期激 素受体阳性/HER2 阴性乳腺癌较单独氟维司群治 疗可显著延长患者的中位无进展生存时间(11 个 月 vs 5.7 个月,HR=0.65,P﹤0.001),而 PI3KCA 未 突变的患者无获益[93]。该 PI3K *制剂抑**已被美国 FDA 批准上市,并已在 2020 年 3 月提交国内临床 试验申请。
6.3 依维莫司
依维莫司是哺乳动物雷帕霉素靶蛋白(mammalian target of rapamycin,MTOR)*制剂抑**。基础研 究显示依维莫司能够逆转内分泌治疗耐药。基于 BOLERO-2 研究的结果,2012 年美国 FDA 批准依 维莫司联合依西美坦治疗非甾体类芳香化酶抑制 剂治疗失败的绝经后激素受体阳性、HER2 阴性的 晚期乳腺癌患者。BOLERO-2研究是一项随机、双盲、安慰剂对照的Ⅲ期临床试验,纳入了 724 例具 备上述适应证的绝经后女性患者,结果显示,依维 莫司联合依西美坦组患者的中位无进展生存时间 较安慰剂联合依西美坦组显著延长(7.8个月vs 3.2 个月,HR=0.45,P﹤0.0001),独立中心评估的结果 分别为11.0个月和4.1个月(HR=0.38,P﹤0.0001), 且无论是整体人群还是前瞻定义的各个亚组(包括 内脏转移的患者,在辅助治疗完成后12个月内复发 的患者)都得出类似的结果;但联合依维莫司在增 强疗效的同时也增加了口腔炎、贫血和呼吸困难等 不良反应的发生率,最常见的3~4级不良反应为口 腔炎(8% vs 1%)、贫血(6% vs ﹤1%)、呼吸困难 (4% vs 1%)、高血糖(4% vs ﹤1%)、疲乏(4% vs ﹤ 1%)和肺炎(3% vs 0%)[61]。因此,医生为患者选择 依维莫司联合芳香化酶*制剂抑**治疗要权衡疗效和 不良反应,根据具体情况进行个体化治疗。
6.4 单克隆抗体
6.4.1 曲妥珠单抗(赫赛汀,汉曲优)
目前进展期 乳腺癌的一线治疗方案是化疗+曲妥珠单抗+帕妥 珠单抗[94-95]。因帕妥珠单抗治疗晚期乳腺癌未在 医保范围,因此也可以选择化疗联合曲妥珠单 抗。在辅助治疗和新辅助治疗阶段接受过曲妥珠 单抗治疗的患者,如果无病生存时间超过 1 年,也 可以考虑复发转移后接受曲妥珠单抗治疗。汉曲 优最新的临床研究结果显示,治疗后 24 周患者的 客观缓解率为71.0%[96]。对于曲妥珠单抗治疗进展的患者,医生通常会 根据治疗的周期数考虑曲妥珠单抗的继续使用, 而仅改变联合用药,如化疗或内分泌治疗;也可以 选择:①曲妥珠单抗联合帕妥珠单抗及化疗,吡咯 替尼联合卡培他滨,T-DM1;②拉帕替尼+卡培他 滨;③曲妥珠单抗+酪氨酸激酶*制剂抑**[97-99]。曲妥珠单抗通常不与蒽环类药物联合应用,因 其会增加心*毒脏**性[67]。
6.4.2 帕妥珠单抗
HER2阳性转移性乳腺癌的一 线治疗可以选择化疗+曲妥珠单抗+帕妥珠单抗联 合治疗方案。CLEOPATRA 研究结果显示,一线治疗中,曲 妥珠单抗+帕妥珠单抗+多西他赛组患者的中位无 进展生存时间显著长于曲妥珠单抗+多西他赛组 (18.5个月vs 12.4个月,P﹤0.001),1年生存率分别 为 23.6%和 17.2%;证实化疗+曲妥珠单抗+帕妥珠 单抗方案较化疗+曲妥珠单抗方案有明显的生存 获益。另有研究结果显示帕妥珠单抗不能单独发 挥作用,而需要与曲妥珠单抗联合应用[100-101]。
6.4.3 伊尼妥单抗(塞普汀)
是中国自主研发的 注射用重组抗 HER2 人源化单克隆抗体“仿创结 合”新药。中国一项多中心随机对照Ⅲ期临床研 究证实,伊尼妥单抗联合长春瑞滨治疗HER2 阳性 晚期乳腺癌具有显著的疗效和安全性,该研究共 纳入 315 例患者,其中试验组 212 例(采用伊尼妥 单抗联合长春瑞滨治疗),对照组103例(采用长春 瑞滨治疗),结果显示,试验组和对照组患者的中 位无进展生存时间分别为 39.1 周和 14.0 周[102]。2020 年 6 月 17 日,国家食品药品监督管理局已正 式批准伊尼妥单抗上市。
6.4.4 贝伐珠单抗
美国 FDA 先批准后又撤回了 贝伐珠单抗用于乳腺癌治疗的批准,欧洲药品管 理局(European Medicines Agency,EMA)人用医疗 产品委员会(Committee for Medicinal Products for Human Use,CHMP)目前批准的适应证包括:
①贝 伐珠单抗联合紫杉醇一线治疗转移性乳腺癌;
② 不适合紫杉类和蒽环类药物治疗的转移性乳腺 癌,可考虑给予贝伐珠单抗联合卡培他滨一线治 疗。
贝伐珠单抗仅有无进展生存时间获益,无总 生存时间获益,且目前没有贝伐珠单抗治疗疗效 的预测因子。因此,贝伐珠单抗仅可作为一线治 疗或二线治疗的一种选择,并且不推荐其在二线 以上的治疗中使用[103-108]。
6.5 酪氨酸激酶*制剂抑**
6.5.1 吡咯替尼
该药是一种口服、不可逆的酪氨 酸激酶*制剂抑**,同时具有抗表皮生长因子受体 (epidermal growth factor receptor,EGFR)/HER1、 HER2 以及HER4 的活性。一项Ⅱ期临床试验结果 显示,吡咯替尼+卡培他滨组患者的客观反应率高 于拉帕替尼+卡培他滨组(78.5% vs 57.1%),中位无 进展生存时间长于拉帕替尼+卡培他滨组(18.1 个 月vs 7.0个月),疾病死亡风险降低63.7%;且吡咯替 尼的真实世界研究也获得了很好的疗效[109]。另有 研究表明,吡咯替尼的耐受性优于拉帕替尼[110]。2018 年吡咯替尼凭借Ⅱ期临床数据被有条件批准 于中国上市。
6.5.2 拉帕替尼
该药通常被用于曲妥珠单抗治 疗失败的患者,尤其是曲妥珠单抗治疗中出现脑 转移的患者,常用方案为曲妥珠单抗联合拉帕替 尼。一项Ⅲ期临床试验(EGF100151)评价了拉 帕替尼联合卡培他滨的疗效,该研究入组了曲 妥珠单抗治疗失败、既往接受过含蒽环类或紫 杉类药物治疗的患者,结果显示,拉帕替尼+卡 培他滨联合治疗组患者的中位肿瘤进展时间为 27.1 周,明显长于卡培他滨单药治疗组的 18.6 周 (P﹤0.001)[111-115]。
6.6 T-DM1
该药可使曲妥珠单抗一线治疗失败的转移性 乳腺癌患者获得生存获益。EMILIA 研究比较了 T-DM1 和拉帕替尼+卡培他滨在二线治疗中的疗效,证实曲妥珠单抗一线治疗失败的HER2 阳性乳 腺癌可优先选择 T-DM1[116]。美国 FDA 于 2013 年 2 月正式批准 T-DM1 作为治疗 HER2 阳性进展期乳 腺癌的药物,国内已于2020年初批准T-DM1上市。
6.7 西达本胺(Tucidinostat)
该药是一种口服苯甲酰胺类组蛋白脱乙酰酶 (histone deacetylase,HDAC)抑 制 剂 ,具 有 抑 制 HDAC1、HDAC2、HDAC3 和 HDAC10 特异性亚型 的作用,在中国已被批准用于治疗复发或难治 性 外周T细胞淋巴瘤。既往研究显示,与其他非选择 性 HDAC *制剂抑**不同,西达本胺+恩替诺特可通过 激活特异性自然*伤杀**细胞和抗原特异性细胞毒性 T 细胞来增强肿瘤的免疫监视作用。西达本胺还 能够阻断雌激素非依赖性生长因子信号通路并恢 复其对雌激素药物的敏感性。ACE 研究主要针对 绝经后、既往接受过内分泌治疗的 ER 阳性/HER2 阴性晚期乳腺癌患者,在经筛选的 443 例患者中, 随机入组365 例,分为西达本胺联合依西美坦治疗 组和安慰剂联合依西美坦治疗组,结果显示,西达 本胺联合依西美坦治疗组患者的中位无进展生存 时间长于安慰剂联合依西美坦治疗组(7.4 个月 vs 3.8个月),客观缓解率和临床获益率也均优于安慰 剂联合依西美坦治疗组,且不良反应可管理[117]。
7 化疗
7.1 化疗适应证
化疗适应证:激素受体阴性的患者,有症状的 内脏转移患者,激素受体阳性但对内分泌治疗耐 药的患者。7.2 化疗方式选择 联合化疗和单药序贯化疗都是合理的选择。化疗药物的联合应用及序贯应用在临床工作中均 可选择,已有多项研究表明患者对单药序贯治疗 的耐受性更佳,且两者的总生存时间相似。基于 现有数据,专家组推荐优选单药序贯化疗;对于病 情进展迅速、存在内脏危象或需要迅速缓解症状、 控制疾病进展的患者,可选择联合化疗。
7.3 化疗药物选择的一般原则
对没有禁忌证,既往未接受过蒽环类或紫杉类 药物辅助治疗的患者,通常选择蒽环类或紫杉类 药物为基础的化疗方案,其他可选择的药物有长 春瑞滨[118]、吉西他滨[119]、卡培他滨[120]、脂质体多柔 比星、白蛋白结合型紫杉醇[121-122]、顺铂和卡铂等。
7.4 化疗中需要特别关注的问题
对蒽环类药物耐药或出现蒽环类药物的剂量 累积毒性(如心*毒脏**性)而未用过紫杉类药物的患 者,后续化疗通常选择以紫杉类药物为基础的方 案,也可以选择紫杉类单药方案。对于 HER2 阳性 的局部晚期乳腺癌患者,专家组建议序贯使用蒽 环类药物与抗 HER2 药物,不建议同时联合使用。对在辅助治疗中使用过紫杉类药物的患者,特别 是无病生存时间至少超过1年的患者,一线治疗时 可再次使用紫杉类药物。
7.5 化疗有效后的维持
专家组建议:应该根据对每位患者具体情况的 评估结果予以个体化的治疗,包括对每种方案持 续时间(周期数)的评估和对患者能否接受多线化 疗的评估。有荟萃分析表明,一线治疗的持续时 间长可轻度延长患者的总生存时间,可显著延长 无进展生存时间;所以这种治疗可持续应用直至 疾病进展或出现不可耐受的不良反应(不可耐受 的不良反应应由患者和医生共同判断)[123]。目前, 大量临床试验已证明卡培他滨适合用于维持治 疗,其还具有口服给药、应用方便的特性。此外, 对于激素受体阳性的患者,内分泌维持治疗也是 很好的选择[124-125]。
7.6 抗HER2治疗联合化疗
在晚期乳腺癌的治疗中,可采用贝伐珠单抗联 合化疗,但要选择合适的患者,谨慎应用。E1193 是一项随机对照临床研究,共纳入739 例转移性乳 腺癌患者,被随机分为多柔比星+紫杉醇联合治疗 组、多柔比星治疗进展后序贯紫杉醇治疗组和紫杉 醇治疗进展后序贯多柔比星组,结果显示,多柔比 星+紫杉醇联合治疗组患者的客观缓解率和无进展 生存时间均优于单药序贯治疗组,但3组患者的总 生存时间比较,差异无统计学意义(P﹥0.05)[126]。一项荟萃分析显示,单药序贯化疗具有延长无进展 生存时间的优势,虽然联合化疗组患者的客观有效 率明显增高,但未明显延长无进展生存时间[127]。两 个研究均显示联合治疗组的不良反应风险较高 (粒细胞缺乏性发热风险显著增高)。
8 不能手术的局部晚期乳腺癌
8.1 诊治原则
针对不能手术的局部晚期乳腺癌患者,首先要 给予粗针穿刺活检,以明确病理诊断,并使用免疫 组化法检测 ER、PR、HER2 和 Ki-67 等生物学指标;另外,还要给予全面的分期检查。因为此类患者容 易存在远处转移,所以专家组推荐优先选择胸部 CT和腹部CT检查,而不是胸部X线平片和腹部超 声检查,也可以考虑 PET-CT 检查。局部晚期乳腺 癌的治疗应强调多学科综合治疗,包括全身性治 疗、手术和放疗,目的是获得局部控制和长期生存。
8.2 新辅助治疗后的手术治疗
在经全身治疗和(或)放疗等有效的新辅助治 疗后,部分患者可获得手术机会。大部分患者可 以进行乳腺切除联合腋窝淋巴结清扫术,小部分 疗效较好的患者可以考虑进行保乳手术。8.3 局部晚期炎性乳腺癌的治疗 专家组建议:局部晚期炎性乳腺癌的治疗可与 局部晚期非炎性乳腺癌相似,首先选择全身治 疗。在后续手术方式的选择上,对于大部分患者, 即使是全身治疗效果较好的患者,也推荐进行乳 腺切除联合腋窝淋巴结清扫术。不推荐术后立即 进行局部重建手术,即使获得病理学完全缓解,也 需给予局部放疗(胸壁+淋巴结引流区)[49-52]。
9 特殊转移部位的治疗
9.1 肝转移
目前亟需前瞻性、随机对照临床试验来评价乳 腺癌肝转移局部治疗的价值。因为尚无随机对照 临床试验的数据提示肝转移病灶的局部治疗能够 延长患者的生存时间,所以在进行局部治疗前,医 生必须告知患者这一事实。局部治疗仅适用于身 体状况好、转移部位局限于肝、无肝外转移病灶且 全身治疗效果好的患者;需要综合考虑各种治疗 方式,包括手术、立体定位放疗、肝内灌注化疗或 其他治疗方式。有文献报道,39 例乳腺癌肝转移 患者接受肝转移灶切除术,中位随访60个月,从肝 病灶切除开始,患者的无病生存时间和总生存时 间分别为 29.4 和 43.0 个月,1、3、5 个月生存率分别 为 84.6%、64.1%和 38.5%,提示外科手术切除能够 延长此类患者的长期生存时间[103]。
9.2 恶性胸腔积液
恶性胸腔积液需要全身治疗联合或不联合局 部治疗。胸腔积液的患者必须进行胸腔穿刺来明 确诊断,有症状的患者建议接受胸腔积液引流。恶性胸腔积液患者虽然可以考虑接受胸腔灌注药 物治疗,包括顺铂、博来霉素、生物调节剂等,但其 最佳治疗方式仍有待临床试验的进一步探索。
9.3 胸壁和区域淋巴结复发
9.3.1 手术治疗
胸壁转移或区域淋巴结复发的 患者很可能同时存在远处转移,因此,需要接受包 括胸部、腹部和骨骼检查在内的全面分期检查。当评估结果提示手术风险小且可行时,此类患者 可接受手术治疗。
9.3.2 放射治疗
复发区域未经放疗的患者可接 受局部区域的放疗。对于复发区域接受过放疗的 患者,胸壁复发区域的再次放疗需慎重考虑,仅适 用于个别患者。
9.3.3 药物治疗
针对仅局部复发而无远处转移 的患者,在局部手术联合或不联合放疗治疗后,建 议行化疗、内分泌治疗和(或)抗 HER2 治疗的全身 治疗。在首次出现局部复发的患者中,激素受体阴性 患者进行全身化疗可以改善预后,激素受体阳性 患者进行内分泌治疗可以改善预后。全身治疗方式的选择应根据肿瘤生物学特征、 既往治疗情况、无病生存时间和患者自身因素(如 伴随疾病和患者意愿等)来决定。
9.3.4 姑息治疗
对不能进行根治性局部治疗的 患者,姑息性的全身治疗应遵循转移性乳腺癌的治 疗原则。这些患者也可接受姑息性的局部治疗。
9.4 骨转移
9.4.1 药物治疗
有骨转移的转移性乳腺癌患者 应在全身治疗中常规联合使用骨改良药物(如双 膦酸盐、地诺单抗)。
9.4.2 手术或放疗
当骨转移灶引发患者持续的 或固定部位的疼痛时,需进行影像学检查以明确 病理性骨折的发生情况(将要发生或已发生)。如 果病理性骨折位于长骨,可予以外科固定及后续 放疗,并需要进行整形外科的评估。如果疼痛部 位没有明确的骨折风险,可进行放射治疗。
9.5 脑转移
9.5.1 脊髓压迫的处理
脊髓压迫属于肿瘤急 症,如果出现相应的神经系统症状及体征,应立 即检查并进行处理。医生应对可能受压的部位 及邻近部位进行充分的影像学检查,推荐采用 MRI 检查。一旦出现脊髓压迫,需要急诊外科 (神经外科或整形外科)评估是否予以外科减压;如果不能实施减压/固定术,可予以急诊放疗或 椎体成形术。
9.5.2 某些特殊情况的处理
对孤立的或数目有 限的、有切除可能的脑转移灶,可进行外科切除或 放射治疗,对某些不可切除的脑转移也可进行放 射治疗。
9.5.3 局部治疗的选择
HER2阳性脑转移的转移 性乳腺癌患者的生存时间可长达几年,应避免治 疗所致的长期毒性作用。在合适的情况下(如脑 转移灶的数目较少),不良反应较小的局部治疗 (如立体定向放疗)相对于全脑放疗可作为首选。
9.5.4 脑转移的发生情况
转移性乳腺癌患者脑 转移的发生率为5%~16%,且不同亚型间的发生率 不同,三阴性乳腺癌和 HER2 阳性乳腺癌脑转移的 发生率较高[128]。
9.5.5 脑转移的主要治疗原则
一部HER2阳性乳 腺癌脑转移治疗指南推荐的主要原则包括:
①预 后良好且仅有单个病灶的脑转移患者,可根据转 移灶的大小、手术切除的可行性和有无症状,选择 下述5种方式进行治疗:局部手术联合术后放射治 疗;立体定向放射手术(stereotactic radiosurgery, SRS);全 脑 放 射 治 疗(whole brain radiotherapy, WBRT),联合或不联合 SRS;分次立体定向放射治 疗(fractionated stereotactic radiotherapy,FSRT);SRS,联合或不联合WBRT。治疗后,推荐每2~4个月进行 1 次脑部 MRI 检查以监测脑转移情况。
② 预后良好且转移灶数目有限(2~4 个)的患者,治疗 选择包括有症状且较大病灶的手术治疗联合术后 放疗,对其他较小的病灶则行 SRS;WBRT,联合或 不联合 SRS;SRS,联合或不联合 WBRT。具体治 疗的选择取决于转移灶可否切除和有无症状。
③ 存在弥漫性病灶或广泛转移但预后相对较好的患 者 ,以 及 有 症 状 的 软 脑 膜 转 移 患 者 ,可 采 用 WBRT。
④ 预 后 较 差 的 患 者 ,指 南 建 议 采 用 WBRT、最佳支持治疗和(或)姑息治疗。10 支持和姑息治疗 专业的支持和姑息治疗,特别是控制症状的治 疗,在进展期乳腺癌的治疗中发挥至关重要的作用。该领域主要关注的是有效的镇痛治疗,包括使用足量 的*啡吗**。疼痛治疗药物,如*啡吗**及其具有较高性价比 的衍生物,对肿瘤相关症状的控制十分重要。