BioMarin公司近日宣布,欧盟委员会(EC)已授予VOXZOGO(vosoritide,研发代码BMN111)上市许可。VOXZOGO(vosoritide)是一种每日注射一次的药物,用于治疗2岁至生长板闭合期间的儿童软骨发育不全,生长板闭合发生在儿童达到最终成人身高时的青春期之后。

软骨发育不全
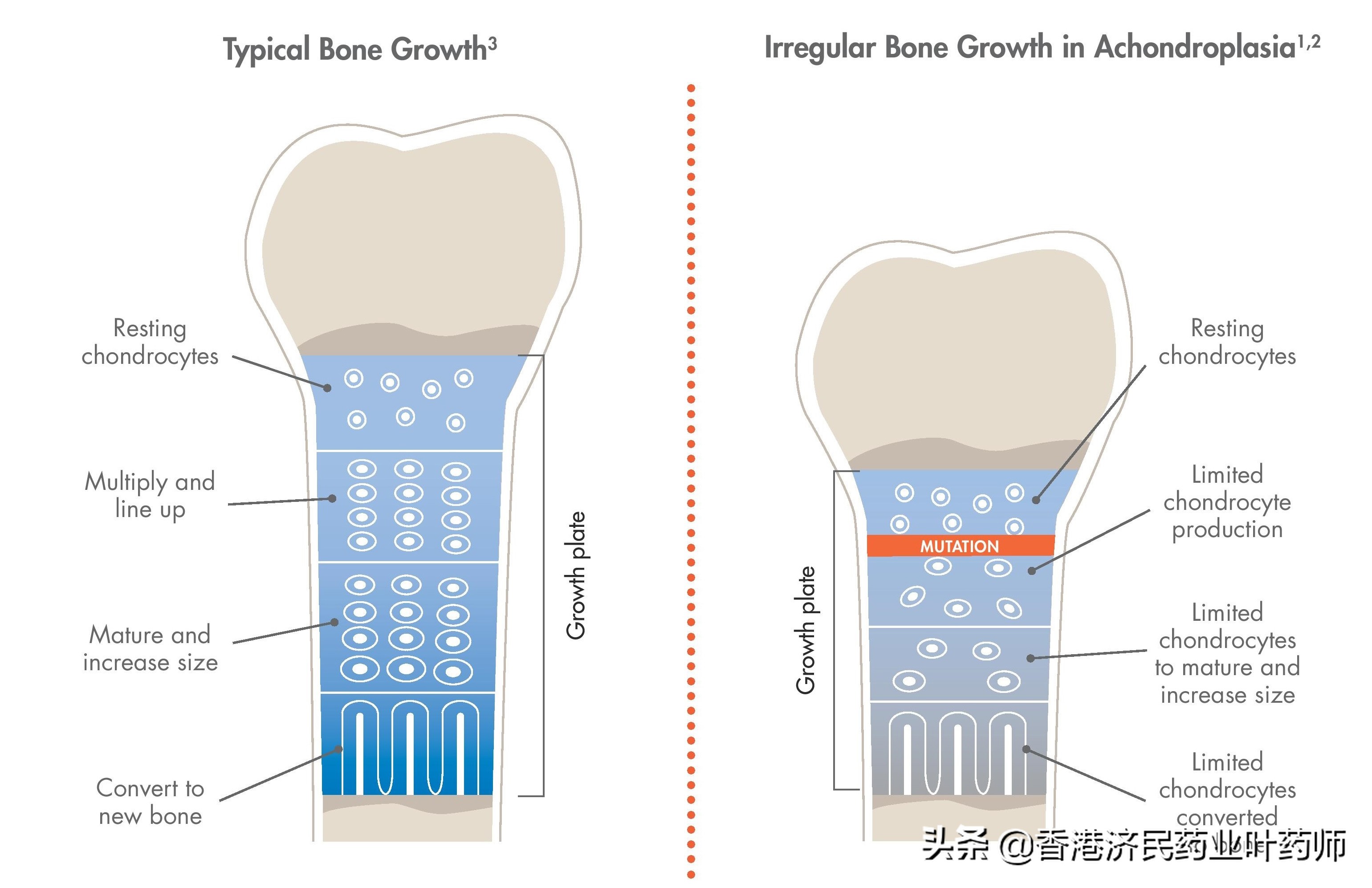
软骨发育不全症与Voxzogo作用机制
软骨发育不全症是人类中最常见的不成比例的身材矮小(侏儒症的常见亚型),其特征是软骨内骨化减慢,导致长骨、脊柱、面部和颅底不成比例的短小和结构紊乱。这种情况是由成纤维细胞生长因子受体3基因(FGFR3)突变引起的,FGFR3是骨生长的负调节因子。
Voxzogo是欧洲第一种被批准用于治疗儿童软骨发育不全的药物。Voxzogo是一种经修饰的C型利钠肽(CNP),通过下调成纤维细胞生长因子受体3 (FGFR3)信号通路从而促进软骨内骨形成,直接靶向作用于软骨发育不全的病理生理基础。
Voxzogo临床数据
EC的决定基于Voxzogo临床开发项目的全部数据,包括评估Voxzogo疗效和安全性的随机、双盲、安慰剂对照3期研究的结果。
3期研究进一步得到了正在进行的2期剂量测定研究的长期安全性和有效性的支持。该研究显示,在目前有数据可查的整个五年观察期内,未治疗的软骨发育不全儿童的增长率一直保持在参与者的基线增长率之上,并高于预期的年增长率。
没有观察到骨龄的加速,这表明Voxzogo并没有减少生长的总持续时间。该数据包包括正在进行的婴幼儿2期随机双盲研究的结果,包括广泛的药代动力学和生物标志物数据,以及来自2至5岁队列参与者的初步生长数据。
哨兵(sentinel)研究参与者的数据显示,在2至5岁的受试者中进行为期两年的Voxzogo治疗后,对生长有积极影响。此外,数据包还包括3期扩展研究的数据和大量自然历史数据。

全球性3期研究
全球性3期研究共入组了121例年龄在5-14岁、生长板依然开放的软骨发育不全症儿童患者,评估了Voxzogo与安慰剂的疗效和安全性。这些患者在进入3期研究之前,至少完成了6个月的基线研究,以确定其各自的基线生长速度。在3期研究中,患者随机分配,接受为期52周的Voxzogo(15ug/kg/天)或安慰剂治疗。主要终点是,与安慰剂相比,Voxzogo治疗的儿童在为期一年治疗期间生长速度相对基线的变化。
结果显示,研究达到了主要终点:治疗一年后,经安慰剂校正,Voxzogo治疗的生长速度相对基线的变化为1.6厘米/年(p<0.0001)。该结果与所研究的广大患者群体中的结果一致。研究中,Voxzogo的一般耐受性良好,无临床上显著的血压下降。
Voxzogo安全性
Voxzogo在所有剂量下通常耐受良好,全球已对儿童进行了约38,000次注射。大多数不良事件(AE)为轻度,未报告与研究药物相关的严重不良事件(SAE)。在所有剂量中,注射部位反应和低血压是最常见的药物相关AE。所有注射部位反应事件均为短暂性的。
低血压AE为轻度和短暂性的,大多数无症状,并且在具有最小临床影响的常规血压测量的背景下报告。未观察到新的安全性发现。没有与不成比例的骨生长或骨病理学相关的AE。没有证据表明骨年龄加快(由不考虑受试者年龄的放射科医生评估)或骨矿物质密度出现负面变化。
目前,美国FDA正在审查Voxzogo新药申请(NDA),处方药用户费法案(PDUFA)的目标生效日期为2021年11月20日。今年早些时候,该公司成功结束了对Voxzogo生产设施的食品和药物管理局现场预批准检查。
此外,Voxzogo接受了FDA和EMA的孤儿药物指定,用于治疗儿童软骨发育不全。孤儿药物指定计划旨在推进对有望诊断和/或治疗罕见疾病或状况的产品的评估和开发。
香港济民药业叶药师认为:“Voxzogo的监管批准是基于身高增长的改善,对软骨发育不全患者群体来说是一个重要的里程碑,其为该群体提供了有意义的靶向治疗方案。”
参考来源:European Commission Approves BioMarin's VOXZOGO® (vosoritide) for the Treatment of Children with Achondroplasia from Age 2 Until Growth Plates Close
注:以上资讯整理自网络,旨在帮助患者了解国际新药动态,不作任何用药依据,具体用药指引请咨询主治医师。